概要
急性肺栓塞(APE)的特征在于许多临床表现,这是不同器官之间复杂相互作用的结果;因此症状是多种多样的,并且是复杂临床表现的一部分。因此,立即诊断可能并不容易。这是对所有各种临床图片的文献的全面回顾,以帮助医生迅速识别这种临床状况,记住我们作为心脏病专家的主导作用依赖于我们的知识和工作方法并受其影响。
关键词:肺栓塞,心源性猝死,晕厥,深静脉血栓形成
介绍
急性肺栓塞(APE)是静脉血栓栓塞(VTE)最严重的临床表现,致命性肺栓塞(PE)是猝死(SD)的常见原因,通常由深静脉血栓形成(DVT)并发症引起。
在美国,PE每年影响约50万至60万人,每年有200,000至300,000人死亡.1)PE是急性心肌梗死(AMI)和中风后第三常见的心血管疾病,年发病率为1-2每1000人(每10万居民100-200人).2),3)
2001年,整个欧洲的VTE相关死亡人数估计为543,454,与获得性免疫缺陷综合症(艾滋病)(5,860),乳腺癌(86,831),前列腺癌死亡人数相比,增加了一倍以上(63,636)和道路交通事故(53,599).4),5),6)由于诊断困难,很难获得正确的年度VTE事件数量主要基于以下因素:1)VTE通常在临床上保持沉默该疾病的第一个迹象是突然致命死亡(30-50%的病例)7); 2)临床表现模仿其他几种情况的特征,导致错误诊断8); 3)尸检时的PE检测非常困难,需要仔细检查肺血管树,以便发现小的急性栓塞或慢性血栓栓塞残留物9); 4)疾病诊断试验的敏感性和特异性仍然很弱.10)
PE风险因素包括肥胖,固定,使用香烟,癌症,手术,创伤,怀孕,口服避孕药或激素替代疗法,以及PE或已知的高凝血障碍的既往病史。然而,30%的PE患者没有可检测到的诱发因素,如真实世界登记处(EMPEROR),国际合作肺栓塞登记处(ICOPER)和Registro Informatizado de EnfermedadTromboEmbólica(RIETE)登记处的急诊医学肺栓塞所示,PE患者的平均年龄为56至66岁,老年人和女性患有轻度患病率.11),12),13),14)PE的临床表现从无症状的小肺栓塞到低死亡率大量PE导致右心室(RV)失败,伴有休克和/或死亡.15)
由于缺乏常规的死后检查导致低估其发病率,许多致命的肺栓塞仍未得到认可.16),17),18),19)这种潜在致命疾病的及时诊断至关重要,因此对突出的知识有所了解与PE相关的特征可以使医生能够进行诊断以促进以下适当的治疗策略。
症状和体征
疼痛可能与肺循环局部紊乱,胸膜受累或冠状动脉循环受损有关。中心PE也可能由于RV缺血而产生典型的心绞痛;胸膜炎性胸痛可能是由于小肺远端动脉(PA)栓塞继发肺部梗塞引起胸膜刺激的结果.20),21),22)呼吸困难具有多因素起源,由支气管痉挛或血管痉挛,干扰引起。肺循环,不动或膈肌呼吸偏移减少,肺不张和/或肺梗塞,缺氧或心功能受损。在患有预先存在的心力衰竭或肺病的患者中,恶化的呼吸困难可能是指示PE的唯一症状。缺氧在临床上表现为紫绀。当肝脏充血共存时可能发生高胆红素血症。呼吸困难,胸痛和咳嗽是PE最常见的症状,而发热,心动过速,肺部异常征象和周围血管塌陷是最常见的体检结果。不常观察到发绀,咯血,晕厥和急性肺源性心脏病的各种表现。
临床图片
PE是一种普遍存在且可能危及生命的心血管疾病,由于其广谱且通常无特异性表现,可能难以诊断(表1)。 因此,PE的诊断可能涉及多个专业,包括急诊医学,心脏病学,内科,妇产科,外科服务,有时还有紧急介入放射学。 美国各地的一些医疗中心,包括马萨诸塞州综合医院和布莱根妇女医院,已经建立了多学科的PE反应小组,以改善诊断和获得先进疗法。 鉴于这一前提,本评价的目的是为了更好地关注可能出现APE的患者的个体症状,以便对PE患者进行更全面的观察。
表格1
PE的临床表现
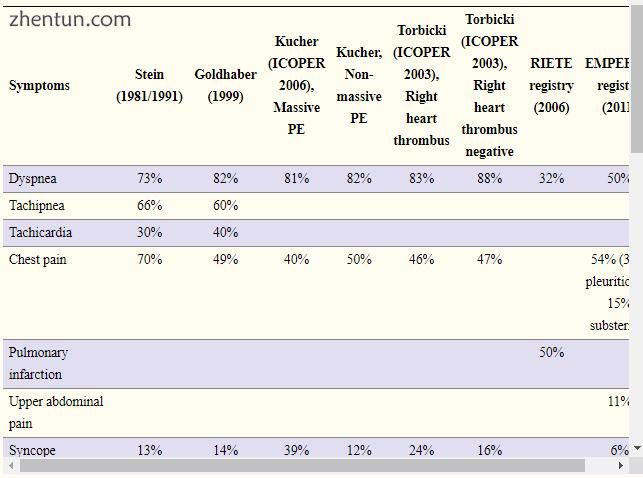
该表突出了每个注册表的症状流行程度。
AF =心房颤动; BBDX = Blocco di Branca Destra; DVT =深静脉血栓形成;心电图=心电图; EMPEROR =真实世界登记处的急诊医学肺栓塞; ICOPER =国际合作肺栓塞登记处; PA =肺动脉; PE =肺栓塞; RIETE = Registro Informatizado de EnfermedadTromboEmbólica; St =稳定的患者; U =不稳定的患者。
APE的临床图片:
SD(心脏骤停; SCA)
与急性呼吸窘迫综合征(ARDS)相似
典型的呼吸衰竭(缺氧和低碳酸血症)
哮喘危象样综合症
有或没有假性肺炎的发热综合征(有或没有胸腔积液)
急性右心衰竭/休克/低血压(常伴有上腹痛)
左心衰竭(肺充血)
伴有或不伴有咯血的胸膜炎综合征(伴有或不伴有积液)的胸痛
与急性冠状动脉综合征(ACS)相似(有或没有胸痛)
PE具有悖论性栓塞(由于栓塞部位而具有相应的临床表现并导致:AMI,中风,侧腹疼痛[由于急性脾梗塞或急性肾梗塞],急腹症和上肢或下肢栓塞。所有这些矛盾的栓塞条件,主要症状可能是全身性的还是不是)
昏厥
完成房室(AV)阻滞与室性心律
持续性或阵发性心房颤动(AF),心房扑动,房性心动过速,阵发性室上性心动过速(PSVT)
DVT和静音PE
平卧呼吸,orthodeoxia
腹痛无腹部急性
谵妄
SD
SD被定义为心脏病因(冠心病,肥厚性心肌病,瓣膜病,无结构异常)或非心源性原因(呼吸,脑,药物过量,放血,代谢,败血症,近溺水低温创伤)的意外自然死亡)24)在没有先前可能致命的病症的患者的短时间间隔内(通常在症状发作后1小时内)发生.25),26),27)。大多数受害者(> 90%)有潜在的心脏异常.28)SD的最常见原因是冠状动脉疾病(80%的病例),男性心脏性猝死(SCD)的风险高于女性,并随之增加由于老年人冠状动脉疾病(CAD)患病率较高而导致年龄增长。只有一小部分患者没有结构异常.29),30)美国SD发病率为每千人1人1人,其中SD是25-30%PE患者的初始临床表现,约占西方国家总死亡人数的1.3%.31),32)75%的SD病例包括超重/肥胖患者,其中31%的患者在药物治疗中有精神疾病史,支持最近报道精神障碍与PE风险之间的关联.33),34),35)据报道,临床上未预料到的导致院内SD的PE百分比高达50%至80%.36),37)SD引起的SD可出现ACS,发生室性心律失常或无休克节律期间。最近,Bougouin等[35]在一个基于人群的大型登记中显示,与PE相关的SCA并不罕见,占所有住院的SCA患者的3%。此外,这项研究强调,在女性和先前血栓栓塞的患者中,应该怀疑与PE相关的SCA无心电节律.38)心脏骤停的原因不容易被识别,特别是在初始节律时与心室颤动不同;在大多数情况下,大量PE中心脏停搏的机制是无脉性电活动(PEA)(一种以无意识患者中具有有组织电活动的可触知脉搏为特征的综合征)。
与ARDS类似
非心源性肺水肿或ARDS发生在多种临床环境中,如低血容量性休克,严重创伤和败血症; 1973年,Windebank和Moran将其描述为经典PE的并发症,尽管在这种情况下没有获得肺毛细血管楔压。 1982年,Adrian等人。记录肺水肿患者的PE,同时进行右心导管检查,毛细血管压力正常,因此排除左心室(LV)失败是导致肺水肿的原因;此外,限制在肺毛细血管床的无阻塞部分的肺水肿的发现证实了诊断。
已经提出从血凝块释放血管活性物质可能直接导致毛细血管通透性增加或静脉收缩和毛细血管静水压增加;此外,纤维蛋白微栓子可能会损伤肺毛细血管。当然,所有这些可能性都可能在阻塞的下游产生水肿。提出的另一种机制是血流分布不均,导致肺部某些区域过度灌注,导致间质和肺泡水肿.39)
典型的呼吸衰竭(缺氧和低碳酸血症)
在血气分析中,低氧血症被认为是APE的典型发现,但这些患者中高达40%具有正常的动脉血氧饱和度,20%具有正常的肺泡 - 动脉氧梯度.40),41)然而,当存在低氧血症时PE期间呼吸困难是血液动力学紊乱导致呼吸衰竭的首发症状。血流动力学紊乱包括低心输出量导致混合静脉血流的去饱和以及流量减少的区域(由于血管阻塞)和流量增加的区域导致通气 - 灌注不匹配。在大约三分之一的患者中,当存在右向左分流(通过卵圆孔未闭[PFO])时,可以检测到严重的低氧血症。这是由右心房和左心房之间的反向压力梯度引起的;在这些临床图片中,也经常出现低碳酸血症。胸部X光检查经常出现异常,虽然PE的发现通常是非特异性的,但它们可用于排除呼吸困难或胸痛的其他原因。
在患有呼吸衰竭的重症患者中,APE的经典表现可能难以或不可能被识别。在插管和接受机械通气治疗的患者中难以获得和评估症状。在先前被诊断患有慢性阻塞性肺病(COPD)的患者中,肺栓塞的常见临床表现(症状,体征,胸部X光片,心电图(ECG)和动脉血气水平的变化)经常出现,因为严重的潜在肺部疾病,肺栓塞的任何叠加表现可能不明显。在该组中,通气/灌注肺扫描与肺血管造影结果相关性较差,并且在尸体解剖检查期间,扫描通常不足以排除或排除肺栓塞。目前,肺血管造影仍然是确认或排除PE的唯一可靠技术.42)
哮喘危象(PE引起的支气管哮喘样症状)
已知PE会引起支气管哮喘等症状,因此如果既往存在哮喘病史,可能难以诊断PE [43]。69)然而,PE中支气管收缩的机制尚不完全清楚。有人提出,药理活性物质可能在血栓栓塞部位释放,导致特定的化学反射激发。这些药物包括乙酰胆碱,组胺,血清素和血浆激肽,所有这些都具有支气管收缩剂特性,11),12)表明肺栓塞发生的支气管收缩可能与肝素阻断其活性或释放的物质的存在有关。因为选择的患者支气管收缩的证据似乎代表了客观和敏感,尽管是非特异性的PE指数.4),45),46)如上所述,慢性哮喘有广泛的鉴别诊断。在成人中,急性重症哮喘几乎总是与慢性哮喘的诊断相关。然而,在PE中,症状的发作(主要是呼吸困难)从非常急性(分钟)到明显的沉淀物变得更缓慢(天数),没有明确的触发因素。与急性重症哮喘一致的症状包括难以完成的句子,心动过速,呼吸急促,以及通常保留氧合作用的广泛复音喘息,但老年患者或慢性疾病基线血气较多的患者可能异常,应始终予以考虑。为了进行鉴别诊断,常规检查应包括适当的血液检查,12导联心电图和胸部X光检查,以评估是否存在其他急性病变(如肺叶肺炎,气胸),此外超声心动图可以进行以评估形状和功能.47)
有或没有假性肺炎的发热综合征(有或没有胸腔积液)
PE可能伴有发热并且在X射线上显示肺部浸润的证据;在这种情况下,必须对肺炎等其他疾病进行鉴别诊断。肺炎和PE的临床特征非常不同。 PE起病较突然,呼吸困难比咳嗽和咳痰更突出。此外,与呼吸困难相关的PE没有放射学特征,并且对抗生素没有反应,发热是该疾病的后期现象。另一方面,肺炎逐渐发作,出现更明显的咳嗽,咳痰和发烧。通常胸部疼痛存在于PE中。应注意没有明显PE特征的年轻患者,应认真进行肺炎和PE的鉴别,以确保及时诊断和适当治疗.48)
急性右心衰竭/休克/低血压(常伴有上腹痛)
右心功能和血流动力学图像在PE患者分类中起关键作用。低血压的存在是预后不良的最重要预测指标,并定义了患有大量PE或高风险PE的患者。通过超声心动图评估具有RV功能障碍证据的血压正常的患者定义了亚大量类别,并且是具有中等风险的患者,结果不佳.49)5-10%的心肌损伤或休克患者的PE患者存在休克或低血压指数(心率/收缩压[mmHg])> 1,预后最差,必须进行快速诊断和治疗.50),51)对这些患者进行体格检查极其重要:颈静脉脉搏常常是伴有突出的V波升高,胸骨上的房颤隆起可能是明显的。在听诊时,可能存在S2增加的三尖瓣杂音和右侧S4(多达25%的患者)。在RV失败的患者中,ECG可显示窦性心动过速,RV应变的迹象,再极化异常或缺血,包括具有右轴偏差(> 90°)或S1Q3T3模式的完整或不完整的右束支传导阻滞;其他心电图特征可以是导联V1中的Qr,V1中的ST上升或者预先亲切的T波倒置。在亲切前导联中的T波倒置似乎与PE的严重程度和RV功能障碍的存在相关,正常化是有利结果的标志。 AF患者的死亡率增加,QRS电压低和室性早搏均反映RV衰竭程度和血流动力学损害[52],53)
对APE的血液动力学反应取决于许多因素,例如对释放的血管活性物质的生理反应,患者在基线时的心肺状态以及栓子的大小和肺血管阻塞的程度.54)肺血管阻塞>超声心动图检查显示30%与RV功能障碍的存在相关.55)
经胸超声心动图(TTE)扩张的RV功能障碍的迹象包括:1)心尖四腔视图中RV与LV舒张末期直径的比率> 1,或2)RV舒张末期直径> 30 mm和/或下腔静脉吸气性塌陷丧失。与RV失败的PAH患者中观察到的全球性运动功能不同,PE患者可能表现出RV顶端保留RV自由壁和基底的运动功能减退;一项名为“麦康奈尔标志”的研究结果显示,McConnell标志具有94%的特异性,诊断PE56的敏感性为77%。超声心动图检查有助于提示存在先前存在的心肺疾病,如慢性PAH。 )
左心衰竭可能伴有肺充血
PE患者的致龋性肺水肿可能是由于78):1)PA分支的闭塞导致其他分支中的流量增加,导致高肺毛细血管压力; 2)扩张RV对LV的压迫
尽管可以及时诊断第一种情况,但是由于通过扩张的RV压迫LV导致的肺水肿患者的PE可能是困难的。事实上,这类患者具有复杂的临床表现,单凭临床表现并且没有超声心动图等技术的帮助可能无法解决;一般来说,他们有长期呼吸困难,体检时双侧肺充血,超声心动图检查时房颤扩大,导致左心室压迫.58),59)
伴有或不伴有咯血的胸膜炎综合征(伴有或不伴有积液)的胸痛
胸痛胸痛综合征描述了一种涉及肺部浸润和胸痛的情况,其中疼痛与呼吸和位置有关;这种临床表现是肺梗塞的证据.60),61)小远端栓子产生肺泡出血区域,没有血流动力学相关性,导致咯血,胸膜炎和胸腔积液,通常是轻微的.61)
与ACS相似(有或没有胸痛)
与左主干病相似
在某些情况下,大量的PE可能会模仿ACS,胸痛,低血压,心动过速,缺氧;心电图ST段抬高导联增强矢量右(aVR)和V1伴ST段压低I,增强矢量左(aVL)和V4-6冠状动脉造影显示非梗阻性冠状动脉.62)“被忽视”导致aVR俯视LV腔并给出关于RV漏斗和基底室间隔的具体信息。因此,在大量APE中,经常看到导联aVR的ST升高,并且与总体上更差的预后相关。发现aVR和V1中ST段抬高的可能原因以及大量APE中侧向导联的弥漫性ST段凹陷可能与弥漫性心内膜下缺血有关,这是由于LV流入不良和随后的冠状动脉血流不良以及急性RV超负荷和可能RV梗塞。认识到这种模式对急性大体积PE患者非常重要,因为需要及时诊断并采取适当的治疗方法.63),64)
与前室间冠状动脉疾病相似
1)假前 - 非ST段抬高心肌梗死(STEMI)
在患有严重APE的患者中,经常在心前导联中观察到负T波(导联V1-4)。然而,由于左前降支CAD,在ACS中也发现了这一发现。两种疾病之间的快速区分对于选择适当的治疗至关重要。在导联V1-4中具有负T波的APE和ACS患者中,导联V1-2中的峰值负T波简单但准确地区分APE和ACS。在APE中,前负T是RV增大的结果,并且由于导联V1和V2面向RV的前部区域,也可能是RV缺血的征兆。此外,由于导联III面向RV的下部区域,导联III中的负T波是非常常见的。在心电图中也发现了负T波,其中有相当数量的患有左主干病的患者类似的心电图检查结果,然而在这类患者中,负性T波更广泛地分布在肢体导联和心前导联的导联aVR周围,除了导联V1.66)
2)假前室间隔STEMI
在70-80%的APE患者中可见心电图异常。许多STE升高V1-V3 / V4的病例已在文献中描述.67),68)如果STEMI未被诊断,将APE与前STEMI区分是非常具有挑战性的,主要是由于致命的结果。然而,当临床表现更多提示APE时,并且心电图特征对于STEMI来说并不典型(例如,没有相互的ST偏差),应立即转诊至肺血管造影计算机断层扫描(CT)并及时提供良好分辨率的图像以加快速度。在这个特定情况下的诊断;在这种情况下,床边超声心动图寻找区域性壁运动异常和RV扩张的证据也可能是有用的.70)然而,当临床图像不那么清楚时,很难区分APE与前STEMI的ST段抬高。已经提出了几种在APE中发展ST段抬高的机制:RV透壁缺血和梗塞的发展;伴有RV扩张和衰竭,在此图中RV无法产生足够的收缩压来克服后负荷急剧增加,导致RV氧需求增加和肺灌注显著减少。这与室间隔的左移一起将减少LV预负荷;以及随后的心输出量和冠状动脉血流量;此外,缺氧可导致严重的RV透壁缺血导致导联V1-V3 / V4.71中的ST段抬高[72],72)73)已经报道了具有这些临床特征且没有闭塞性CAD的顺从性和大量PE的大量研究。 74),对于APE导联V1-V3 / V4中ST段抬高的另一种解释是通过房间隔缺损或PFO(尸检系列中普遍存在25-35%)的反常冠状动脉栓塞。右心压力突然升高,产生右向左分流[76),77),78)这表明STEMI的初始表现可能掩盖伴随的APE,并迅速识别和治疗这两种病变非常重要;事实上,具有矛盾性冠状动脉栓塞的患者可能没有潜在的动脉粥样硬化,并且血栓抽吸可能是治疗的首选。
PE伴有反常栓塞(临床图片取决于栓塞部位)
具有反常栓塞的PE是指源自静脉血管系统并通过心内或肺分流进入体循环的血栓栓塞的临床现象。
肺动脉高压和大量或亚大量PE是反常外周动脉栓塞的高危因素。 PFO是最常见的心内分流术。 PFO的患病率似乎随着年龄的增长而降低,前三十年发病率为34%,第三至第七十年发病率为25%,八十年代发病率<20%.79)在生理条件下,压力梯度为保持在左心房和右心房之间,导致PFO的被动闭合。如果右心房压力增加超过左心房压力,如在瓦尔萨尔瓦演习结束时观察(如咳嗽,打喷嚏,下蹲,排便和排尿),可能会出现短暂的右侧左分流,这可能导致血栓进入体循环。在PE或肺动脉高压的其他原因后观察到的右侧心脏压力的永久性增加可能导致左心房间分流的显著或可能永久的权利,增加了矛盾性栓塞的风险。
其他解剖变异也与PFO有关:
Eustakian瓣膜是窦静脉右瓣膜的胚胎残余物,在子宫内将含氧静脉血从下腔静脉引导至卵圆孔。在大多数个体分娩后,Eustakian瓣膜逐渐消失,但是残余突出可能将静脉血引导至卵圆窝并且在一些个体中引起显著的右向左分流。发现PFO和残留显著的Eustakian瓣膜共存(约70%的病例),特别是在矛盾栓塞的患者中.80)
在2-4%的一般人群中观察到的Chiari网络是窦静脉右心瓣(右心房)的另一个胚胎残余,这是由于胚胎心脏发育过程中不完全再吸收所致。它经常与PFO,右向左分流或房间隔动脉瘤(ASA)相关,所有这些都促进了矛盾的栓塞。
所有心内通讯,包括室间隔缺损,都有一定的反常栓塞风险。相比之下,患有肺动静脉畸形的患者具有永久性左侧分流功能,允许血栓或脓毒性栓子进入体循环.81)
心内通讯产生的临床表现取决于栓塞部位,可能与以下因素有关:
AMI(STEMI):通过PFO的矛盾性栓塞是AMI的最可能原因,发生在大约5 / 1,000名患者中。虽然这是一个相当低的比率,但发病率仍然很高,足以引起临床关注,特别是在年轻患者或RV梗死的情况下.82),83),84)
中风:脑血管意外是假定的矛盾性栓塞最常见的相关临床表现。大约40%的患者通常进行常规诊断检查仍然无法确定卒中的原因,即所谓的隐源性卒中.85)与传统卒中原因相比,隐源性卒中患者的PFO增加2倍以上。
腰部疼痛(由于急性肾梗塞,腰痛伴血尿)86)
急性肠系膜缺血(急腹症)87)
下肢栓塞:继发于外周动脉闭塞的冷和无脉四肢.88)与保守治疗溶栓或抗凝治疗相比,外科血栓栓塞切除术可有效降低死亡率。肺动脉高压和大量或亚大量PE是反常外周动脉栓塞的高危因素。对于反常外周动脉栓塞的二级预防,联合药物治疗可以显著降低复发性栓塞事件或死亡的风险.89),90)
这些病例证实了由于并发的动脉和静脉栓塞引起的可能的矛盾栓子的高指数。正确和迅速的诊断非常重要,使用超声心动图检查和更敏感的经食管超声心动图和经颅多普勒(TCD)超声检查在检测右向左分流时起着关键作用,无论其位置如何。
昏厥
晕厥被定义为可归因于全脑性低灌注的短暂性意识丧失,其进一步的特征在于快速起效,简洁和自发恢复。这是到达急诊室(ED)的常见原因,约占就诊人数的1%。在美国,30-40%的此类患者随后被接受进一步调查。住院治疗晕厥的患者的PE患病率尚未得到充分证实,但Duplyakov等人最近的研究[66]和德国登记,肺栓塞登记管理策略和预后(MAPPET)显示高患者的晕厥发生率-risk PE分别为29.9%和35%。
已经提出了三种可能的PE患者晕厥机制:
晕厥可能是由肺动脉系统超过50%的血栓形成引起的,这会导致心输出量增加,导致动脉低血压和脑血流量减少。
引起晕厥的第二种机制可能是血管迷走神经反射的激活。 1867年,von Bezold提出了心脏抑制反射理论,后来由Jarisch完成。 Bezold-Jarisch反射的关键点是激活位于左心室的机械感受器。在急性肺血栓栓塞中,当栓子滞留在PA的大分支中时,它可能引发超肾上腺素能状态,导致LV收缩性的增加,同时限制舒张期充盈。这可能刺激Bezold-Jarisch反射中涉及的心室机械感受器(C型传入纤维)并导致传出迷走神经反应的增加,导致心率降低,AV传导延迟和交感神经紧张减少,从而导致在外周血管扩张,最后晕厥。
第三种可能的解释是RV过载引起的心律失常和传导障碍。
疑似PE患者的晕厥史应被视为住院期间致命并发症高风险的可能标准。
具有室性心律的完整AV阻滞
具有特发性心律的完整AV阻滞可能是APE的初始表现,有时与晕厥一起。
在由于大量栓塞和Bezold-Jarisch反射引起的肺血栓栓塞期间存在晕厥(如前所述),可能发生不同程度的AV阻滞。但是,在存在完整的左束支传导阻滞的情况下,完整的AV阻滞是可能的。事实上,在这一部分患者中,已知完整的AV阻滞是由于急性右束支传导阻滞的发展,导致晕厥。右束支传导阻滞的发展与其解剖位置有关;实际上,His束的右分支由于其在隔膜的RV面上的浅表亚心内膜轨迹而特别暴露,因此它对右腔的突然扩张非常敏感。
持续性或阵发性房颤,心房扑动,房性心动过速,PSVT
由于其非典型症状,PE常常被诊断不足很长时间,并且仅在临床情况由于强迫患者去医院的心律失常发作而复杂化时才进行诊断。在这种情况下,医生发现自己面临心律失常,这是另一个可能未被认识到的问题的结果,92)是房颤,心房扑动,房性心动过速和PSVT的情况。
DVT和静音PE
在PE患者中,32%的病例中存在表明血栓性静脉炎的临床体征和症状。然而,在79%的病例中存在DVT,如果不存在,则可能意味着它已经栓塞。在大多数DVT患者中,凝块位于近端,40-50%的病例具有更复杂的临床表现,其中存在PE,但通常是沉默的。沉默的PE在手术后阶段经常发生,尤其是在没有预防的患者中。 APE在DVT后3-7天发展,10%的病例在症状出现后1小时内致命.93)
平卧呼吸,直立低氧血症
Platypnea-orthodeoxia是一种直立姿势(脱饱和SO2)的呼吸困难和缺氧综合症,通过卧床缓解。 Platypnea-orthodeoxia也与有和没有PE的PFO有关,有或没有矛盾栓塞。两种情况必须共存才能引起这种综合征:一种是房间交流形式的解剖学成分,以及在房间隔中产生畸形的功能性成分,导致分流的重定向,假设是直立姿势。前者可能是房间隔缺损,PFO或有孔ASA。后者可能是心脏,如心包积液或缩窄性心包炎;肺气肿,如肺气肿,动静脉畸形,全肺切除术或胺碘酮毒性;腹部,如肝硬化或肠梗阻;或血管,如主动脉瘤或伸长。可以在异常分流的位置修改的基础上解释扁平动脉 - 正畸。直立位置可以延伸房间交流(PFO,房间隔缺损或有孔ASA),允许更多的静脉血从下腔静脉穿过缺损,无论是否持续的咽鼓管瓣膜共存。在PFO的情况下,PE的发生会产生更高的左心房压力,这可能是解释分流和倾斜性胸闷的一个因素.94)
腹痛无急腹症
众所周知,许多受血流动力学稳定性PE影响的患者入院时出现胸痛而没有进一步的PE症状,但在少数情况下,出现的症状更为罕见:事实上,2例PE患者年轻男性在ED中评估上腹部急性疼痛并显示出与PE92相符的基础肺部异常,已在文献中进行了描述。
谵妄
谵妄是一种急性混淆状态,是一种常见的复杂医学疾病,与65岁及以上患者的严重发病率和死亡率相关。这种潜在的可逆性认知障碍越来越被认为是严重潜在疾病的征兆。缺氧是众所周知的谵妄诱发因素,PE是缺氧的常见原因。
因此,谵妄可能使患有其他疾病证据的患者的PE复杂化。老年人谵妄应该被视为与低氧血症图片,急性心室损害,低血压和/或反常栓塞相关的非典型性PE,这可以解释这种“肺 - 脑连接”,但完整的机制仍然未知。) ,95)
结论
由于不同装置的参与(图1),APE可能是几种不同症状之间复杂的相互作用,这可能导致可能难以诊断的危及生命的心血管疾病;多种团队方法可能是必要的,以改善患者评估和帮助临床决策,以提供最好的护理;朝着这个方向努力应该是我们未来的目标。
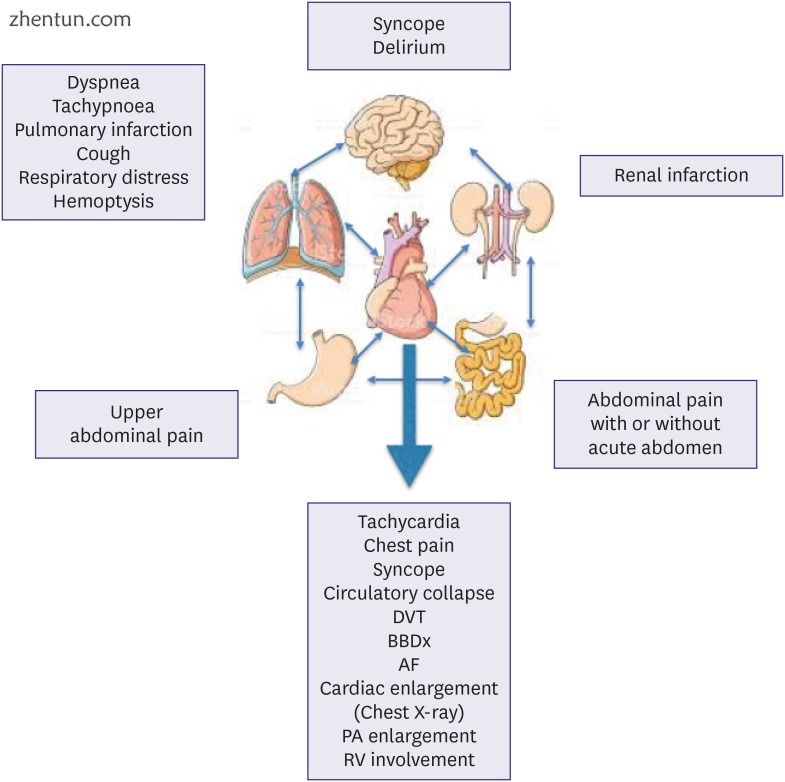
图1
PE中的装置。
PE可能出现在几张临床图片下。 仔细的患者评估是关键,以免错过诊断。
AF =心房颤动; BBDX = Blocco di Branca Destra; DVT =深静脉血栓形成; PA =肺动脉; PE =肺栓塞; RV =右心室。
参考:
Acute Pulmonary Embolism: Focus on the Clinical Picture
1. Marshall PS, Mathews KS, Siegel MD. Diagnosis and management of life-threatening pulmonary embolism. J Intensive Care Med. 2011;26:275–294. [PubMed]
2. Heit JA. The epidemiology of venous thromboembolism in the community. Arterioscler Thromb Vasc Biol. 2008;28:370–372. [PMC free article] [PubMed]
3. Cohen AT, Agnelli G, Anderson FA, et al. Venous thromboembolism (VTE) in Europe. The number of VTE events and associated morbidity and mortality. Thromb Haemost. 2007;98:756–764. [PubMed]
4. Eurostat: Eurostat statistics on health and safety 2001 [Internet] Luxembourg: Eurostat; 2001. Available from: http://ec.europa.eu/eurostat/sea ... PULMONARY+EMBOLISM.
5. Klok FA, van Kralingen KW, van Dijk AP, et al. Quality of life in long-term survivors of acute pulmonary embolism. Chest. 2010;138:1432–1440. [PubMed]
6. Fanikos J, Piazza G, Zayaruzny M, Goldhaber SZ. Long-term complications of medical patients with hospital-acquired venous thromboembolism. Thromb Haemost. 2009;102:688–693. [PubMed]
7. Stein PD, Henry JW. Prevalence of acute pulmonary embolism among patients in a general hospital and at autopsy. Chest. 1995;108:978–981. [PubMed]
8. Heit JA, Silverstein MD, Mohr DN, Petterson TM, O'Fallon WM, Melton LJ. Predictors of survival after deep vein thrombosis and pulmonary embolism: a population-based, cohort study. Arch Intern Med. 1999;159:445–453. [PubMed]
9. Pichereau C, Maury E, Monnier-Cholley L, et al. Post-mortem CT scan with contrast injection and chest compression to diagnose pulmonary embolism. Intensive Care Med. 2015;41:167–168. [PubMed]
10. Opinions regarding the diagnosis and management of venous thromboembolic disease. ACCP Consensus Committee on Pulmonary Embolism. American College of Chest Physicians. Chest. 1998;113:499–504. [PubMed]
11. Laporte S, Mismetti P, Décousus H, et al. Clinical predictors for fatal pulmonary embolism in 15,520 patients with venous thromboembolism: findings from the Registro Informatizado de la Enfermedad TromboEmbolica venosa (RIETE) Registry. Circulation. 2008;117:1711–1716. [PubMed]
12. Tzoran I, Brenner B, Papadakis M, Di Micco P, Monreal M. VTE registry: what can be learned from RIETE? Rambam Maimonides Med J. 2014;5:e0037 [PMC free article] [PubMed]
13. Goldhaber SZ, Visani L, De Rosa M. Acute pulmonary embolism: clinical outcomes in the International Cooperative Pulmonary Embolism Registry (ICOPER) Lancet. 1999;353:1386–1389. [PubMed]
14. Heit JA, Silverstein MD, Mohr DN, Petterson TM, O'Fallon WM, Melton LJ. Risk factors for deep vein thrombosis and pulmonary embolism: a population-based case-control study. Arch Intern Med. 2000;160:809–815. [PubMed]
15. Pineda LA, Hathwar VS, Grant BJ. Clinical suspicion of fatal pulmonary embolism. Chest. 2001;120:791–795. [PubMed]
16. Babak S, Sriram KB. Misinterpreting risk and test results delays diagnosis in a patient with pulmonary embolism. BMJ Case Rep. 2014;2014:bcr2014204172 [PMC free article] [PubMed]
17. Cohen AT, Edmondson RA, Phillips MJ, et al. The changing pattern of venous thromboembolic disease. Haemostasis. 1996;26:65–71. [PubMed]
18. Sandler DA, Martin JF. Autopsy proven pulmonary embolism in hospital patients: are we detecting enough deep vein thrombosis? J R Soc Med. 1989;82:203–205. [PMC free article] [PubMed]
19. Pollack CV, Schreiber D, Goldhaber SZ, et al. Clinical characteristics, management, and outcomes of patients diagnosed with acute pulmonary embolism in the emergency department: initial report of EMPEROR (Multicenter Emergency Medicine Pulmonary Embolism in the Real World Registry) J Am Coll Cardiol. 2011;57:700–706. [PubMed]
20. Stein PD, Henry JW. Clinical characteristics of patients with acute pulmonary embolism stratified according to their presenting syndromes. Chest. 1997;112:974–979. [PubMed]
21. Thames MD, Alpert JS, Dalen JE. Syncope in patients with pulmonary embolism. JAMA. 1977;238:2509–2511. [PubMed]
22. Islam M, Filopei J, Frank M, et al. Pulmonary infarction secondary to pulmonary embolism: an evolving paradigm. Respirology. 2018 Epub ahead of print. [PubMed]
23. Jaff MR, McMurtry MS, Archer SL, et al. Management of massive and submassive pulmonary embolism, iliofemoral deep vein thrombosis, and chronic thromboembolic pulmonary hypertension: a scientific statement from the American Heart Association. Circulation. 2011;123:1788–1830. [PubMed]
24. Adabag AS, Luepker RV, Roger VL, Gersh BJ. Sudden cardiac death: epidemiology and risk factors. Nat Rev Cardiol. 2010;7:216–225. [PMC free article] [PubMed]
25. Zipes DP, Wellens HJ. Sudden cardiac death. Circulation. 1998;98:2334–2351. [PubMed]
26. Knight B. Forensic pathology. 2nd ed. London: Edward Arnold; 1996.
27. Chugh SS. Sudden cardiac death with apparently normal heart: clinical implications of progress in pathophysiology. Card Electrophysiol Rev. 2001;5:394–402.
28. Eckart RE, Shry EA, Burke AP, et al. Sudden death in young adults: an autopsy-based series of a population undergoing active surveillance. J Am Coll Cardiol. 2011;58:1254–1261. [PubMed]
29. Lucena J, Rico A, Vázquez R, et al. Pulmonary embolism and sudden-unexpected death: prospective study on 2477 forensic autopsies performed at the Institute of Legal Medicine in Seville. J Forensic Leg Med. 2009;16:196–201. [PubMed]
30. Kürkciyan I, Meron G, Behringer W, et al. Accuracy and impact of presumed cause in patients with cardiac arrest. Circulation. 1998;98:766–771. [PubMed]
31. Beckman MG, Hooper WC, Critchley SE, Ortel TL. Venous thromboembolism: a public health concern. Am J Prev Med. 2010;38:S495–S501. [PubMed]
32. Heit JA. The epidemiology of venous thromboembolism in the community: implications for prevention and management. J Thromb Thrombolysis. 2006;21:23–29. [PubMed]
33. Patriquin L, Khorasani R, Polak JF. Correlation of diagnostic imaging and subsequent autopsy findings in patients with pulmonary embolism. AJR Am J Roentgenol. 1998;171:347–349. [PubMed]
34. Bharadwaj RS, Slade TB. Diagnosis of pulmonary thromboembolism in psychiatric patients. Prim Care Companion CNS Disord. 2011;13 CC.10l01076 [PMC free article] [PubMed] CC.10l01076 [PMC free article] [PubMed]
35. Bougouin W, Marijon E, Planquette B, et al. Factors associated with pulmonary embolism-related sudden cardiac arrest. Circulation. 2016;134:2125–2127. [PubMed]
36. Roger VL, Go AS, Lloyd-Jones DM, et al. Heart disease and stroke statistics--2012 update: a report from the American Heart Association. Circulation. 2012;125:e2–220. [PMC free article] [PubMed]
37. Rodger MA, Carrier M, Jones GN, et al. Diagnostic value of arterial blood gas measurement in suspected pulmonary embolism. Am J Respir Crit Care Med. 2000;162:2105–2108. [PubMed]
38. Stein PD, Goldhaber SZ, Henry JW, Miller AC. Arterial blood gas analysis in the assessment of suspected acute pulmonary embolism. Chest. 1996;109:78–81. [PubMed]
39. Geibel A, Zehender M, Kasper W, et al. Prognostic value of the ECG on admission in patients with acute major pulmonary embolism. Eur Respir J. 2005;25:843–848. [PubMed]
40. Page IH. Serotonin (5-hydroxytryptamine); the last four years. Physiol Rev. 1958;38:277–335. [PubMed]
41. Lewis GP. Active polypeptides derived from plasma proteins. Physiol Rev. 1960;40:647–676. [PubMed]
42. Boyer NH, Curry JJ. Bronchospasm associated with pulmonary embolism. Arch Intern Med (Chic) 1944;73:403–409.
43. Xu K, Tang X, Song Y, Chen Z. The diagnostic dilemma between pulmonary embolism with positive chest imaging and pneumonia: a case report and literature review. J Transl Med Epidemiol. 2015;3:1039.
44. Karabulut N, Kiroğlu Y. Relationship of parenchymal and pleural abnormalities with acute pulmonary embolism: CT findings in patients with and without embolism. Diagn Interv Radiol. 2008;14:189–196. [PubMed]
45. Duru S, Keleşoğlu A, Ardıç S. Clinical update on pulmonary embolism. Arch Med Sci. 2014;10:557–565. [PMC free article] [PubMed]
46. Konstantinides S. Pulmonary embolism: impact of right ventricular dysfunction. Curr Opin Cardiol. 2005;20:496–501. [PubMed]
47. Fonarow GC, Abraham WT, Albert NM, et al. Factors identified as precipitating hospital admissions for heart failure and clinical outcomes: findings from OPTIMIZE-HF. Arch Intern Med. 2008;168:847–854. [PubMed]
48. McMichael J. Pulmonary heart disease acute and chronic. Br Heart J. 1948;10:80–87. [PMC free article] [PubMed]
49. McIntyre KM, Sasahara AA. The hemodynamic response to pulmonary embolism in patients without prior cardiopulmonary disease. Am J Cardiol. 1971;28:288–294. [PubMed]
50. Wolfe MW, Lee RT, Feldstein ML. Prognostic significance of right ventricular hypokinesis and perfusion lung scan defects in pulmonary embolism. Am Heart J. 1994;127:1371–1375. [PubMed]
51. McConnell MV, Solomon SD, Rayan ME, et al. Regional right ventricular dysfunction detected by echocardiography in acute pulmonary embolism. Am J Cardiol. 1996;78:469–473. [PubMed]
52. Wood KE. Major pulmonary embolism: review of a pathophysiologic approach to the golden hour of hemodynamically significant pulmonary embolism. Chest. 2002;121:877–905. [PubMed]
53. Luisada AA, Cardi L. Acute pulmonary edema; pathology, physiology and clinical management. Circulation. 1956;13:113–135. [PubMed]
54. Harjola VP, Mebazaa A, Čelutkienė J, et al. Contemporary management of acute right ventricular failure: a statement from the Heart Failure Association and the Working Group on Pulmonary Circulation and Right Ventricular Function of the European Society of Cardiology. Eur J Heart Fail. 2016;18:226–241. [PubMed]
55. Wolff L. Pulmonary embolism. Circulation. 1952;6:768–776. [PubMed]
56. ESC Committee for Practice guidelines (CPG) Konstantinides SV, Torbicki A, et al. 2014 ESC Guidelines on the diagnosis and management of acute pulmonary embolism: the Task Force for the Diagnosis and Management of Acute Pulmonary Embolism of the European Society of Cardiology (ESC) Eur Heart J. 2014;35:3033–3073. [PubMed]
57. Amini R, Jyothidasan A, Poommipanit P, Kapoor D. EKG findings mimicking left main coronary disease in a patient with acute massive pulmonary embolism. J Am Coll Cardiol. 2014;63(suppl):A699
58. Manne JR. Acute ST segment elevation in a patient with massive pulmonary embolism mimicking acute left main coronary artery obstruction. J Am Coll Cardiol. 2016;67:1118.
59. Ciliberti P, Rapezzi C, Villani C, Boriani G. Massive pulmonary embolism with acute coronary syndrome-like electrocardiogram mimicking acute left main coronary artery obstruction. J Emerg Med. 2012;43:e255–e258. [PubMed]
60. Kosuge M, Ebina T, Hibi K, et al. Simple electrocardiographic criteria for discriminating between acute pulmonary embolism and acute coronary syndrome. J Am Coll Cardiol. 2016;67:528.
61. Kosuge M, Ebina T, Hibi K, et al. Differences in negative T waves among acute coronary syndrome, acute pulmonary embolism, and Takotsubo cardiomyopathy. Eur Heart J Acute Cardiovasc Care. 2012;1:349–357. [PMC free article] [PubMed]
62. Yaméogo NV, Mbaye A, Kagambèga LJ, et al. Pulmonary embolism mimicking acute anterior myocardial infarction: diagnostic trap. Ann Cardiol Angeiol (Paris) 2011;60:169–172. [PubMed]
63. Falterman TJ, Martinez JA, Daberkow D, Weiss LD. Pulmonary embolism with ST segment elevation in leads V1 to V4: case report and review of the literature regarding electrocardiographic changes in acute pulmonary embolism. J Emerg Med. 2001;21:255–261. [PubMed]
64. Omar HR. ST-segment elevation in V1-V4 in acute pulmonary embolism: a case presentation and review of literature. Eur Heart J Acute Cardiovasc Care. 2016;5:579–586. [PubMed]
65. Mittal SR, Maheshwari M. Electrocardiographic changes in submassive pulmonary embolism. Indian Heart J. 2005;57:80–81. [PubMed]
66. Duplyakov D, Kurakina E, Pavlova T, et al. Value of syncope in patients with high-to-intermediate risk pulmonary artery embolism. Eur Heart J Acute Cardiovasc Care. 2015;4:353–358. [PubMed]
67. Jenab Y, Lotfi-Tokaldany M, Alemzadeh-Ansari MJ, et al. Correlates of syncope in patients with acute pulmonary thromboembolism. Clin Appl Thromb Hemost. 2015;21:772–776. [PubMed]
68. Yamaki T, Nozaki M, Sakurai H, et al. Presence of lower limb deep venous thrombosis and prognosis in patients with symptomatic pulmonary embolism: preliminary report. Eur J Vasc Endovasc Surg. 2009;37:225–231. [PubMed]
69. Jiménez D, Aujesky D, Díaz G, et al. Prognostic significance of deep vein thrombosis in patients presenting with acute symptomatic pulmonary embolism. Am J Respir Crit Care Med. 2010;181:983–991. [PubMed]
70. Lin JF, Li YC, Yang PL. A case of massive pulmonary embolism with ST elevation in leads V1-4. Circ J. 2009;73:1157–1159. [PubMed]
71. Mittal SR, Arora H. Pulmonary embolism with isolated right ventricular infarction. Indian Heart J. 2001;53:218–220. [PubMed]
72. Mittal SR, Jain S, Maheshwari S. Pulmonary embolism with isolated right ventricular infarction. Indian Heart J. 1996;48:704–706. [PubMed]
73. Jerjes Sánchez C, Gutiérrez-Fajardo P, Ramírez-Rivera A, et al. Acute infarct of the right ventricle secondary to a massive pulmonary thromboembolism. Arch Inst Cardiol Mex. 1995;65:65–73. [PubMed]
74. Olivares-Reyes A, Chan S, Lazar EJ, Bandlamudi K, Narla V, Ong K. Atrial septal aneurysm: a new classification in two hundred five adults. J Am Soc Echocardiogr. 1997;10:644–656. [PubMed]
75. Kleber FX, Hauschild T, Schulz A. Paradoxical embolic myocardial infarction. J Am Coll Cardiol. 2014;64:TCT-163
76. Wąsek WC, Samul W, Ryczek R, Skrobowski A. Unique case of ST-segment-elevation myocardial infarction related to paradoxical embolization and simultaneous pulmonary embolization: clinical considerations on indications for patent foramen ovale closure in no-guidelines land. Circulation. 2015;131:1214–1223. [PubMed]
77. Yildiz A, Bostan C, Akin F, Arat Ozkan A, Gurmen T. Concurrent pulmonary embolism and acute coronary syndrome with dynamic electrocardiographic changes. Am J Emerg Med. 2012;30:637.e1–637.e4. [PubMed]
78. Windecker S, Stortecky S, Meier B. Paradoxical embolism. J Am Coll Cardiol. 2014;64:403–415. [PubMed]
79. Carey HB, Boltax R, Dickey KW, Finkelstein FO. Bilateral renal infarction secondary to paradoxical embolism. Am J Kidney Dis. 1999;34:752–755. [PubMed]
80. Vicente DC, Kazmers A. Acute mesenteric ischemia. Curr Opin Cardiol. 1999;14:453–458. [PubMed]
81. Loscalzo J. Paradoxical embolism: clinical presentation, diagnostic strategies, and therapeutic options. Am Heart J. 1986;112:141–145. [PubMed]
82. Wei F, Zhang Y, Tian H, Zhang J, Ma Q. Pulmonary hypertension and massive or sub-massive pulmonary embolism are the high risk factors for paradoxical peripheral arterial embolism. J Am Coll Cardiol. 2016;68:C154
83. Akrawinthawong K, Damrongwatanasuk R, Abuzahra M. Acute limb ischemia and silent pulmonary emboli as a key to identify thrombus-in-transit through patent foramen ovale. J Am Coll Cardiol. 2016;67:1194.
84. Konstantinides S, Geibel A, Kasper W, Olschewski M, Blümel L, Just H. Patent foramen ovale is an important predictor of adverse outcome in patients with major pulmonary embolism. Circulation. 1998;97:1946–1951. [PubMed]
85. Di Tullio M, Sacco RL, Venketasubramanian N, Sherman D, Mohr JP, Homma S. Comparison of diagnostic techniques for the detection of a patent foramen ovale in stroke patients. Stroke. 1993;24:1020–1024. [PubMed]
86. Pinto FJ. When and how to diagnose patent foramen ovale. Heart. 2005;91:438–440. [PMC free article] [PubMed]
87. Prandoni P, Lensing AW, Prins MH, et al. Prevalence of pulmonary embolism among patients hospitalized for syncope. N Engl J Med. 2016;375:1524–1531. [PubMed]
88. Kearon C. Natural history of venous thromboembolism. Circulation. 2003;107:I22–I30. [PubMed]
89. Varkul M, Robinson T, Ng E, Hyland R. Orthodeoxia and platypnea secondary to a patent foramen ovale despite normal right-sided cardiac pressures. Can Respir J. 2001;8:105–107. [PubMed]
90. Sentjens RE, Houtman S, Meijerink MR, Konings TC. Emboli on the move. J Crit Care. 2010;14:399–401.
91. Giorgi-Pierfranceschi M, Cattabiani C, Mumoli N, Dentali F. Abdominal pain as pulmonary embolism presentation, usefulness of bedside ultrasound: a report of two cases. Blood Coagul Fibrinolysis. 2017;28:107–111. [PubMed]
92. Inouye SK. Delirium in older persons. N Engl J Med. 2006;354:1157–1165. [PubMed]
93. Laack TA, Goyal DG. Pulmonary embolism: an unsuspected killer. Emerg Med Clin North Am. 2004;22:961–983. [PubMed]
94. Søgaard KK, Schmidt M, Pedersen L, Horváth-Puhó E, Sørensen HT. 30-year mortality after venous thromboembolism: a population-based cohort study. Circulation. 2014;130:829–836. [PubMed]
95. Carrascosa MF, Batán AM, Novo MF. Delirium and pulmonary embolism in the elderly. Mayo Clin Proc. 2009;84:91–92. [PMC free article] [PubMed] |