当脑内出现异常细胞时就会发生脑肿瘤。[2]有两种主要类型的肿瘤:癌性(恶性)肿瘤和良性(非癌性)肿瘤。[2]癌症肿瘤可分为原发性肿瘤,其起源于脑内,而继发性肿瘤则从其他地方扩散,称为脑转移瘤[1]。所有类型的脑肿瘤都可能产生各种症状,这些症状取决于所涉及的大脑部分。[2]这些症状可能包括头痛,癫痫发作,视力问题,呕吐和精神变化。[1] [2] [7]早上经常头痛加重,呕吐消失。[2]其他症状可能包括行走,说话或感觉困难。[1] [3]随着疾病的进展,可能会出现无意识。[3]
大多数脑瘤的病因尚不清楚。[2]罕见的危险因素包括接触氯乙烯,爱泼斯坦 - 巴尔病毒,电离辐射和遗传性综合征,如神经纤维瘤病,结节性硬化症和von Hippel-Lindau病。[1] [2] [3]关于手机曝光的研究并没有明显的风险。[3]成人中最常见的原发性肿瘤类型是脑膜瘤(通常为良性)和星形细胞瘤,如胶质母细胞瘤[1]。在儿童中,最常见的类型是恶性髓母细胞瘤。[3]诊断通常通过医学检查以及计算机断层扫描(CT)或磁共振成像(MRI)进行。[2]然后通常通过活组织检查证实结果。[1]根据研究结果,肿瘤分为不同严重程度。[1]
治疗可能包括手术,放射治疗和化疗的某些组合。[1]如果发生癫痫发作,可能需要抗惊厥药物。[1]地塞米松和呋塞米是可用于减少肿瘤周围肿胀的药物。[1]有些肿瘤逐渐生长,只需要监测,可能不需要进一步干预。[1]正在研究使用人体免疫系统的治疗方法。[2]结果差异很大,取决于肿瘤的类型以及它在诊断时的传播范围。[3]虽然良性肿瘤只在一个区域生长,但由于它们的位置,它们可能仍然会危及生命。[8]胶质母细胞瘤通常结果非常差,而脑膜瘤通常有良好的预后。[3]美国所有脑癌的平均五年存活率为33%。[4]
继发性或转移性脑肿瘤的发生率约为原发性脑肿瘤的4倍[2] [9],约有一半的转移灶来自肺癌。[2]全球每年大约有250,000人患有原发性脑肿瘤,占癌症的比例不到2%。[3]在15岁以下的儿童中,脑肿瘤仅次于急性淋巴细胞白血病,是最常见的癌症形式。[10]在澳大利亚,一例脑癌的平均终生经济成本为190万美元,是任何类型癌症中最大的。[11]
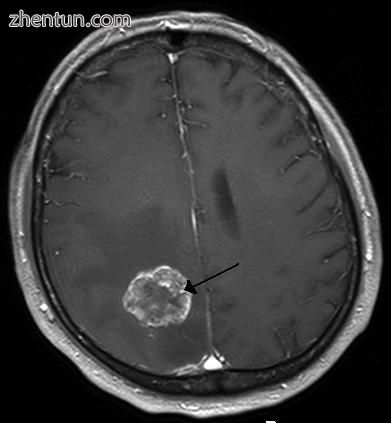
右脑半球肺癌脑转移,磁共振成像显示
目录
1 症状和体征
1.1 头痛
1.2 特定位置的症状
1.3 行为改变
2 原因
3 病理生理学
3.1 脑膜
3.2 脑部问题
3.3 脊髓
4 诊断
4.1 影像
4.2 病理学
4.3 分类
5 治疗
5.1 手术
5.2 放射治疗
5.3 化疗
5.4 其他
6 预后
6.1 多形性胶质母细胞瘤
6.2 少突胶质细胞
6.3 听神经瘤
7 流行病学
7.1 美国
7.2 UK
7.3 儿童
8 研究
8.1 免疫治疗
8.2 水泡性口炎病毒
8.3 逆转录病毒复制载体
9 参考
体征和症状
脑瘤的症状和体征很广泛。无论肿瘤是良性(非癌性)还是癌性,人们都可能出现症状[12]。原发性和继发性脑肿瘤具有相似的症状,取决于肿瘤的位置,大小和生长速度。[13]例如,额叶中较大的肿瘤可引起思考能力的变化。然而,在Wernicke区域(负责语言理解的小区域)等较小的肿瘤可导致更大的功能丧失。[14]
头痛
由于颅内压升高引起的头痛可能是脑癌的早期症状。[15] 然而,没有其他症状的孤立性头痛是罕见的,并且在头痛变得普遍之前经常会出现其他症状。[15] 头痛的某些警告标志使头痛更容易与脑癌相关。[15] 根据美国神经病学学会的定义,这些是“异常的神经系统检查,Valsalva动作导致的头痛加剧,头痛导致睡眠觉醒,老年人头痛,头痛逐渐加重,头痛特征不典型或不能满足的患者 偏头痛的严格定义“。[15]
特定位置的症状
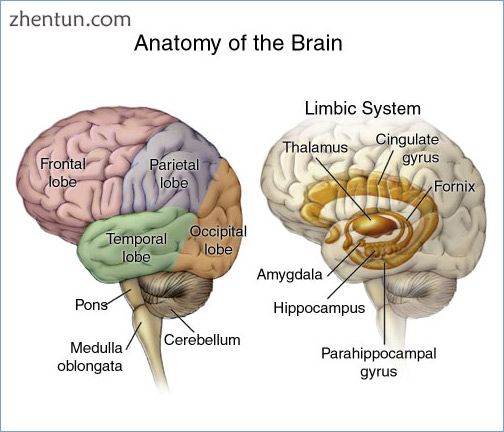
大脑和边缘系统的主要区域
大脑被分成叶,每个叶或区域都有自己的功能。[16] [17]任何这些叶片中的肿瘤都可能影响该区域的表现。所经历的症状通常与肿瘤的位置有关,但每个人可能会遇到不同的情况。[18]
额叶:肿瘤可能导致推理不良,社交行为不当,性格改变,计划不良,抑制率降低,言语产生减少(布罗卡区)。[18]
颞叶:这个肺叶肿瘤可能导致记忆力差,听力丧失,语言理解困难(韦尼克区位于这个肺叶)。[17]
顶叶:这里的肿瘤可能导致对语言的不良解释,说话,写作,绘图,命名和识别的困难,以及差的空间和视觉感知。[19]
枕叶:此叶损伤可能导致视力不佳或视力丧失。[20]
小脑:这个区域的肿瘤可能导致平衡不良,肌肉运动和姿势。[21]
脑干:脑干肿瘤可引起癫痫发作,内分泌问题,呼吸改变,视力改变,头痛和部分麻痹。[21]
行为改变
由于肿瘤破坏大脑的裂片,人的性格可能会改变。由于额叶,颞叶和顶叶[13]控制抑制,情绪,判断,推理和行为,这些地区的肿瘤可能导致不适当的社交行为,[22]脾气暴躁,[22]嘲笑那些不值得笑,[22]甚至是抑郁和焦虑等心理症状。[18]
人格变化可能会产生破坏性影响,如失业,不稳定的关系和缺乏控制。[16]
原因
需要进行流行病学研究以确定风险因素。[23]除了暴露于氯乙烯或电离辐射之外,没有已知的与脑肿瘤相关的环境因素。肿瘤抑制基因(如P53)的突变和缺失被认为是某些形式的脑肿瘤的原因。[24] Von Hippel-Lindau病,结节性硬化症,多发性内分泌肿瘤和2型神经纤维瘤病等遗传性疾病对脑肿瘤的发展具有很高的风险。[1] [25] [26]患有乳糜泻的人患脑瘤的风险略有增加。[27]
尽管研究尚未显示手机或手机辐射与脑肿瘤发生之间存在任何联系,[28]但世界卫生组织已将IARC规模的手机辐射分为2B组 - 可能致癌。[29]手机使用可能导致脑癌的说法可能基于流行病学研究,该研究发现无线和无绳电话的重度用户中胶质瘤风险略有增加。当进行这些研究时,GSM(2G)电话正在使用中。现代的第三代(3G)手机平均释放这些GSM(2G)手机发出的能量的约1%,因此发现手机使用与脑癌风险增加之间的联系并非基于目前的手机使用情况。[3]
病理生理学
脑膜
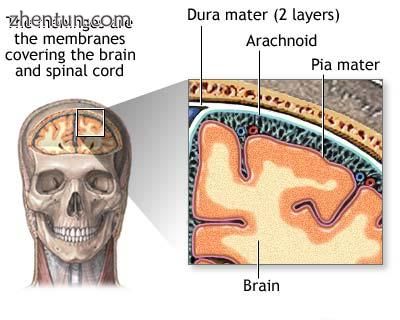
脑膜位于头骨和脑部物质之间。来自脑膜的肿瘤是脑膜瘤。
人脑被称为脑膜的结缔组织膜系统包围,脑膜将脑与颅骨分开。这种三层覆盖物由(从外部进入)硬脑膜,蛛网膜和软脑膜组成。蛛网膜和软脑膜是物理连接的,因此通常被认为是单层,即软脑膜。在蛛网膜和软脑膜之间是包含脑脊髓液(CSF)的蛛网膜下腔。这种液体在细胞之间的狭窄空间内循环,并通过大脑中称为脑室的空腔,以支持和保护脑组织。血管通过软脑膜上方的血管周围空间进入中枢神经系统。血管壁中的细胞紧密连接,形成血脑屏障,保护大脑免受可能通过血液进入的毒素。[30]
脑膜肿瘤是脑膜瘤,通常是良性肿瘤。虽然技术上不是脑组织肿瘤,但它们通常被认为是脑肿瘤,因为它们突出到大脑所在的空间,引起症状。由于它们通常是生长缓慢的肿瘤,因此症状出现时脑膜瘤可能非常大。[31]
脑部问题
人类和其他脊椎动物的大脑由非常柔软的组织组成,并具有明胶样纹理。活体脑组织外部呈灰色(灰质),内部几乎完全白色(白质),颜色微妙变化。大脑的三个最大部门是:
大脑皮质
脑干
小脑[30]
这些区域由两大类细胞组成:神经元和神经胶质。这两种类型在整个大脑中同样多,尽管神经胶质细胞在大脑皮层中的数量大约超过4到1个神经元。 Glia有几种类型,它们具有许多关键功能,包括结构支持,代谢支持,绝缘和发育指导。[32]神经胶质细胞的原发性肿瘤称为神经胶质瘤,在诊断时通常是恶性的。[33]
丘脑和下丘脑是间脑的主要分裂,垂体附着在脑垂体和松果腺; 垂体和松果体的肿瘤通常是良性的。
脑干位于大脑皮层和脊髓之间。 它分为中脑,脑桥和延髓。[30]
脊髓
脊髓被认为是中枢神经系统的一部分。 它由与大脑相同的细胞组成:神经元和神经胶质细胞。[30]
诊断
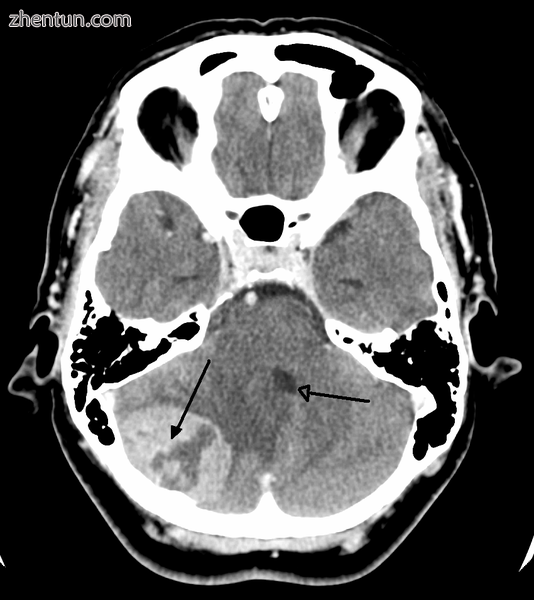
后颅窝肿瘤导致肿块效应和中线移位
虽然没有特定或单一的症状或体征,但症状组合的存在和缺乏其他原因的相应指示可以作为研究脑肿瘤可能性的指标。当涉及到位于身体其他部位的肿瘤的诊断和治疗时,脑肿瘤具有相似的特征和障碍。然而,它们产生了与其所在器官特性密切相关的具体问题。[34]
诊断通常从记录医学前因和当前症状的病史开始。临床和实验室检查将排除感染作为症状的原因。这个阶段的检查可能包括眼睛,耳鼻喉科和电生理检查。脑电图(EEG)的使用通常在脑肿瘤的诊断中起作用。
与身体其他部位的肿瘤相比,脑肿瘤对诊断提出了挑战。通常,由于肿瘤细胞的高活性,放射性示踪剂在肿瘤中大量摄取,允许肿瘤的放射性成像。然而,大部分大脑通过血脑屏障(BBB)与血液分离,血脑屏障是一种严格控制允许哪些物质进入大脑的膜。因此,在肿瘤破坏BBB之前,许多可能容易到达身体其他部位肿瘤的示踪剂将无法到达脑肿瘤。 BBB的破坏通过MRI或CT扫描成像良好,因此被认为是恶性胶质瘤,脑膜瘤和脑转移的主要诊断指标[34]。
儿童脑脊液(CSF)肿胀或阻塞可引起(早期)颅内压增高的迹象,临床表现为头痛,呕吐或意识状态改变,儿童颅骨直径改变和囟门鼓胀。更复杂的症状,如内分泌功能障碍,应该警告医生不要排除脑肿瘤。
双侧颞侧视野缺损(由视交叉压迫引起)或瞳孔扩张,以及发生缓慢进展或局灶性神经系统症状突然发作,如认知和行为障碍(包括判断力受损,记忆力减退) ,缺乏认知,空间定向障碍),人格或情绪变化,偏瘫,感觉减退,失语,共济失调,视野受损,嗅觉受损,听力受损,面瘫,复视或更严重的症状,如震颤,瘫痪在身体偏瘫的一侧,或癫痫病史阴性的患者(癫痫)癫痫发作,应该提高脑肿瘤的可能性。
成像
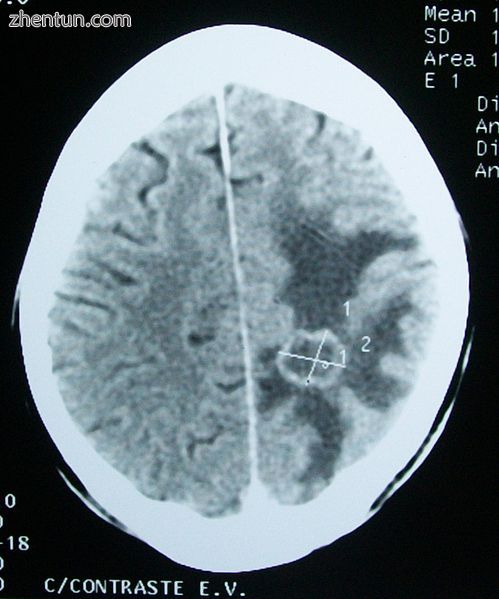
脑肿瘤的CT扫描,其直径标记为X.在周围的白质中存在低衰减(暗)肿瘤周围水肿,具有“手指状”扩散。
医学成像在脑肿瘤的诊断中起着重要作用。早期成像方法 - 侵入性和有时危险 - 如脑血管造影和脑血管造影已被放弃,有利于非侵入性,高分辨率技术,尤其是磁共振成像(MRI)和计算机断层扫描(CT)扫描,尽管MRI通常是使用的参考标准。[35]肿瘤通常在CT或MRI结果中显示为不同颜色的肿块(也称为过程)。
在CT扫描中,良性脑肿瘤通常表现为低密度(比脑组织更暗)的肿块。在MRI上,它们在T1加权扫描中出现低密度或等强度(与脑组织相同的强度),或在T2加权MRI上出现高信号(比脑组织更亮),尽管外观是可变的。
在大多数恶性原发性和转移性脑肿瘤中,可以在CT或MRI扫描中证明对比剂摄取,有时以特征模式摄取。
脑组织被肿瘤压缩的压力区域在T2加权扫描中也显示高信号,并且可能表明由于轮廓不清楚而存在弥漫性肿瘤。肿瘤周围肿胀称为肿瘤周围水肿也可以显示类似的结果。
这是因为这些肿瘤破坏了BBB的正常功能并导致其渗透性增加。最近,已经进步以增加MRI在提供有助于诊断和预后的生理数据方面的效用。灌注加权成像(PWI)和扩散加权成像(DWI)是两种MRI技术,已经证明这些技术可用于按等级对肿瘤进行分类,这在以前仅使用结构成像是不可行的。[36]然而,这些技术不能单独诊断高级别和低级别的胶质瘤,因此脑肿瘤​​的确定诊断只能通过对通过脑活组织检查或开放手术获得的肿瘤组织样本进行组织学检查来确认。组织学检查对于确定适当的治疗和正确的预后至关重要。由病理学家进行的该检查通常具有三个阶段:新鲜组织的术中检查,制备的组织的初步显微镜检查,以及免疫组织化学染色或遗传分析后制备的组织的后续检查。
病理
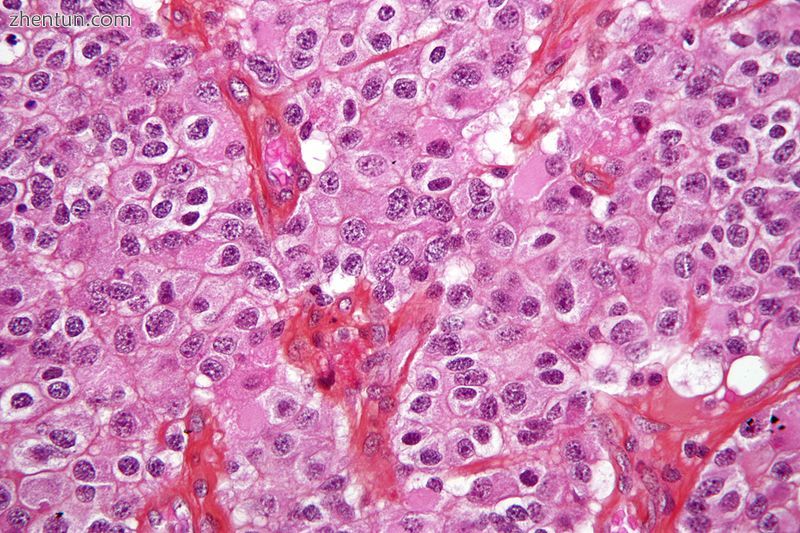
少突神经胶质瘤的显微照片,一种脑癌。脑活组织检查。 H&E染色
肿瘤具有允许确定恶性肿瘤以及它们将如何进化的特征,并且确定这些特征将允许医疗团队确定管理计划。
变形或去分化:细胞分化和它们彼此的定向和血管的缺失,这是间变性肿瘤组织的特征。间变细胞已失去对其正常功能的完全控制,并且许多细胞结构恶化。间变细胞通常具有异常高的核 - 细胞质比率,并且许多是多核的。另外,间变性细胞的细胞核通常是不自然的形状或过大的。细胞可以通过两种方式变为间变性:肿瘤性肿瘤细胞可以去分化成为变性(去分化导致细胞失去其所有正常结构/功能),或者癌症干细胞可以增加它们繁殖的能力(即,由于无法控制的生长分化失败)。
Atypia:细胞异常的指征(可能是恶性肿瘤的指征)。异常的重要性高度依赖于背景。
瘤形成:细胞的(不受控制的)分裂。因此,瘤形成没有问题,但其后果是:细胞的不受控制的分裂意味着肿瘤的质量增加,并且在诸如颅内腔的狭窄空间中这很快变得有问题,因为质量侵入了空间。大脑将它推到一边,导致脑组织受压,颅内压增高,脑实质受到破坏。颅内压增高(ICP)可归因于肿瘤的直接质量效应,血容量增加或脑脊液(CSF)体积增加,这可能反过来具有继发症状。
坏死:由感染,毒素或创伤等外部因素引起的细胞(过早)死亡。坏死细胞发出错误的化学信号,阻止吞噬细胞处理死细胞,导致坏死细胞部位或附近死亡组织,细胞碎片和毒素累积[37]
当肿瘤利用附近的血管供应血液并且肿瘤进入与周围脑组织的营养竞争时,就会发生动脉和静脉缺氧,或剥夺大脑某些区域的充足氧气供应。
更一般地,肿瘤可以引起代谢终产物(例如,自由基,改变的电解质,神经递质)的释放,以及破坏正常实质功能的细胞介质(例如,细胞因子)的释放和募集。
分类
肿瘤可以是良性的或恶性的,可以发生在大脑的不同部位,并且可以分类为原发性或继发性。原发性肿瘤是在大脑中开始的肿瘤,与转移性肿瘤相反,转移性肿瘤是从身体的另一个区域扩散到大脑的肿瘤。[38]转移性肿瘤的发病率约为原发性肿瘤的4倍[9]。肿瘤可能有症状也可能没有症状:一些肿瘤被发现,因为患者有症状,其他肿瘤偶然出现在成像扫描或尸检时。
中枢神经系统肿瘤的分级通常发生在1993年世界卫生组织创建的4分制(I-IV)上.I级肿瘤是最不严重的并且通常与长期存活相关,严重程度和预后恶化随着年级的增加。低级别肿瘤通常是良性的,而较高级别的肿瘤是恶性和/或转移性的。其他分级量表确实存在,许多基于与WHO量表相同的标准,并从I-IV分级。
主要
最常见的原发性脑肿瘤是:[39]
胶质瘤(50.4%)
脑膜瘤(20.8%)
垂体腺瘤(15%)
神经鞘瘤(8%)
这些常见肿瘤也可根据原始组织进行组织,如下所示:[40]
组织起源
次要
大脑的继发性肿瘤是转移性的,并且已经从源自其他器官的癌症侵入大脑。这意味着癌症肿瘤已经在身体其他部位的另一个器官中发展,癌细胞从原发肿瘤中泄漏,然后进入淋巴系统和血管。然后它们在血液中循环,并沉积在大脑中。在那里,这些细胞继续生长和分裂,成为原发性癌组织的另一种侵袭性肿瘤。在患有无法治愈的转移性癌症的患者的末期,脑的继发性肿瘤非常常见;导致脑部继发性肿瘤的最常见类型的癌症是肺癌,乳腺癌,恶性黑素瘤,肾癌和结肠癌(按频率递减顺序)。
继发性脑肿瘤比原发性肿瘤更常见;在美国,每年约有170,000例新病例。继发性脑肿瘤是颅内腔肿瘤的最常见原因。颅骨结构也可能受到肿瘤的影响,这种肿瘤本质上会减少颅内腔的体积,并可能损害大脑。[41]
按行为
脑肿瘤或颅内肿瘤可以是癌性(恶性)或非癌性(良性)。然而,恶性或良性肿瘤的定义不同于体内其他类型的癌性或非癌性肿瘤中常见的定义。在身体其他部位的癌症中,三种恶性特征将良性肿瘤与恶性癌症形式区分开来:良性肿瘤是自限性的,不会侵入或转移。恶性肿瘤的特征包括:
不受控制的有丝分裂(超出正常范围的分裂增长)
anaplasia:肿瘤中的细胞形态(大小和形状)明显不同。间变性细胞显示出明显的多形性。细胞核特征性地极度染色深(染黑)并扩大;细胞核可能与细胞的细胞质具有相同的大小(核 - 细胞质比率可能接近1:1,而不是正常的1:4或1:6比例)。巨细胞 - 比它们的邻居大得多 - 可能形成并拥有一个巨大的核或几个核(合胞体)。间变核在大小和形状上是可变的和奇异的。
入侵或渗透(医学文献使用这些术语作为同义词等同。但是,为了清楚起见,下面的文章遵循一个约定略有不同的约定;这些约定不在这些文章之外):
入侵或侵入是肿瘤通过不受控制的有丝分裂的空间扩张,在这种意义上,肿瘤侵入邻近组织占据的空间,从而将其他组织推到一边并最终压迫组织。这些肿瘤通常与成像中明显轮廓的肿瘤相关。
浸润是肿瘤的生长(微观)触须进入周围组织(通常使肿瘤的轮廓不明确或扩散)或使肿瘤细胞“接种”到肿瘤周围超出肿瘤块周围的组织中的行为;这并不意味着浸润性肿瘤不会占据空间或在周围组织生长时不会压迫周围组织,但是渗透性肿瘤使得难以说出肿瘤结束的位置和健康组织的开始。
转移(通过淋巴或血液扩散到身体的其他部位)。
在上述恶性特征中,某些元素不适用于大脑原发性肿瘤:
原发性脑肿瘤很少转移到其他器官;某些形式的原发性脑肿瘤可以转移,但不会扩散到颅内腔或中央椎管外。由于BBB,原发性肿瘤的癌细胞不能进入血流并被带到体内的另一个位置。 (偶尔的孤立病例报告表明某些脑肿瘤在中枢神经系统外扩散,例如多形性胶质母细胞瘤的骨转移[42])
原发性脑肿瘤通常是侵入性的(即它们将在空间上扩张并侵入其他脑组织占据的空间并压缩那些脑组织);然而,一些更恶性的原发性脑肿瘤会渗入周围组织。
通过遗传学
2016年,世界卫生组织对某些类别的胶质瘤进行了重组,包括可用于区分肿瘤类型,预后和治疗反应的不同基因突变。通常通过免疫组织化学检测基因突变,免疫组织化学是一种通过染色可视化目标蛋白质存在与否的技术[35]。
IDH1和IDH2基因的突变常见于低级别胶质瘤
IDH基因的丢失与染色体臂1p和19q的丧失相结合表明肿瘤是少突神经胶质瘤
TP53和ATRX的缺失是星形细胞瘤的特征
基因EFGR,TERT和PTEN通常在胶质瘤中发生改变,可用于区分肿瘤分级和生物学[35]。
具体类型
主要文章:WHO中枢神经系统肿瘤的分类
间变性星形细胞瘤,星形细胞瘤,中枢神经细胞瘤,脉络丛癌,脉络丛乳头状瘤,脉络丛肿瘤,胚胎发育不良神经上皮肿瘤,室管膜瘤,纤维星形细胞瘤,巨细胞胶质母细胞瘤,多形性胶质母细胞瘤,脑胶质瘤病,胶质瘤,血管外皮细胞瘤,成神经管细胞瘤,髓母细胞瘤,脑膜瘤癌病,神经母细胞瘤,神经细胞瘤,少星形细胞瘤,少突神经胶质瘤,视神经鞘膜脑膜瘤,小儿室管膜瘤,Pilocytic星形细胞瘤,松果体细胞瘤,松细胞瘤,多形性间变性神经母细胞瘤,多形性黄色星形细胞瘤,原发性中枢神经系统淋巴瘤,蝶骨翼膜脑膜瘤,室管膜下巨细胞星形细胞瘤,室管膜下瘤,三边形视网膜母细胞瘤。
治疗
医疗团队通常评估治疗方案并将其呈现给受影响的人及其家人。根据肿瘤的类型和位置,可以提供各种类型的治疗,并且可以组合起来以产生最佳的生存机会:
手术:完全或部分切除肿瘤,目的是尽可能多地去除肿瘤细胞。
放射治疗:脑肿瘤最常用的治疗方法;用β,X射线或γ射线照射肿瘤。
化疗:癌症的一种治疗选择,然而,它并不总是用于治疗脑肿瘤,因为血脑屏障可以阻止一些药物到达癌细胞。
通过临床试验可获得各种实验疗法。
原发性脑肿瘤的存活率取决于肿瘤的类型,年龄,患者的功能状态,手术切除的程度以及每种病例特有的其他因素。[43]
手术
医学文献中描述的主要和最期望的作用过程是通过开颅手术切除(切除)。微创技术正成为神经外科肿瘤学的主流趋势。[44]手术的主要目的是尽可能多地去除肿瘤细胞,完全去除是肿瘤的最佳结果和细胞减少术(“减灭”)。在某些情况下,不可能进入肿瘤,阻碍或禁止手术。
除了位于颅底的一些肿瘤外,许多脑膜瘤可通过外科手术成功切除。大多数垂体腺瘤可通过手术切除,通常采用微创方法通过鼻腔和颅底(经鼻,经蝶窦入路)。大型垂体腺瘤需要开颅(开放颅骨)才能切除。包括立体定向方法在内的放射治疗仅适用于不能手术的病例。
目前的一些研究旨在通过用5-氨基乙酰丙酸标记肿瘤细胞来改善脑肿瘤的手术切除,使其发荧光。[45]术后放疗和化疗是恶性肿瘤治疗标准的组成部分。当无法通过外科手术实现显着的肿瘤减少时,在“低级”神经胶质瘤的情况下也可以施用放射疗法。
多发性转移性肿瘤通常用放疗和化学疗法而不是手术治疗,并且在这种情况下的预后由原发性肿瘤决定,并且通常较差。
放射治疗
放射治疗的目标是杀死肿瘤细胞,同时保持正常脑组织不受伤害。在标准的外部射束放射治疗中,对大脑施加标准剂量“分数”辐射的多种治疗。根据肿瘤的类型,重复该过程总共10至30次治疗。这种额外的治疗为一些患者提供了改善的结果和更长的存活率。
放射外科是一种治疗方法,其使用计算机化计算将辐射聚焦在肿瘤部位,同时最小化对周围脑的辐射剂量。放射外科可能是其他治疗的辅助手段,或者它可能代表某些肿瘤的主要治疗技术。使用的形式包括立体定向放射外科,如伽玛刀,Cyber​​knife或Novalis Tx放射外科。[46] [不可靠的医疗来源?]
放射治疗是继发性脑肿瘤最常见的治疗方法。放射治疗的数量取决于受癌症影响的大脑区域的大小。如果将来有其他继发性肿瘤发生风险,可以建议常规外照射“全脑放射治疗”(WBRT)或“全脑照射”。[47]在涉及少于三个小的继发性脑肿瘤的病例中通常推荐立体定向放射疗法。放射疗法可以在切除肿瘤之后使用,或者在某些情况下代替切除肿瘤。用于脑癌的放射治疗形式包括最常见的外照射放射治疗,近距离放射治疗和质子治疗,最后一种特别用于儿童。
接受立体定向放射外科(SRS)和全脑放射治疗(WBRT)治疗转移性脑肿瘤的患者发生学习和记忆问题的风险是单独使用SRS治疗的两倍多。[48] [49]
化疗
接受化疗的患者服用旨在杀死肿瘤细胞的药物。尽管化疗可以改善患有最恶性原发性脑肿瘤的患者的总体存活率,但仅在约20%的患者中这样做。化学疗法通常用于幼儿而不是辐射,因为辐射可能对发育中的大脑产生负面影响。开出这种治疗方案的决定取决于患者的整体健康状况,肿瘤类型和癌症程度。药物的毒性和许多副作用,以及化疗在脑肿瘤中的不确定结果使得该治疗进一步降低了治疗选择的范围,优选手术和放射治疗。
加州大学洛杉矶分校神经肿瘤学公布了诊断为多形性胶质母细胞瘤的患者的实时生存数据。他们是美国唯一一家展示脑肿瘤患者如何在现有疗法上表现的机构。他们还列出了用于治疗高级别胶质瘤肿瘤的化疗药物清单。[50]
基因突变对化疗的有效性有显着影响。具有IDH1或IDH2突变的神经胶质瘤比没有突变的神经胶质瘤对化学疗法的反应更好。染色体臂1p和19q的丢失也表明对化放疗的反应更好。[35]
其他
分流可用于缓解由颅内压引起的症状,通过减少由脑脊液自由流动阻塞引起的液体积聚(脑积水)。[51]
预测
脑癌的预后取决于诊断的癌症类型。髓母细胞瘤在化疗,放疗和手术切除方面具有良好的预后,而多形性胶质母细胞瘤的中位生存期仅为12个月,即使采用积极的放化疗和手术治疗也是如此。脑干胶质瘤对任何形式的脑癌都有最差的预后,大多数患者在一年内死亡,即使治疗通常包括对肿瘤的放射以及皮质类固醇。然而,一种类型的儿童局灶性脑干胶质瘤似乎可以预见到特殊的预后,并且经常报道长期存活[52]。
预后也受基因突变的影响。某些突变比其他突变提供更好的预后。胶质瘤中的IDH1和IDH2突变以及染色体臂1p和19q的缺失通常表明预后更好。 TP53,ATRX,EGFR,PTEN和TERT突变也可用于确定预后。[35]
多形性胶质母细胞瘤
主要文章:多形性胶质母细胞瘤
多形性胶质母细胞瘤(GBM)是最具侵袭性(IV级)和最常见的恶性脑肿瘤形式。即使使用由放射疗法,化学疗法和手术切除组成的积极的多模式疗法,中位生存期仅为12-17个月。多形性胶质母细胞瘤的标准疗法包括肿瘤的最大手术切除,然后在手术后2至4周进行放射治疗以除去癌症,然后通过化学疗法,例如替莫唑胺。[53]大多数胶质母细胞瘤患者在患病期间服用皮质类固醇,通常是地塞米松,以缓解症状。实验性治疗包括靶向治疗,伽玛刀放射外科治疗,[54]硼中子俘获治疗和基因治疗。[55] [56]
少突胶质细胞
主要文章:少突神经胶质瘤
少突神经胶质瘤是无法治愈的但是缓慢进展的恶性脑肿瘤。它们可以通过手术切除,化疗,放疗或联合治疗。对于一些疑似低度(II级)肿瘤,只选择一个观察等待和对症治疗的过程。这些肿瘤分别显示染色体1和染色体19的p和q臂共同缺失的高频率(1p19q共缺失),并且已发现其特别是化学敏感性,一份报告声称它们是最具化学敏感性的肿瘤之一。 [57]。据报道,II级少突神经胶质瘤的中位生存期高达16.7岁。[58]
听神经瘤
听神经瘤是非癌性肿瘤。[59]它们可以通过手术,放射疗法或观察来治疗。建议尽早进行手术或放射治疗,以防止进行性听力损失。[60]
流行病学
大脑癌症发病率数据显示,发达国家和欠发达国家之间存在显着差异(欠发达国家的大脑肿瘤发病率较低)。[61]这可以解释为未确诊的肿瘤相关死亡(极端恶劣情况下的患者无法诊断,仅仅是因为他们无法获得诊断脑肿瘤所需的现代诊断设施)以及其他贫困相关原因导致的死亡在肿瘤发展或肿瘤危及生命之前抢先患病。然而,统计数据表明某些形式的原发性脑肿瘤在某些人群中更为常见。[62]
低级别星形细胞瘤的发病率并未显示出与国籍有显着差异。然而,检查恶性中枢神经系统(CNS)肿瘤发病率的研究显示出一些与国籍有关的变异。由于一些高度病变来自低度恶性肿瘤,因此值得一提的是这些趋势。具体而言,美国,以色列和北欧国家中枢神经系统肿瘤的发病率相对较高,而日本和亚洲国家的发病率较低。这些差异可能反映了一些生物学差异以及病理诊断和报告的差异。[63]有关癌症发病率的全球数据可在世界卫生组织(世界卫生组织)上找到,并由位于法国的IARC(国际癌症研究机构)处理。[64]
美国
在2015年的美国,大约有166,039人患有脑部或其他中枢神经系统肿瘤。 2018年,预计2018年将有23,880例新发脑肿瘤和16830例死亡,[62]占所有癌症的1.4%,占所有癌症死亡的2.8%。[65]诊断的中位年龄为58岁,而死亡的中位年龄为65岁。男性的诊断稍微多一点,每10万人约7.5例,而女性在5.4岁时减少2例。男性死于脑癌的死亡率为每10万人5.3例,女性死亡人数为每10万人3.6例,这使得脑癌成为美国癌症死亡的第10大原因。男性和女性患脑癌的总体终生风险约为0.6%[62] [66]。
UK
脑,其他中枢神经系统或颅内肿瘤是英国第九大常见癌症(2013年约有10,600人被诊断出),并且是导致癌症死亡的第八大常见原因(2012年约有5,200人死亡)。[67]
儿童
在美国,估计有超过28,000名20岁以下的人患有脑瘤。[68]预计2019年15岁以下的人将诊断出约3,720例新的脑肿瘤病例。[69] 1985 - 1994年报告的比率高于1975 - 1983年。关于原因存在一些争论;一种理论认为,趋势是改进诊断和报告的结果,因为跳跃发生在MRI广泛可用的同时,并且死亡率没有同步跳跃。中枢神经系统肿瘤占儿童癌症的20-25%[70] [65] [71]。
儿童所有原发性脑癌的平均存活率为74%。[68]脑癌是19岁以下儿童中最常见的癌症,导致该组死亡率高于白血病。[72]年纪较小的人做得不太好。[73]
儿童(0-14)中最常见的脑肿瘤类型是:毛细胞星形细胞瘤,恶性神经胶质瘤,成神经管细胞瘤,神经元和混合神经胶质瘤,以及室管膜瘤。
在2岁以下儿童中,约70%的脑肿瘤是成神经管细胞瘤,室管膜瘤和低级别胶质瘤。不太常见,通常在婴儿中看到的是畸胎瘤和非典型的畸形性横纹肌样瘤。[74]生殖细胞肿瘤,包括畸胎瘤,仅占儿科原发性脑肿瘤的3%,但全球发病率差异很大。[75]
在英国,每年平均有429名14岁及以下儿童被诊断出患有脑瘤,并且诊断出563名19岁以下的儿童和青少年。[76]
研究
免疫治疗
正在积极研究癌症免疫疗法。对于恶性胶质瘤,截至2015年,没有任何治疗方法可以改善预期寿命。[77]
水泡性口炎病毒
另见:溶瘤病毒
2000年,研究人员使用水泡性口炎病毒(VSV)来感染和杀死癌细胞而不影响健康细胞。[78] [79]
逆转录病毒复制载体
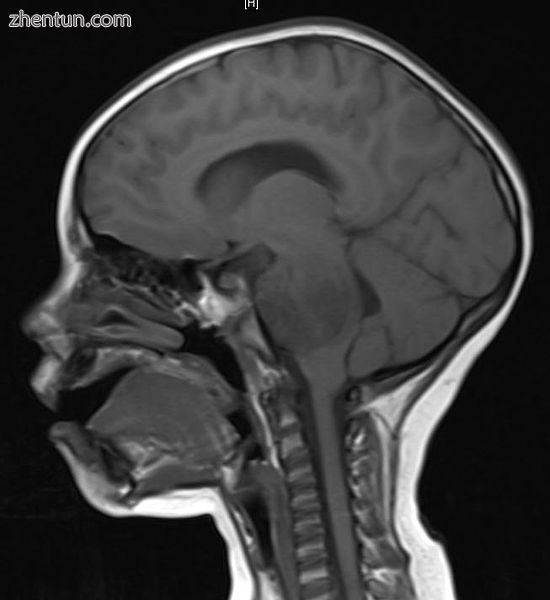
四岁时的脑干胶质瘤。 MRI,矢状,无对比
在南加州大学洛杉矶分校的研究人员Nori Kasahara教授的带领下,2001年报告了第一个成功应用逆转录病毒复制载体用于转导实体瘤细胞系的实例。[80] 在这项初步工作的基础上,研究人员将这项技术应用于癌症的体内模型,2005年报告了一项实验性脑肿瘤动物模型的长期生存获益[81] [不可靠的医疗来源?]随后,为人类做准备 临床试验中,该技术由Tocagen(一家主要致力于脑癌治疗的制药公司)进一步开发,作为组合治疗(Toca 511和Toca FC)。 自2010年以来,该项目一直在进行I / II期临床试验,目的是治疗复发性高级别胶质瘤,包括多形性胶质母细胞瘤(GBM)和间变性星形细胞瘤。 尚未公布任何结果。[82]
另见:
Timeline of brain cancer
List of notable brain tumor patients
Pituitary adenomas ("pituitary tumours") are sometimes incorrectly referred to as a brain tumours.[83][84] This is perhaps because the pituitary gland is in the skull, however it is not part of the brain. Pituitary adenomas are rarely cancerous.
参考:
"Adult Brain Tumors Treatment". NCI. 28 February 2014. Archived from the original on 5 July 2014. Retrieved 8 June 2014.
"General Information About Adult Brain Tumors". NCI. 14 April 2014. Archived from the original on 5 July 2014. Retrieved 8 June 2014.
"Chapter 5.16". World Cancer Report 2014. World Health Organization. 2014. ISBN 978-9283204299. Archived from the original on 19 September 2016.
"Cancer of the Brain and Other Nervous System - Cancer Stat Facts". SEER. Retrieved 22 July 2019.
GBD 2015 Disease and Injury Incidence and Prevalence, Collaborators. (8 October 2016). "Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1545–1602. doi:10.1016/S0140-6736(16)31678-6. PMC 5055577. PMID 27733282.
GBD 2015 Mortality and Causes of Death, Collaborators. (8 October 2016). "Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980–2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1459–1544. doi:10.1016/S0140-6736(16)31012-1. PMC 5388903. PMID 27733281.
Longo, Dan L (2012). "369 Seizures and Epilepsy". Harrison's principles of internal medicine (18th ed.). McGraw-Hill. p. 3258. ISBN 978-0-07-174887-2.
"Benign brain tumour (non-cancerous)". nhs.uk. 20 October 2017. Retrieved 29 July 2019.
Merrel RT (December 2012). "Brain tumors". Disease-a-Month. 58 (12): 678–89. doi:10.1016/j.disamonth.2012.08.009. PMID 23149521.
World Cancer Report 2014. World Health Organization. 2014. pp. Chapter 1.3. ISBN 978-9283204299.
"Brain Tumour Facts 2011" (PDF). Brain Tumour Alliance Australia. Archived from the original (PDF) on 25 January 2014. Retrieved 9 June 2014.
"Brain Tumors". Archived from the original on 12 August 2016. Retrieved 2 August 2016.
"Mood Swings and Cognitive Changes | American Brain Tumor Association". www.abta.org. Archived from the original on 2 August 2016. Retrieved 3 August 2016.
"Coping With Personality & Behavioral Changes". www.brainsciencefoundation.org. Archived from the original on 30 July 2016. Retrieved 3 August 2016.
Kahn, Kevin; Finkel, Alan (June 2014). "It IS a tumor -- current review of headache and brain tumor". Current Pain and Headache Reports. 18 (6): 421. doi:10.1007/s11916-014-0421-8. ISSN 1534-3081. PMID 24760490.
Gregg, N. (2014). "Neurobehavioural Changes In Patients Following Brain Tumour: Patients And Relatives Perspective". Supportive Care in Cancer.
"Coping With Personality & Behavioral Changes". www.brainsciencefoundation.org. Archived from the original on 30 July 2016. Retrieved 27 July 2016.
"Mood Swings and Cognitive Changes | American Brain Tumor Association". www.abta.org. Archived from the original on 15 August 2016. Retrieved 27 July 2016.
Warnick, MD, Ronald (August 2018). "Brain Tumors: an introduction". Mayfield Brain and Spine Clinic. Retrieved 6 March 2019.
"Changes in Vision - Brain Tumour Symptoms". www.thebraintumourcharity.org. Retrieved 9 February 2018.
"Brain Tumors". Children's Hospital of Wisconsin. 6 March 2019.
Jones, Caleb. "Brain Tumor Symptoms | Miles for Hope | Brain Tumor Foundation". milesforhope.org. Archived from the original on 14 August 2016. Retrieved 3 August 2016.
Krishnatreya, M; Kataki, AC; Sharma, JD; Bhattacharyya, M; Nandy, P; Hazarika, M (2014). "Brief descriptive epidemiology of primary malignant brain tumors from North-East India". Asian Pacific Journal of Cancer Prevention. 15 (22): 9871–73. doi:10.7314/apjcp.2014.15.22.9871. PMID 25520120.
Kleihues P, Ohgaki H, Eibl RH, Reichel MB, Mariani L, Gehring M, Petersen I, Höll T, von Deimling A, Wiestler OD, Schwab M (1994). "Type and frequency of p53 mutations in tumors of the nervous system and its coverings". Molecular Neuro-oncology and Its Impact on the Clinical Management of Brain Tumors. Recent results in cancer research. 135. Springer. pp. 25–31. ISBN 978-3540573517.
Hodgson TS, Nielsen SM, Lesniak MS, Lukas RV (2016). "Neurological Management of Von Hippel-Lindau Disease". Neurologist (Review). 21 (5): 73–78. doi:10.1097/NRL.0000000000000085. PMID 27564075.
Rogers L, Barani I, Chamberlain M, Kaley TJ, McDermott M, Raizer J, et al. (2015). "Meningiomas: knowledge base, treatment outcomes, and uncertainties. A RANO review". J Neurosurg (Review). 122 (1): 4–23. doi:10.3171/2014.7.JNS131644. PMC 5062955. PMID 25343186.
Hourigan CS (2006). "The molecular basis of coeliac disease". Clin Exp Med (Review). 6 (2): 53–59. doi:10.1007/s10238-006-0095-6. PMID 16820991.
Frei P, Poulsen AH, Johansen C, Olsen JH, Steding-Jessen M, Schüz J (19 October 2011). "Use of mobile phones and risk of brain tumours: update of Danish cohort study". BMJ. 343: d6387. doi:10.1136/bmj.d6387. PMC 3197791. PMID 22016439.
"IARC classifies radiofrequency electromagnetic fields as possibly carcinogenic to humans" (PDF). World Health Organization press release N° 208 (Press release). International Agency for Research on Cancer. 31 May 2011. Archived (PDF) from the original on 1 June 2011. Retrieved 2 June 2011.
Moore, Keith L. (September 2017). Clinically oriented anatomy. Agur, A. M. R.,, Dalley, Arthur F., II (Eighth ed.). Philadelphia. ISBN 9781496347213. OCLC 978362025.
"Meningioma Brain Tumor". neurosurgery.ucla.edu. Retrieved 29 July 2019.
"Neurons & Glial Cells | SEER Training". training.seer.cancer.gov. Retrieved 29 July 2019.
Ostrom, Quinn T.; Gittleman, Haley; Farah, Paul; Ondracek, Annie; Chen, Yanwen; Wolinsky, Yingli; Stroup, Nancy E.; Kruchko, Carol; Barnholtz-Sloan, Jill S. (November 2013). "CBTRUS Statistical Report: Primary Brain and Central Nervous System Tumors Diagnosed in the United States in 2006-2010". Neuro-Oncology. 15 (Suppl 2): ii1–ii56. doi:10.1093/neuonc/not151. ISSN 1522-8517. PMC 3798196. PMID 24137015.
Herholz, Karl; Langen, Karl-Josef; Schiepers, Christiaan; Mountz, James M. (2012). "Brain Tumors". Seminars in Nuclear Medicine. 42 (6): 356–70. doi:10.1053/j.semnuclmed.2012.06.001. PMC 3925448. PMID 23026359.
Iv, Michael; Yoon, Byung C.; Heit, Jeremy J.; Fischbein, Nancy; Wintermark, Max (January 2018). "Current Clinical State of Advanced Magnetic Resonance Imaging for Brain Tumor Diagnosis and Follow Up". Seminars in Roentgenology. 53 (1): 45–61. doi:10.1053/j.ro.2017.11.005. ISSN 1558-4658. PMID 29405955.
Margiewicz, Stefan; Cordova, Christine; Chi, Andrew S.; Jain, Rajan (January 2018). "State of the Art Treatment and Surveillance Imaging of Glioblastomas". Seminars in Roentgenology. 53 (1): 23–36. doi:10.1053/j.ro.2017.11.003. ISSN 1558-4658. PMID 29405952.
MedlinePlus Encyclopedia Necrosis
"What you need to know about brain tumors". National Cancer Institute. Archived from the original on 27 January 2012. Retrieved 25 February 2012.
Park, Bong Jin; Kim, Han Kyu; Sade, Burak; Lee, Joung H. (2009). "Epidemiology". In Lee, Joung H. (ed.). Meningiomas: Diagnosis, Treatment, and Outcome. Springer. p. 11. ISBN 978-1-84882-910-7.
"Classifications of Brain Tumors". AANS. American Association of Neurological Surgeons. Archived from the original on 24 April 2017. Retrieved 23 April 2017.
MedlinePlus Encyclopedia Metastatic brain tumor
Frappaz D, Mornex F, Saint-Pierre G, Ranchere-Vince D, Jouvet A, Chassagne-Clement C, Thiesse P, Mere P, Deruty R (1999). "Bone metastasis of glioblastoma multiforme confirmed by fine needle biopsy". Acta Neurochirurgica. 141 (5): 551–52. doi:10.1007/s007010050342. PMID 10392217.
Nicolato, Antonio; Gerosa, Massimo A.; Fina, Paolo; Iuzzolino, Paolo; Giorgiutti, Fabrizia; Bricolo, Albino (1995). "Prognostic factors in low-grade supratentorial astrocytomas: A uni-multivariate statistical analysis in 76 surgically treated adult patients". Surgical Neurology. 44 (3): 208–21, discussion 221–23. doi:10.1016/0090-3019(95)00184-0. PMID 8545771.
Spetzler RF, Sanai N (2012). "The quiet revolution: Retractorless surgery for complex vascular and skull base lesions". Journal of Neurosurgery. 116 (2): 291–300. doi:10.3171/2011.8.JNS101896. PMID 21981642.
Paul Brennan (4 August 2008). "Introduction to brain cancer". cliniclog.com. Archived from the original on 17 February 2012. Retrieved 19 December 2011.
"Radiosurgery treatment comparisons – Cyberknife, Gamma knife, Novalis Tx". Archived from the original on 20 May 2007. Retrieved 22 July 2014.
"Treating secondary brain tumours with WBRT". Cancer Research UK. Archived from the original on 25 October 2007. Retrieved 5 June 2012.
"Whole Brain Radiation increases risk of learning and memory problems in cancer patients with brain metastases". MD Anderson Cancer Center. Archived from the original on 5 October 2008. Retrieved 5 June 2012.
"Metastatic brain tumors". International RadioSurgery Association. Archived from the original on 16 June 2012. Retrieved 5 June 2012.
"How Our Patients Perform: Glioblastoma Multiforme". UCLA Neuro-Oncology Program. Archived from the original on 9 June 2012. Retrieved 5 June 2012.
Dalvi A. "Normal Pressure Hydrocephalus Causes, Symptoms, Treatment". eMedicineHealth. Emedicinehealth.com. Archived from the original on 22 February 2012. Retrieved 17 February 2012.
"Brain Stem Gliomas in Childhood". Childhoodbraintumor.org. Archived from the original on 9 March 2012. Retrieved 17 February 2012.
Sasmita, Andrew Octavian; Wong, Ying Pei; Ling, Anna Pick Kiong (1 February 2018). "Biomarkers and therapeutic advances in glioblastoma multiforme". Asia-Pacific Journal of Clinical Oncology. 14 (1): 40–51. doi:10.1111/ajco.12756. ISSN 1743-7563. PMID 28840962.
"GBM Guide – MGH Brain Tumor Center". Brain.mgh.harvard.edu. Archived from the original on 16 February 2012. Retrieved 17 February 2012.
Chien-Kuo Tai; Noriyuki Kasahara (1 January 2008). "Replication-competent retrovirus vectors for cancer gene therapy" (PDF). Frontiers in Bioscience. 13 (13): 3083–95. doi:10.2741/2910. PMID 17981778. Archived from the original (PDF) on 19 March 2012.
Murphy AM, Rabkin SD (April 2013). "Current status of gene therapy for brain tumors". Transl. Res. 161 (4): 339–54. doi:10.1016/j.trsl.2012.11.003. PMC 3733107. PMID 23246627.
Ty AU, See SJ, Rao JP, Khoo JB, Wong MC (January 2006). "Oligodendroglial tumor chemotherapy using "decreased-dose-intensity" PCV: a Singapore experience". Neurology. 66 (2): 247–49. doi:10.1212/01.wnl.0000194211.68164.a0. PMID 16434664. Archived from the original on 20 July 2008.
"Neurology". Neurology. Archived from the original on 19 February 2012. Retrieved 17 February 2012.
"Acoustic Neuroma (Vestibular Schwannoma)". www.hopkinsmedicine.org. Retrieved 19 July 2019.
"UpToDate". www.uptodate.com. Retrieved 19 July 2019.
Bondy ML, Scheurer ME, Malmer B, et al. (2008). "Brain Tumor Epidemiology: Consensus from the Brain Tumor Epidemiology Consortium (BTEC)". Cancer. 113 (7 Suppl): 1953–68. doi:10.1002/cncr.23741. PMC 2861559. PMID 18798534.
"Cancer Stat Facts: Brain and Other Nervous System Cancer". National Cancer Institute. 31 March 2019.
Jallo GI, Benardete EA (January 2010). "Low-Grade Astrocytoma". Archived from the original on 27 July 2010.
"CANCERMondial". International Agency for Research on Cancer. Archived from the original on 17 February 2012. Retrieved 17 February 2012.
"What are the key statistics about brain and spinal cord tumors?". American Cancer Society. 1 May 2012. Archived from the original on 2 July 2012.
"2018 CBTRUS Fact Sheet". Central Brain Tumor Registry of the United States. 31 March 2019.
"Brain, other CNS and intracranial tumours statistics". Cancer Research UK. Archived from the original on 16 October 2014. Retrieved 27 October 2014.
"Quick Brain Tumor Facts". National Brain Tumor Society. Retrieved 14 February 2019.
"CBTRUS - 2018 CBTRUS Fact Sheet". www.cbtrus.org. Retrieved 14 February 2019.
Hoda, Syed A; Cheng, Esther (6 November 2017). "Robbins Basic Pathology". American Journal of Clinical Pathology. 148 (6): 557. doi:10.1093/ajcp/aqx095. ISSN 0002-9173.
Chamberlain MC, Kormanik PA (February 1998). "Practical guidelines for the treatment of malignant gliomas". West. J. Med. 168 (2): 114–20. PMC 1304839. PMID 9499745.
"Childhood Brain Cancer Now Leads to More Deaths than Leukemia". Fortune. Retrieved 14 February 2019.
Gurney JG, Smith MA, Bunin GR. "CNS and Miscellaneous Intracranial and Intraspinal Neoplasms" (PDF). SEER Pediatric Monograph. National Cancer Institute. pp. 51–57. Archived (PDF) from the original on 17 December 2008. Retrieved 4 December 2008. In the US, approximately 2,200 children and adolescents younger than 20 years of age are diagnosed with malignant central nervous system tumors each year. More than 90 percent of primary CNS malignancies in children are located within the brain.
Rood BR. "Infantile Brain Tumors". The Childhood Brain Tumor Foundation. Archived from the original on 11 November 2012. Retrieved 23 July 2014.
Echevarría ME, Fangusaro J, Goldman S (June 2008). "Pediatric central nervous system germ cell tumors: a review". Oncologist. 13 (6): 690–99. doi:10.1634/theoncologist.2008-0037. PMID 18586924.
"About childhood brain tumours". Archived from the original on 7 August 2016. Retrieved 16 June 2016.
Bloch, O (2015). Immunotherapy for malignant gliomas. Cancer Treatment and Research. 163. pp. 143–58. doi:10.1007/978-3-319-12048-5_9. ISBN 978-3-319-12047-8. PMID 25468230.
Auer R, Bell JC (January 2012). "Oncolytic viruses: smart therapeutics for smart cancers". Future Oncology. 8 (1): 1–4. doi:10.2217/fon.11.134. PMID 22149027.
Garber K (1 March 2006). "China Approves World's First Oncolytic Virus Therapy For Cancer Treatment". J Natl Cancer Inst. 98 (5): 298–300. doi:10.1093/jnci/djj111. PMID 16507823. Archived from the original on 10 June 2013.
Logg CR, Tai CK, Logg A, Anderson WF, Kasahara N (20 May 2001). "A uniquely stable replication-competent retrovirus vector achieves efficient gene delivery in vitro and in solid tumors". Human Gene Therapy. 12 (8): 921–32. doi:10.1089/104303401750195881. PMID 11387057.
Tai CK, Wang WJ, Chen TC, Kasahara N (November 2005). "Single-shot, multicycle suicide gene therapy by replication-competent retrovirus vectors achieves long-term survival benefit in experimental glioma". Molecular Therapy. 12 (5): 842–51. doi:10.1016/j.ymthe.2005.03.017. PMID 16257382. Archived from the original on 12 September 2010.
"A Study of a Retroviral Replicating Vector Administered to Subjects With Recurrent Malignant Glioma". Clinical Trials.gov. July 2014. Archived from the original on 26 November 2011.
Tara Palmer-Tomkinson reveals brain tumour battle Archived 9 February 2017 at the Wayback Machine BBC News 19 November 2016
UAE patient’s brain tumour removed through nostrils Archived 6 December 2016 at the Wayback Machine Gulf News, 9 December 2016 |