卵巢癌是一种在卵巢内或卵巢上形成的癌症。[4] [9]它导致异常细胞有能力侵入或扩散到身体的其他部位。[10]当这个过程开始时,可​​能没有或只有模糊的症状。[1]随着癌症的发展,症状变得更加明显。[1] [11]这些症状可能包括腹胀,骨盆疼痛,腹部肿胀和食欲不振等。[1]癌症可能传播的常见区域包括腹部衬里,淋巴结,肺和肝脏。[12]
在一生中排卵更多的女性患卵巢癌的风险增加。这包括那些从未生过孩子的人,那些在较小年龄开始排卵的人和那些在较大年龄就达到更年期的人。[3]其他风险因素包括绝经后激素治疗,生育药物治疗和肥胖。[4] [5]降低风险的因素包括激素分娩控制,输卵管结扎和母乳喂养。[5]大约10%的病例与遗传性遗传风险有关; BRCA1或BRCA2基因突变的女性有50%的几率患上这种疾病。[3]卵巢癌是最常见的卵巢癌类型,占95%以上。[3]卵巢癌有五种主要亚型,其中以高级别浆液性癌(HGSC)最为常见。[3]据信这些肿瘤始于覆盖卵巢的细胞[3],尽管有些可能在输卵管中形成[13]。不常见的卵巢癌类型包括生殖细胞肿瘤和性索间质肿瘤。[3]通过组织活检确认卵巢癌的诊断,通常在手术过程中切除[1]。
对于平均风险的女性,不建议进行筛查,因为证据不支持减少死亡,并且高误报率可能导致不必要的手术,伴随着自身的风险。[14]那些风险很高的人可能会将卵巢切除作为预防措施。[4]如果在早期接受和治疗,卵巢癌通常是可以治愈的。[1]治疗通常包括手术,放射治疗和化疗的某些组合。[1]结果取决于疾病的程度,存在的癌症亚型和其他疾病。[15] [3]美国的整体五年生存率为45%。[6]发展中国家的结果更糟。[3]
2012年,大约239,000名妇女发生了新病例。[3] 2015年,它出现在120万名妇女中,导致全世界有161,100人死亡。[8] [7]在女性中,它是第七大常见癌症,也是癌症死亡的第八大常见原因。[3]典型的诊断年龄是63岁。[2]卵巢癌死亡在北美和欧洲比在非洲和亚洲更常见。[3]
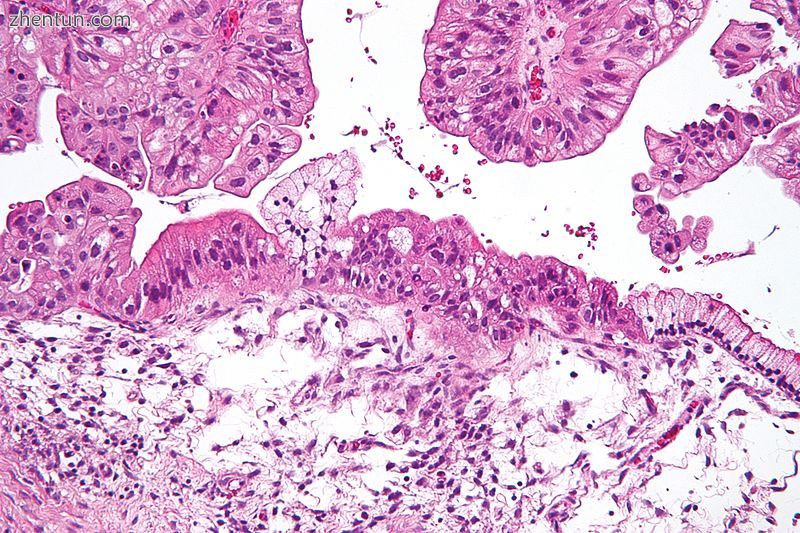
由H&E染色的粘液性卵巢癌的显微照片。
目录
1 症状和体征
1.1 早期症状
1.2 后期症状
1.3 儿童
2 风险因素
2.1 激素
2.2 遗传学
2.3 环境因素
2.4 其他
2.5 保护因素
3 病理生理学
4 诊断
4.1 检验
4.2 病理学
4.3 分期
5 筛选
6 防治
7 管理
7.1 手术
7.2 化疗
7.3 放射治疗
7.4 激素疗法
7.5 免疫治疗
7.6 随访
7.7 姑息治疗
7.8 社会心理护理
8 预后
8.1 预后因素
8.2 生存率
8.3 复发率
9 流行病学
9.1 美国
9.2 英国
9.3 种族
9.4 老年妇女
10 在怀孕期间
11 其他动物
12 研究
12.1 筛选
12.2 预后研究
12.3 免疫治疗
12.4 药
12.5 激素和辐射
12.6 炎症
12.7 临床试验
13 参考资料
体征和症状
早期症状
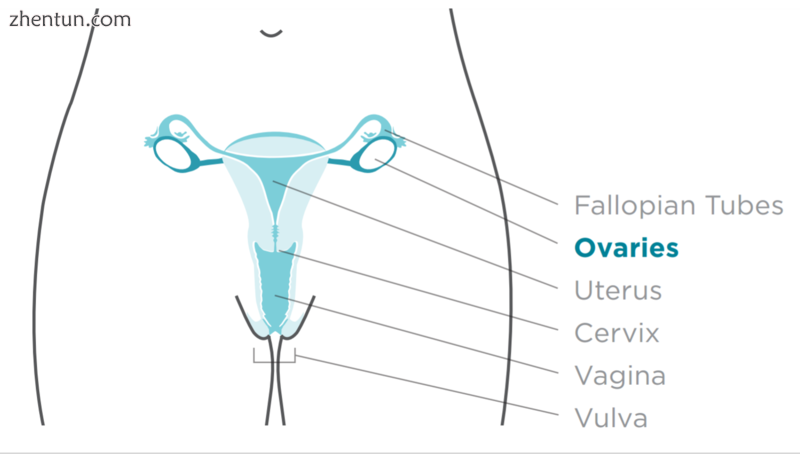
卵巢癌的部位
卵巢癌的早期症状和体征可能不存在或微妙。在大多数情况下,症状在被识别和诊断之前存在几个月。[16] [17]症状可能被误诊为肠易激综合征[18]。卵巢癌的早期阶段往往是无痛的。症状可能因子类型而异。[16]低恶性潜能(LMP)肿瘤,也称为交界性肿瘤,不会引起CA125水平的增加,并且不能用超声波识别。 LMP肿瘤的典型症状可包括腹胀或骨盆疼痛。特别大的群众往往是良性或边缘。[19] [16]
卵巢癌最典型的症状包括腹胀,腹部或盆腔疼痛或不适,背痛,月经不调或绝经后阴道出血,性交后或性交时疼痛或出血,食欲不振,疲劳,腹泻,消化不良,胃灼热,便秘,恶心,感觉饱满,可能还有泌尿系统症状(包括尿频和尿急)。[17]
后来症状
如果卵巢扭转发展,肿块的增加可能会引起疼痛。症状可能是由于对其他腹部器官或转移瘤的大量按压引起的。[16] [20] [21]如果这些症状比平时更常发生或更严重,特别是在没有这些症状的明显病史后,就会考虑卵巢癌[16] [19]。转移可能导致玛丽约瑟夫姐妹的结节。[21]很少,畸胎瘤可引起畸胎瘤综合征或腹膜胶质瘤病。[21]在大多数情况下,有些人在绝经后会出现子宫出血和阴道异常出血。其他常见症状包括多毛症,腹痛,男性化和附件包块。[22]
孩子
在患有卵巢肿瘤的青少年或儿童中,症状可能包括严重的腹痛,腹膜刺激或出血。[23]性索间质肿瘤的症状产生的激素可以影响第二性征的发展。青春期前儿童的性索间质肿瘤可能表现为青春期早期;腹痛和腹胀也很常见。患有性索间质肿瘤的青少年可能会出现闭经。随着癌症变得更加先进,它可以导致腹部积液。如果恶性肿瘤在引起腹水时尚未确诊,则通常在此后不久就会被诊断出来。[16]晚期癌症也可引起腹部肿块,淋巴结肿块或胸腔积液。[21]
风险因素
卵巢癌与排卵时间有关。因此,没有孩子是卵巢癌的风险因素,可能是因为通过怀孕抑制了排卵。在排卵期间,不断刺激细胞分裂,同时排卵周期继续。因此,没有孩子的人患卵巢癌的风险是那些患卵巢癌的人的两倍。早期第一次月经和绝经晚期引起的较长时间的排卵也是一个危险因素。[19] [24] [25]肥胖和激素替代疗法也会增加风险。[16]
对于月经周期较少,没有月经周期,母乳喂养,服用口服避孕药,多胎妊娠以及早年怀孕的女性,患卵巢癌的风险较小。输卵管结扎的妇女(俗称有一个“管系”),卵巢切除或子宫切除术(子宫切除术,有时宫颈切除术)的妇女患卵巢癌的风险降低。 [17]年龄也是一个风险因素。[16] [15]
激素
使用生育药物可能会导致卵巢肿瘤形成,但两者之间的联系是有争议的,难以研究。[18]生育药物可能与临界肿瘤的风险较高有关。[21]那些接受过不育治疗但仍未生育的人患上皮性卵巢癌的风险更高;然而,那些成功接受不孕症治疗并随后分娩的患者风险并不高。这可能是由于怀孕期间癌前细胞脱落,但原因尚不清楚。[19]风险因素可能是不育症本身,而不是治疗。[24]
激素状况如多囊卵巢综合征和子宫内膜异位症与卵巢癌有关,但这种联系并未得到完全证实。[18]绝经后激素替代疗法(HRT)与雌激素可能会增加卵巢癌的风险。该协会尚未在大规模研究中得到证实[19] [26],但包括百万妇女研究在内的着名研究已经支持这一联系。如果使用超过5年,绝经后HRT与雌激素和黄体酮合用可能会增加同期风险,但这种风险在停止治疗后会恢复正常[24]。含有或不含孕激素的雌激素HRT会增加子宫内膜样和浆液性肿瘤的风险,但会降低粘液性肿瘤的风险。更高剂量的雌激素会增加这种风险。[21]子宫内膜异位症是卵巢癌的另一个危险因素[24],月经疼痛也是如此。子宫内膜异位症与透明细胞和子宫内膜样亚型,低度浆液性肿瘤,I期和II期肿瘤,1级肿瘤和较低的死亡率相关[21]。
绝经前,肥胖会增加一个人患卵巢癌的风险,但绝经后这种风险并不存在。 这种风险也与那些既肥胖又从未使用过HRT的人有关。 与卵巢癌类似的关联出现在较高的人群中[24]。
遗传学
进一步的信息:遗传性乳腺癌 - 卵巢癌综合征
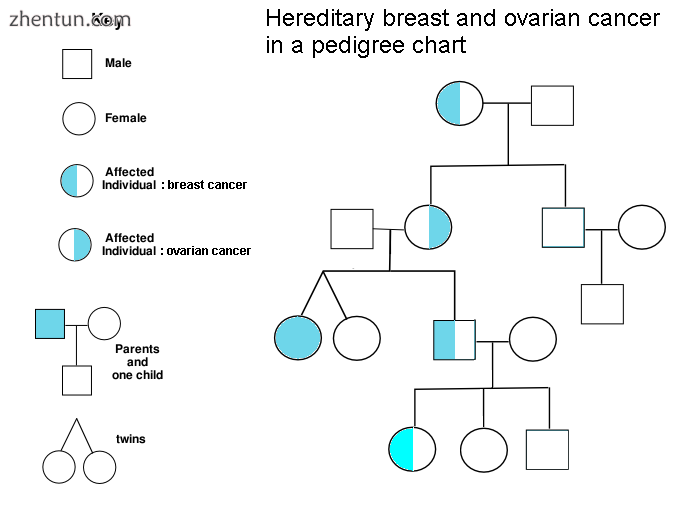
患有卵巢癌或乳腺癌的人在一个家庭的血统图表中
卵巢癌的家族史是卵巢癌的危险因素。患有遗传性非息肉病性结肠癌(Lynch综合征)的人以及患有BRCA-1和BRCA-2遗传异常的人的风险增加。
卵巢癌的主要遗传风险因素是BRCA1或BRCA2 DNA错配修复基因的突变,其存在于10%的卵巢癌病例中。只有一个等位基因需要进行突变才能使人处于高风险状态。该基因可以通过母系或父系遗传,但具有可变的外显率。[16] [19]虽然这些基因的突变通常与乳腺癌风险增加有关,但它们也会导致卵巢癌的终生风险,这种风险在40岁和50岁时达到高峰。引用的最低风险是30%,最高的是60%。[18] [16] [19] BRCA1突变导致卵巢癌的终生风险为15-45%[21]。 BRCA2的突变风险低于BRCA1,终身风险为10%(引用风险最低)至40%(引用风险最高)。[16] [21]平均而言,BRCA相关癌症在它们的散发对应物之前15年发展,因为在其基因的一个拷贝上遗传突变的人只需要一个突变来开始致癌过程,而具有两个正常基因的人需要获得两个突变[19]
在美国,100名患有卵巢癌的一级亲属的女性中有5名最终会患上卵巢癌,将受影响家庭成员的女性置于患有未受影响家庭成员的女性的三倍风险中。 100名患有卵巢癌的两位或更多亲属的女性中有7位最终会患上卵巢癌。[19] [27]一般来说,5-10%的卵巢癌病例有遗传原因。[19] BRCA突变与高级别浆液性非粘液性上皮性卵巢癌有关[21]。
子宫内膜癌,结肠癌或其他胃肠道癌症的强烈家族史可能表明存在一种称为遗传性非息肉病性结肠直肠癌(也称为Lynch综合征)的综合征,这种综合征会导致发生多种癌症的风险增加,包括卵巢癌癌症。 Lynch综合征是由错配修复基因的突变引起的,包括MSH2,MLH1,MLH6,PMS1和PMS2。[16] Lynch综合征患者患卵巢癌的风险在10%至12%之间[16] [19]。冰岛血统,欧洲犹太血统/德系犹太人血统和匈牙利血统的人患上皮性卵巢癌的风险较高。[19]雌激素受体β基因(ESR2)似乎是发病机制和治疗反应的关键。[28]其他与卵巢癌相关的基因是BRIP1,MSH6,RAD51C和RAD51D。[29] CDH1,CHEK2,PALB2和RAD50也与卵巢癌有关。[30]
几种罕见的遗传性疾病与卵巢癌的特定亚型有关。 Peutz-Jeghers综合征是一种罕见的遗传性疾病,也使人易患有环状小管的性索肿瘤。[18] [16] Ollier病和Maffucci综合征与儿童颗粒细胞瘤有关,也可能与Sertoli-Leydig肿瘤有关。良性纤维瘤与痣样基底细胞癌综合征有关[16]。
环境因素
除日本外,工业化国家的上皮性卵巢癌发病率很高,这可能与这些国家的饮食有关。与黑人和西班牙裔人相比,白种人患卵巢癌的风险高30-40%,可能是由于社会经济因素造成的;白人妇女往往有更少的孩子和不同的妇科手术率,影响卵巢癌的风险。[19]
队列研究发现乳制品消费与卵巢癌之间存在相关性,但病例对照研究未显示出这种相关性。有关红肉和加工肉类对卵巢癌的影响的综合证据。[21]
初步证据表明,滑石粉,杀虫剂和除草剂会增加患卵巢癌的风险。[31]美国癌症协会指出,截至目前,没有研究能够将环境或人类饮食中的任何单一化学物质直接与导致卵巢癌的突变直接联系起来。[32]
其他
酒精消费似乎与卵巢癌没有关系。[21] [33]已经调查过的其他因素,如吸烟,血液中维生素D水平低,[34]包含卵巢囊肿和人乳头瘤病毒感染(某些宫颈癌病例的原因),已被证实为卵巢癌的危险因素[18] [21]会阴滑石的致癌性是有争议的,因为它可以作为一种刺激物,如果它通过生殖道进入卵巢。[21] [19] [24]病例对照研究表明,使用会阴滑石确实会增加患卵巢癌的风险,但使用滑石通常不会产生更大的风险。[21]在身体其他部位使用滑石与卵巢癌无关。[24]长期定期坐位与上皮性卵巢癌的死亡率较高有关。虽然降低了风险,但定期运动并没有否定风险。[35]
年龄增加(直至70岁)是上皮性卵巢癌的危险因素,因为细胞中的更多突变可以累积并最终导致癌症。那些80岁以上的人的风险略低。[19]
吸烟有助于增加粘液性卵巢癌的风险;戒烟后,风险最终恢复正常。富含动物脂肪的饮食可能与卵巢癌有关,但关系尚不清楚。如果有的话,饮食似乎在卵巢癌风险中扮演一个非常小的角色。[24]较高水平的C反应蛋白与发生卵巢癌的风险较高有关。[21]
保护因素
抑制排卵,否则会导致卵巢上皮损伤,从而导致炎症,通常是保护性的。这种效果可以通过让孩子服用复方口服避孕药和母乳喂养来实现,所有这些都是保护因素。[16]较长时间的母乳喂养与卵巢癌风险的较大降低相关。[24]每次分娩都会降低患卵巢癌的风险,这种影响最多可见于5个分娩。联合口服避孕药可将卵巢癌的风险降低多达50%,联合口服避孕药的保护作用可在停药后持续25 - 30年。[19] [24]经常使用阿司匹林或对乙酰氨基酚(扑热息痛)可能会降低患卵巢癌的风险;其他NSAID似乎没有类似的保护作用。[21]
输卵管结扎具有保护作用,因为致癌物质无法通过阴道,子宫和输卵管到达卵巢和菌毛。[16]输卵管结扎对BRCA1突变的女性也具有保护作用,但对BRCA2突变没有保护作用。[21]子宫切除术降低了风险,并且移除输卵管和卵巢(双侧输卵管卵巢切除术)不仅可以显着降低患卵巢癌的风险,还可以降低患乳腺癌的风险。[18]这仍然是一个研究课题,因为子宫切除术和降低卵巢癌风险之间的联系是有争议的。到2015年,子宫切除术可能具有保护作用的原因尚未阐明。[24]
含有大量胡萝卜素,纤维和维生素以及少量脂肪的饮食 - 特别是非淀粉类蔬菜(例如西兰花和洋葱)的饮食 - 可能具有保护作用,[19]尽管该领域仍在进行研究[24]每天摄入更多的咖啡因和摄入超过两杯茶都会降低卵巢癌的风险。[21]吸烟烟草对性索间质肿瘤具有保护作用。[22]
病理生理学
当正常卵巢细胞生长发生错误时,就会形成卵巢癌。通常,当细胞变老或受损时,它们会死亡,新的细胞会取而代之。当新细胞形成不需要时,癌症开始,旧的或受损的细胞不会死亡。额外细胞的累积通常形成称为生长或肿瘤的大量组织。这些异常的癌细胞有许多遗传异常导致它们过度生长。[37]当卵巢释放卵子时,卵泡破裂并变成黄体。这种结构需要通过分裂卵巢中的细胞进行修复。[24]连续排卵很长一段时间意味着通过分裂细胞来修复卵巢,这可以在每个分裂中获得突变。[19]
总体而言,卵巢癌中最常见的基因突变发生在NF1,BRCA1,BRCA2和CDK12中。 I型卵巢癌往往攻击性较低,往往在几种基因中具有微卫星不稳定性,包括致癌基因(最明显的是BRAF和KRAS)和肿瘤抑制因子(最显着的是PTEN)。[18] I型癌症中最常见的突变是KRAS,BRAF,ERBB2,PTEN,PIK3CA和ARID1A。[21] II型癌症,更具攻击性的类型,具有突变的不同基因,包括p53,BRCA1和BRCA2。[18]低级别癌症倾向于在KRAS中发生突变,而从低恶性潜在肿瘤发展的任何级别的癌症都倾向于在p53中发生突变。[19] I型癌症倾向于从前驱病变发展,而II型癌症可从浆液性输卵管上皮内癌发展[21]。具有BRCA突变的浆液性癌症也不可避免地具有p53突变,表明两种功能基因的去除对于癌症发展是重要的。[19]
在50%的高级别浆液性癌症中,同源重组DNA修复功能失调,缺口和FOXM1信号通路也是如此。他们几乎总是有p53突变。除此之外,高级浆液性癌的突变很难表征超出其高度的基因组不稳定性。 BRCA1和BRCA2对于同源重组DNA修复至关重要,这些基因中的种系突变在约15%的卵巢癌患者中发现[18]。 BRCA1和BRCA2中最常见的突变是起源于Ashkenazi犹太人的小型创始人群的移码突变。[19]
几乎100%的罕见粘液性癌都有KRAS突变和ERBB2扩增(也称为Her2 / neu)。[18]总体而言,20%的卵巢癌在Her2 / neu中有突变[16]。
浆液性癌可能从浆液性输卵管上皮内癌发展而不是从卵巢组织自发发展。其他癌由皮质包涵囊肿发展而来,这些囊肿是基质内的上皮卵巢细胞群。[19]
诊断
检查
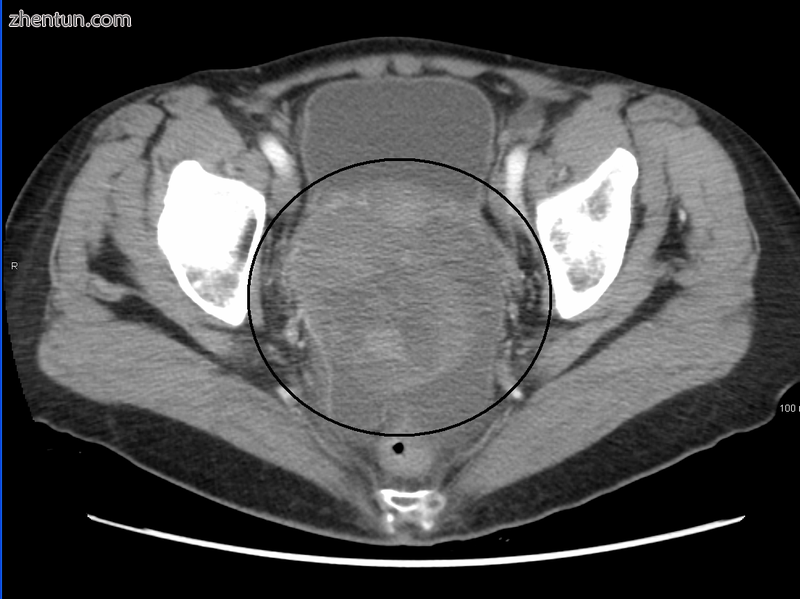
在CT上看到的非常大的卵巢癌
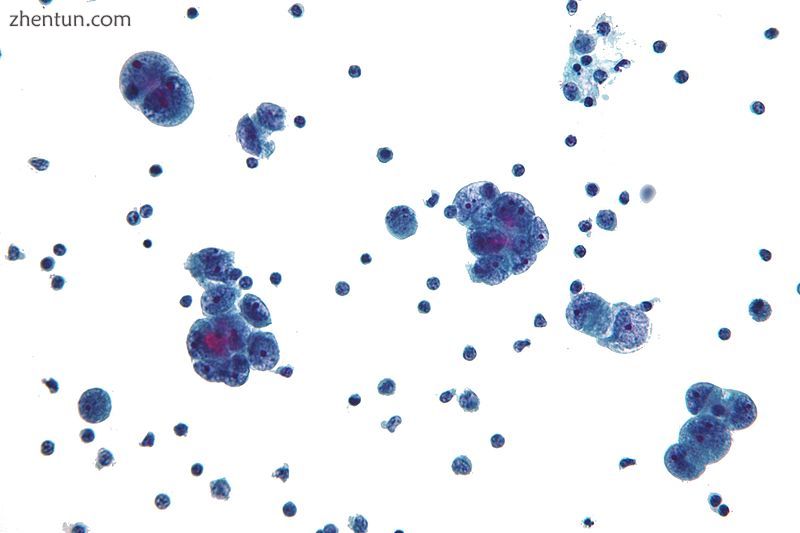
浆液性癌的显微照片,一种卵巢癌,在腹膜液中诊断
卵巢癌的诊断始于体格检查(包括盆腔检查),血液检查(CA-125和其他标记),以及经阴道超声[16]。有时直肠阴道检查用于帮助计划手术。[19]必须通过手术确认诊断以检查腹腔,进行活组织检查(用于显微镜分析的组织样本),并在腹腔液中寻找癌细胞。这有助于确定卵巢肿块是良性还是恶性。[16]
卵巢癌的早期阶段(I / II)难以诊断,因为大多数症状是非特异性的,因此在诊断中几乎没有用;因此,它很少被诊断出来,直到它传播并进入后期阶段(III / IV)。[38]此外,卵巢癌的症状可能与肠易激综合征相似。在可能怀孕的患者中,可以在诊断过程中测量BHCG水平。血清甲胎蛋白,神经元特异性烯醇化酶和乳酸脱氢酶可以在怀疑卵巢肿瘤的年轻女孩和青少年中测量,因为年轻患者更可能患有恶性生殖细胞肿瘤。[16] [21]
体检,包括盆腔检查和盆腔超声(经阴道或其他)都是诊断必不可少的:体格检查可能显示腹围和/或腹水增加(腹腔内液体),而盆腔检查可能显示卵巢或腹部肿块。[18]附件包块是一个重要的发现,通常表明卵巢癌,特别是如果它是固定的,结节的,不规则的,实心的和/或双侧的。 13-21%的附件包块是由恶性肿瘤引起的;然而,附件包块还有其他良性病因,包括卵巢滤泡囊肿,平滑肌瘤,子宫内膜异位症,异位妊娠,输卵管积水,输卵管脓肿,卵巢扭转,皮样囊肿,囊腺瘤(浆液性或粘液性),憩室或阑尾脓肿,神经鞘瘤,盆腔肾,输尿管或膀胱憩室,腹膜良性囊性间皮瘤,腹膜结核或卵巢囊肿。可以感觉到的卵巢也是绝经后妇女卵巢癌的征兆。怀疑卵巢癌的身体检查的其他部分可包括乳房检查和直肠指检。触诊锁骨上,腋窝和腹股沟淋巴结可能会发现淋巴结肿大,这可能是转移的指征。另一个指标可能是胸腔积液的存在,可以在听诊时注意到。[21]
当卵巢恶性肿瘤包括在诊断可能性列表中时,指示了有限数量的实验室测试。通常可以获得全血细胞计数和血清电解质测试; [39]当存在卵巢癌时,这些测试通常显示大量血小板(20-25%的人)和由于化学信号分泌的低血钠水平。肿瘤。[19]抑制素A和抑制素B的阳性检测可以指示颗粒细胞瘤。[21]
一种名为CA-125的标记物分子的血液检测可用于鉴别诊断和疾病的随访,但它本身并未被证明是筛查早期卵巢癌的有效方法,因为其不可接受的低敏感性和特异性。[39]超过200 U / mL的绝经前人群的CA-125水平可能表明卵巢癌,绝经后人群中CA-125的任何升高可能超过35 U / mL。 CA-125水平在早期卵巢癌中不准确,因为完全一半的I期卵巢癌患者具有正常的CA-125水平。[21] [19] CA-125也可能在良性(非癌)条件下升高,包括子宫内膜异位症,妊娠,子宫肌瘤,月经,卵巢囊肿,系统性红斑狼疮,肝脏疾病,炎症性肠病,盆腔炎性疾病和平滑肌瘤[21]。 [40] HE4是卵巢癌检测的另一个候选药物,但尚未经过广泛测试。卵巢癌的其他肿瘤标志物包括CA19-9,CA72-4,CA15-3,免疫抑制酸性蛋白,触珠蛋白-α,OVX1,间皮素,溶血磷脂酸,骨桥蛋白和成纤维细胞生长因子23 [21]。
使用血液检查板可能有助于诊断。[21] [39] OVA1组包括CA-125,β-2微球蛋白,转铁蛋白,载脂蛋白A1和转甲状腺素蛋白。 OVA1在绝经前人群中高于5.0,在绝经后人群中为4.4,表明患癌症的风险很高[19]。一组不同的实验室测试用于检测性索间质肿瘤。高水平的睾酮或脱氢表雄酮硫酸盐,结合其他症状和高水平的抑制素A和抑制素B可以指示任何类型的SCST。[22]
目前的研究正在寻找将肿瘤标志物蛋白质组学与其他疾病指标(即放射学和/或症状)相结合的方法,以提高诊断的准确性。这种方法的挑战在于,卵巢癌的不同患病率意味着即使以非常高的敏感性和特异性进行检测仍会导致许多假阳性结果,这反过来可能导致诸如进行癌症的外科手术等问题。术中未发现。[引证需要]尚未开发出用于卵巢癌的基因组学方法。[21]
虽然也可以使用磁共振成像,但首选CT扫描来评估腹腔内腔内肿瘤的范围。[18] CT扫描还可用于发现网膜结块或区分腹部实体肿瘤的液体,特别是在低恶性潜在肿瘤中。然而,它可能无法检测到较小的肿瘤。有时,胸部X光检查用于检测胸腔或胸腔积液中的转移灶。对于转移性疾病的另一项测试,虽然很少使用,但是钡灌肠,可以显示直肠乙状结肠是否与疾病有关。正电子发射断层扫描,骨扫描和腹腔穿刺的用途有限;事实上,腹腔穿刺术可能会在针插入部位形成转移,并且可能无法提供有用的结果。[19]然而,腹腔穿刺术可用于没有盆腔肿块且腹水仍然存在的情况。[19]怀疑卵巢癌的医生也可以进行乳房X光检查或子宫内膜活检(在异常出血的情况下)以分别评估乳腺恶性肿瘤和子宫内膜恶性肿瘤的可能性。阴道超声检查通常是在发现附件肿块时进行的一线成像研究。附件包块的几个特征表明卵巢恶性肿瘤;它们通常是实心的,不规则的,多房的和/或大的;它们通常具有乳头状特征,中央血管和/或不规则的内部隔膜。[21]然而,SCST在射线照相研究中没有明确的特征。[22]
为了明确诊断卵巢癌,需要进行检查腹部的外科手术。这可以是开放手术(剖腹手术,通过腹壁切开)或锁孔手术(腹腔镜检查)。在此过程中,移除可疑组织并送去进行显微镜分析。通常,这包括单侧输卵管卵巢切除术,切除单个受影响的卵巢和输卵管。还可以分析来自腹腔的流体的癌细胞。如果发现癌症,该程序也可用于确定其扩散程度(这是肿瘤分期的一种形式)。[16]
风险评分
一种广泛认可的估计恶性卵巢癌风险的方法是恶性指数(RMI)的风险,根据初步检查计算[18] [41]。一般认为RMI评分超过200或250表明卵巢癌的高风险[18] [21]。
RMI计算如下:
RMI =超声评分×绝经评分x CA-125水平,单位为U / ml。[18]
可以使用两种方法来确定超声分数和绝经期分数,所得分数分别被称为RMI 1和RMI 2,这取决于使用何种方法。
量化卵巢癌风险的另一种方法是卵巢癌风险算法(ROCA),随时间观察水平并确定它们是否正在迅速增加以保证经阴道超声。[19]卵巢恶性肿瘤风险算法使用CA-125水平和HE4水平来计算卵巢癌的风险;它可能比RMI更有效。 IOTA模型可用于估计附件肿瘤是恶性的概率。[43]它们包括LR2风险模型,简单规则风险(SRrisk)计算和Adnexa中不同瘤形成的评估(ADNEX)模型,可用于根据其特征和风险因素评估附件肿块中恶性肿瘤的风险。 QCancer(卵巢)算法用于从风险因素预测卵巢癌的可能性。[21]
病理
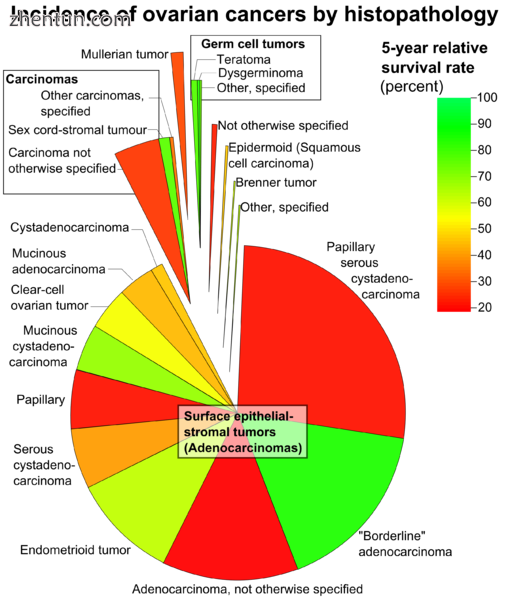
20岁以上女性的卵巢癌,面积代表相对发病率,颜色代表五年相对存活率[44]
卵巢癌根据其结构的微观外观(组织学或组织病理学)进行分类。 组织学决定临床治疗,管理和预后的许多方面。 无论组织学类型如何,卵巢癌的总体病理学非常相似:肿瘤具有实性和囊性肿块[19]。 根据SEER,20岁及以上女性的卵巢癌类型是:[44]
卵巢癌在组织学和遗传上分为I型或II型。 I型癌症具有低组织学分级,包括子宫内膜样,粘液性和透明细胞癌。 II型癌症的组织学分级较高,包括浆液性癌和癌肉瘤[18]。
上皮癌
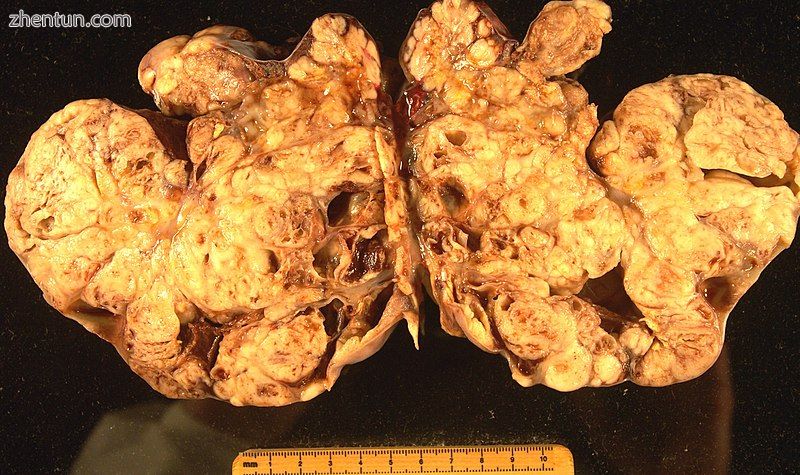
卵巢癌的病理标本
表面上皮 - 间质肿瘤,也称为卵巢上皮癌,是最常见的卵巢癌类型,占大约90%的卵巢癌。它包括浆液性肿瘤,子宫内膜样肿瘤和粘液性囊腺癌。较少见的肿瘤是恶性Brenner肿瘤和卵巢的移行细胞癌。上皮卵巢癌是从上皮细胞发育而来的,上皮是覆盖卵巢的一层细胞。[45]
浆液性癌
大多数患有上皮性卵巢癌的人,约三分之二,患有浆液性癌,[18]尽管这一比例估计高达80%[21] [46]。低级别浆液性癌的侵袭性低于高级别浆液性癌,但通常对化疗或激素治疗无效。[18]浆液性癌被认为是在输卵管中开始的。[45]组织学上,浆液性腺癌具有沙门氏体。低级别浆液性腺癌类似于输卵管上皮,而高级别浆液性腺癌则表现为异常和核异型。[19]
50%的时间,浆液性癌是双侧的,85%的病例在诊断时已经扩散到卵巢以外。大多数人的直径超过15厘米。[46]
小细胞癌
小细胞卵巢癌是罕见的和侵袭性的,有两种主要的亚型:高钙血症和肺癌。它通常在诊断后2年内致命。高钙血症小细胞卵巢癌绝大多数影响20多岁的人,导致高血钙水平,并影响一个卵巢。肺小细胞卵巢癌通常影响老年妇女的卵巢,看起来像肺部的燕麦细胞癌。[19]
原发性腹膜癌
主要文章:原发性腹膜癌
原发性腹膜癌由腹膜发展而来,腹膜是覆盖腹腔的膜,其具有与卵巢相同的胚胎起源。 当它们影响卵巢时,它们经常被讨论并归类为卵巢癌。[45] [47] 它们甚至可以在卵巢移除后发育,并且可能与间皮瘤相似。[19]
透明细胞癌
透明细胞卵巢癌通常对化疗反应不佳,可能与子宫内膜异位症有关[18]。 它们占所有子宫内膜癌的约5%。 日本女性比其他女性更容易患上透明细胞卵巢癌。[21]
透明细胞腺癌
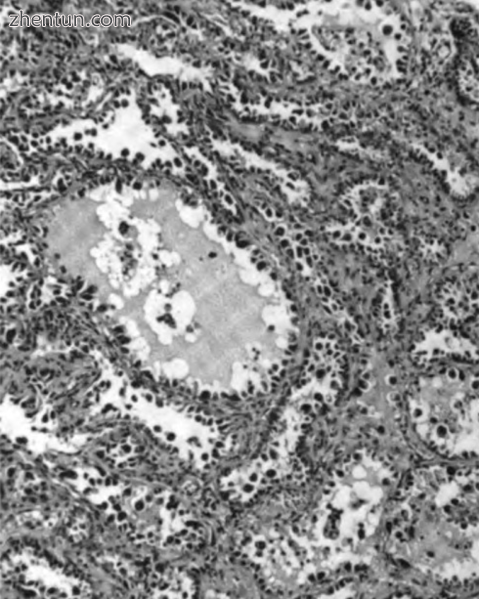
在透明细胞癌样品中看到的脱落细胞
透明细胞腺癌在组织病理学上与其他透明细胞癌类似,具有透明细胞和甲状腺细胞。它们代表约5-10%的上皮卵巢癌并且与盆腔中的子宫内膜异位症相关。它们通常是早期阶段,因此可通过手术治愈,但晚期透明细胞腺癌(约20%)的预后较差,并且通常对铂类化疗有抵抗作用。[19]
子宫内膜样腺癌
子宫内膜样腺癌占上皮性卵巢癌的约15-20%。因为它们通常是低级别的,所以子宫内膜样腺癌具有良好的预后。这些肿瘤经常与子宫内膜异位症或子宫内膜癌共同发生[19]。
恶性混合性苗勒肿瘤(carcinosarcoma)
混合的苗勒氏肿瘤占卵巢癌的不到1%。它们可见上皮细胞和间充质细胞,预后较差。[19]
粘液
粘液性肿瘤包括粘液腺癌和粘液性囊腺癌。[19]
粘液腺癌
主要文章:粘液腺癌
粘液腺癌占上皮性卵巢癌的5-10%。在组织学上,它们类似于肠或宫颈腺癌,并且通常实际上是阑尾癌或结肠癌的转移。晚期粘液性腺癌的预后较差,一般比浆液性肿瘤更差,并且往往对铂类化疗耐药,尽管它们很少见[19]。
腹膜假性粘液瘤
主要文章:腹膜假性粘液瘤
腹膜假性粘液瘤是指腹腔内腔中包裹的粘液或凝胶状物质的集合,其很少由原发性粘液性卵巢肿瘤引起。更常见的是,它与肠癌的卵巢转移有关。[19]
未分化的上皮细胞
未分化的癌症 - 无法确定细胞类型的癌症 - 占上皮性卵巢癌的10%左右,并且预后相对较差。[19] [45]当在显微镜下检查时,这些肿瘤具有非常异常的细胞,这些细胞排列成团块或片状。通常肿瘤内有可识别的浆液性细胞团。[19]
恶性Brenner肿瘤
主要文章:Brenner肿瘤
恶性Brenner肿瘤很少见。在组织学上,它们具有致密的纤维基质,具有过渡上皮区域和一些鳞状分化。为了被归类为恶性Brenner肿瘤,它必须具有Brenner肿瘤病灶和移行细胞癌。过渡性细胞癌成分通常分化不良,类似于泌尿道癌。[19]
移行细胞癌
主要文章:移行细胞癌
移行细胞癌占卵巢癌的不到5%。在组织学上,它们看起来与膀胱癌相似。预后是中等的 - 比大多数上皮癌更好,但比恶性Brenner肿瘤更差。[19]
性索间质瘤
主要文章:性索间质瘤
性索间质肿瘤,包括产生雌激素的颗粒细胞瘤,良性肿瘤和男性化的Sertoli-Leydig细胞瘤或成神经细胞瘤,占卵巢癌的7%。它们最常见于50至69岁的女性,但可发生在任何年龄的女性,包括年轻女孩。它们通常不具有攻击性,通常是单侧的; [16]因此它们通常仅通过手术治疗。性索间质肿瘤是产生激素的主要卵巢肿瘤。[22]
来自间充质的几种不同细胞可以产生性索或间质肿瘤。这些包括成纤维细胞和内分泌细胞。性索或卵巢间质瘤的症状可能与其他类型的卵巢癌不同。常见症状和体征包括卵巢扭转,肿瘤出血或破裂,腹部肿块和激素破坏。在儿童中,同种性早熟可能与颗粒细胞肿瘤发生,因为它们产生雌激素。这些肿瘤导致月经异常(出血过多,月经不频或无月经)或绝经后出血。因为这些肿瘤产生雌激素,它们可以在子宫内膜癌或乳腺癌的同时引起或发生。其他性索/间质肿瘤表现出明显的症状。 Sertoli-Leydig细胞肿瘤由于睾酮和雄烯二酮的产生而导致男性化和过度毛发生长,这在极少数情况下也会引起库欣综合征。此外,性索间质肿瘤不会引起激素失衡,包括引起腹水和胸腔积液的良性纤维瘤。[16]对于生殖细胞肿瘤,性索 - 间质肿瘤是20岁以下女性最常见的卵巢癌。[22]
颗粒细胞瘤
颗粒细胞瘤是最常见的性索间质肿瘤,占病例的70%,分为两种组织学亚型:50岁以上女性发育成人颗粒细胞肿瘤,青春期前发育的幼年型颗粒肿瘤或在30岁之前,两者都是从围绕生殖细胞的细胞群中发育出来的。[22]
成人颗粒细胞瘤
成人颗粒细胞肿瘤的特征是发病较晚(30年以上,平均50例)。这些肿瘤产生高水平的雌激素,导致其特征性症状:子宫出血;子宫内膜增生;柔软,乳房增大;绝经后出血;和继发性闭经。如果肿瘤出血和破裂,肿瘤的质量可引起其他症状,包括腹痛和腹胀,或类似于异位妊娠的症状。[22]
幼年颗粒细胞瘤
Sertoli-Leydig细胞肿瘤
Sertoli-Leydig肿瘤在30岁以前的女性中最常见,在青春期之前尤为常见[22]。
硬化性间质瘤
硬化性间质瘤通常发生在青春期前的女孩或30岁以前的女性。[22]
生殖细胞肿瘤
主要文章:卵巢生殖细胞肿瘤
卵巢的生殖细胞肿瘤来自卵巢生殖细胞。[45]生殖细胞肿瘤占卵巢肿瘤的约30%,但仅占卵巢癌的5%,因为大多数生殖细胞肿瘤是畸胎瘤,而大多数畸胎瘤是良性的。当肿瘤中的一个胚层发展成鳞状细胞癌时,恶性畸胎瘤往往发生在老年妇女身上。[16]生殖细胞肿瘤往往发生在年轻女性(20s-30s)和女孩中,占该年龄组卵巢癌的70%。[23]当胚胎出现在卵巢中时,生殖细胞肿瘤可包括无性细胞瘤,畸胎瘤,卵黄囊肿瘤/内胚窦瘤和绒毛膜癌。一些生殖细胞肿瘤具有异染色体12,其中12号染色体的一条臂被删除,并被另一条的副本替换。[16]大多数生殖细胞癌的预后比其他亚型更好,对化疗更敏感。他们更有可能在诊断时成为第一阶段。[22]总体而言,它们比上皮性卵巢癌更频繁地转移。此外,使用的癌症标志物随肿瘤类型而变化:绒毛膜癌用β-HCG监测,内胚窦瘤用甲胎蛋白监测[16]。
生殖细胞肿瘤通常在它们变成大的可触及肿块时被发现。然而,像性索肿瘤一样,它们可能导致卵巢扭转或出血,而在儿童中,它们会导致同性恋性早熟。它们经常转移到附近的淋巴结,尤其是主动脉旁和盆腔淋巴结。[16]生殖细胞肿瘤最常见的症状是由肿瘤出血,坏死或拉伸卵巢囊引起的亚急性腹痛。如果肿瘤破裂,引起明显出血或对卵巢进行检查,则可引起急性腹痛,其发生率仅为生殖细胞肿瘤的10%。它们还可以分泌改变月经周期的激素。在25%的生殖细胞肿瘤中,癌症是在常规检查中发现的,不会引起症状。[22]
诊断生殖细胞肿瘤可能很困难,因为正常的月经周期和青春期会导致疼痛和盆腔症状,而年轻女性甚至可能认为这些症状是怀孕的,并且由于青少年怀孕的耻辱而不寻求治疗。甲胎蛋白,核型,人绒毛膜促性腺激素和肝功能的血液检测用于诊断生殖细胞肿瘤和潜在的共存性腺发育不全。生殖细胞肿瘤最初可能被误认为是良性卵巢囊肿。[22]
无性细胞瘤
主要文章:Dysgerminoma
Dysgerminoma占年轻女性卵巢癌的35%,是最有可能转移到淋巴结的生殖细胞肿瘤;淋巴结转移发生在25-30%的病例中[23] [22]。这些肿瘤可能在KIT基因中具有突变,这是一种以其在胃肠道间质瘤中的作用而闻名的突变。具有XY核型和卵巢(性腺发育不全)或X,0核型和卵巢(特纳综合征)的人发展为单侧无性细胞瘤,其他卵巢中有性腺母细胞瘤的风险,在这种情况下,两个卵巢通常都会被切除。发现单侧无性细胞瘤可避免另一种恶性肿瘤的风险。在Swyer或Turner综合征患者中,性腺母细胞瘤在大约40%的病例中变得恶变。然而,一般来说,无性细胞瘤是双侧的10-20%。[16] [22]
它们由不能进一步分化并直接从生殖细胞或性腺母细胞瘤发育的细胞组成。 无性细胞瘤在大约5%的病例中含有合体滋养细胞,因此可以引起hCG水平升高。在整体外观上,无性细胞瘤通常是粉红色到棕褐色,有多个裂片,并且是实心的。在显微镜下,它们看起来与精原细胞瘤相同,并且非常接近胚胎原始生殖细胞,具有大的多面体圆形透明细胞。细胞核均匀,圆形或方形,核仁明显,细胞质中含有高水平的糖原。炎症是无性细胞瘤的另一个突出的组织学特征。[22]
绒毛膜癌
主要文章:绒毛膜癌
绒毛膜癌可以作为从生殖细胞发育的原发性卵巢肿瘤发生,但它通常是转移到卵巢的妊娠疾病。原发性卵巢绒毛膜癌的预后较差,可以在没有怀孕的情况下发生。它们产生高水平的hCG,可导致儿童早期青春期或月经初潮后的月经过多(月经不调,月经不调)。[22]
未成熟(实体)畸胎瘤
主要文章:未成熟的畸胎瘤
未成熟或实性畸胎瘤是最常见的卵巢生殖细胞肿瘤类型,占病例的40-50%。畸胎瘤的特征在于存在来自所有三个胚胎胚层的无组织组织:外胚层,中胚层和内胚层;未成熟的畸胎瘤也有未分化的干细胞,使它们比成熟的畸胎瘤(皮样囊肿)更具恶性。不同的组织在大体病理学上是可见的,并且通常包括骨,软骨,毛发,粘液或皮脂,但是从外面看不到这些组织,这看起来是具有裂片和囊肿的固体块。在组织学上,他们将大量的神经外胚层组织成片状和小管以及神经胶质;神经组织的数量决定了组织学分级。未成熟的畸胎瘤通常仅影响一个卵巢(10%与皮样囊肿共同发生)并且通常在整个腹膜中转移。它们还可以导致成熟的畸胎瘤植入物在称为生长畸胎瘤综合征的疾病中在整个腹部生长;这些通常是良性的,但在化疗期间会继续增长,并且通常需要进一步手术。与成熟畸胎瘤不同,未成熟畸胎瘤形成许多粘连,使其不太可能引起卵巢扭转。未成熟畸胎瘤没有特异性标志物,但癌胚抗原(CEA),CA-125,CA19-9或AFP有时可能表明未成熟的畸胎瘤[22]。
I期畸胎瘤占病例的大多数(75%)且预后最佳,98%的患者存活5年;如果I期肿瘤也是1级,则可以仅用单侧手术治疗。第二阶段虽然IV肿瘤构成了剩余的四分之一的病例并且预后较差,73-88%的患者存活了5年。[22]
成熟畸胎瘤(皮样囊肿)
主要文章:皮样囊肿
成熟的畸胎瘤或皮样囊肿是罕见的肿瘤,主要由绝经后发生的良性组织组成。肿瘤由具有恶性组织结节的紊乱组织组成,其可以是各种类型的。最常见的恶性肿瘤是鳞状细胞癌,但是腺癌,基底细胞癌,类癌,神经外胚层肿瘤,恶性黑素瘤,肉瘤,皮脂腺瘤和卵巢肿瘤也可以是皮样囊肿的一部分。他们接受手术和辅助铂类化疗或放射治疗。[22]
卵黄囊肿瘤/内胚窦瘤
主要文章:卵黄囊肿瘤
卵黄囊肿瘤,以前称为内胚窦瘤,占卵巢生殖细胞恶性肿瘤的约10-20%,并且对所有卵巢生殖细胞肿瘤的预后最差。它们发生在月经初潮前(三分之一的病例)和月经初潮(其余三分之二的病例)。半数患有卵黄囊肿瘤的人在阶段I中被诊断出来。通常,它们是单侧的,直到转移,其发生在腹膜腔内并且通过血流到达肺部。卵黄囊肿瘤生长迅速并且容易复发,一旦复发就不容易治疗。 I期卵黄囊肿瘤是高度可治疗的,5年无病生存率为93%,但II-IV期肿瘤治疗较差,存活率为64-91%。[22]
它们的整体外观是坚实的,易碎的和黄色的,具有坏死和出血区域。它们通常还含有可以退化或破裂的囊肿。组织学上,卵黄囊肿瘤的特征在于存在Schiller-Duval体(其为卵黄囊肿瘤的特征)和网状图案。卵黄囊肿瘤通常分泌甲胎蛋白,并且可以通过免疫组织化学方法对其存在进行染色;血液中的甲胎蛋白水平是复发的有用标志。[22]
胚胎癌
主要文章:胚胎癌
胚胎癌是一种罕见的肿瘤类型,通常在混合肿瘤中发现,直接从生殖细胞发育,但没有终末分化;在极少数情况下,它们可能在发育不良的性腺中发展。它们可以进一步发展成各种其他肿瘤,包括绒毛膜癌,卵黄囊肿瘤和畸胎瘤。它们发生在年轻人身上,平均诊断年龄为14岁,分泌甲胎蛋白(75%的病例)和hCG。[22]
在组织学上,胚胎癌似乎与胚胎盘相似,由上皮,无组织片中的间变细胞组成,具有腺样空间和乳头状结构。[22]
多胚胎瘤
主要文章:多胚胎瘤
多胚胎是最不成熟的畸胎瘤和非常罕见的卵巢肿瘤,其组织学特征在于具有几个类似于胚盘,卵黄囊和羊膜囊的胚胎样体。合胞体滋养细胞巨细胞也存在于多发性骨髓瘤中[22]。
鳞状细胞癌
原发性卵巢鳞状细胞癌罕见,晚期预后不良。更典型地,卵巢鳞状细胞癌是宫颈转移,子宫内膜样肿瘤中的分化区域,或源自成熟畸胎瘤。[19]
混合肿瘤
混合肿瘤含有多于一种上述肿瘤组织学的元素。被归类为混合肿瘤,次要类型必须占肿瘤的10%以上。[21]虽然混合型癌可以有任何细胞类型的组合,但混合卵巢癌通常是浆液性/子宫内膜样癌或透明细胞/子宫内膜样癌。[19]混合生殖细胞肿瘤构成所有生殖细胞卵巢癌的约25-30%,具有无性细胞瘤,卵黄囊肿瘤和/或未成熟畸胎瘤的组合。预后和治疗因成分细胞类型而异。[22]
继发性卵巢癌
卵巢癌也可能是继发性癌症,是身体其他部位原发癌转移的结果。[16]大约7%的卵巢癌是由转移引起的,而其余的则是原发性癌症。[引证需要]常见的原发性癌症是乳腺癌,结肠癌,阑尾癌和胃癌(转移到卵巢的原发性胃癌称为Krukenberg)瘤)。[16] Krukenberg肿瘤有印戒细胞和粘液细胞。[19]子宫内膜癌和淋巴瘤也可以转移到卵巢。[46]
低恶性潜在肿瘤
低恶性潜在卵巢肿瘤,也称为交界性肿瘤,具有一些良性和某些恶性特征。[19] LMP肿瘤占所有卵巢肿瘤的约10%-15%[21] [45]。它们比上皮性卵巢癌早发育,大约40-49岁。他们通常没有广泛的入侵; 10%的LMP肿瘤具有基质微侵袭区域(<3mm,<5%的肿瘤)。 LMP肿瘤具有其他异常特征,包括有丝分裂增加,细胞大小或核大小的变化,细胞核异常,细胞分层和细胞上的小突起(乳头状突起)。在组织学检查中可以看到浆液性和/或粘液性特征,浆液性组织学构成了绝大多数晚期LMP肿瘤。超过80%的LMP肿瘤是I期; 15%是第二阶段和第三阶段,不到5%是第四阶段。[19] LMP肿瘤的植入物通常是非侵入性的。[45]
分期
卵巢癌使用FIGO分期系统进行分期并使用手术后获得的信息,其中包括通过中线剖腹手术进行全腹式子宫切除术,切除(通常)卵巢和输卵管,(通常)网膜,盆腔(腹膜)洗液,评估腹膜后淋巴结(包括盆腔和腹主动脉旁淋巴结),疑似粘液性肿瘤的阑尾切除术和盆腔/腹膜活检的细胞病理学[18] [16] [21] [48]大约30%的卵巢癌似乎局限于卵巢,在显微镜下已经转移,这就是为什么即使是Ⅰ期癌症也必须完全分期。[16]据推测,22%的癌症被认为是第一阶段的淋巴转移。[21] AJCC阶段与FIGO阶段相同。 AJCC分期系统描述了原发肿瘤的程度(T),是否存在或不存在向附近淋巴结转移(N),以及是否存在远处转移(M)。[49]诊断时最常见的阶段是IIIc期,超过70%的诊断。[16]
FIGO
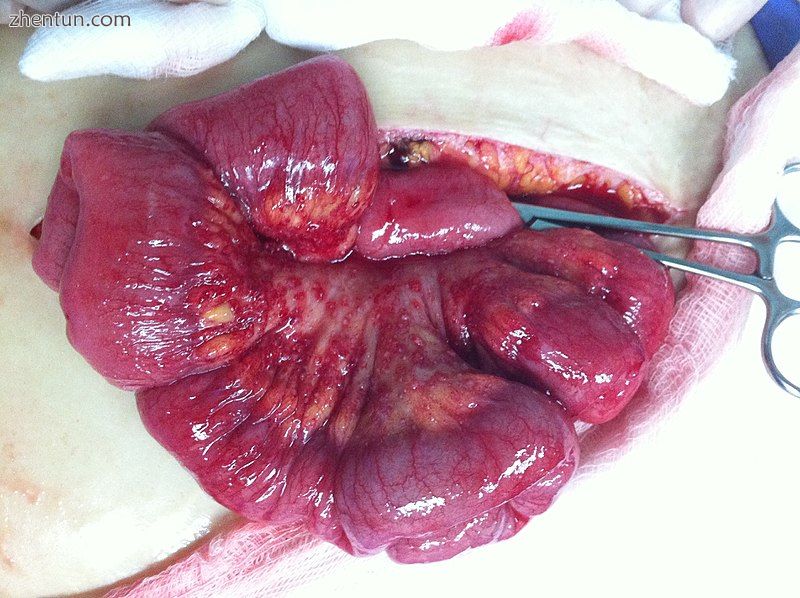
卵巢腺癌沉积在小肠的肠系膜中
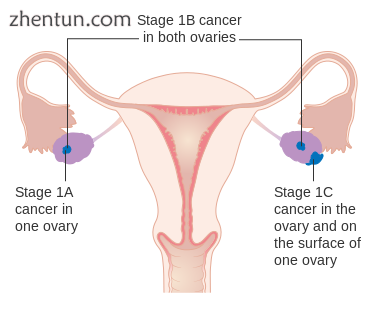
第1阶段卵巢癌
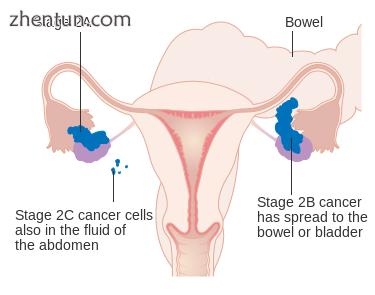
第2阶段卵巢癌
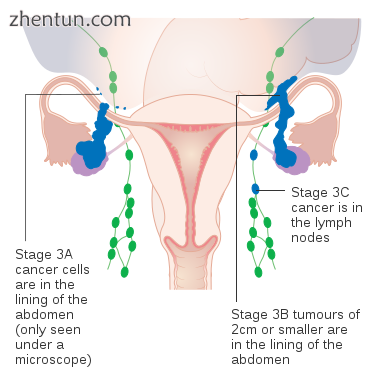
第3阶段卵巢癌
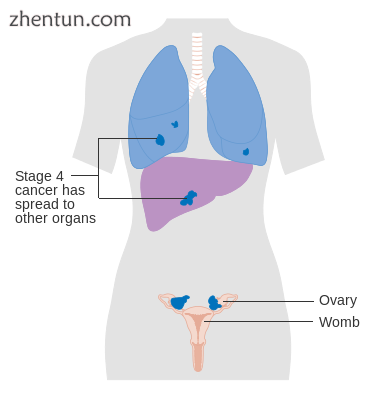
第4阶段卵巢癌
等级
1级肿瘤具有分化良好的细胞(看起来与正常组织非常相似),并且是具有最佳预后的细胞。 2级肿瘤也称为中度分化良好,它们由类似于正常组织的细胞组成。 3级肿瘤预后最差,细胞异常,称为低分化。[50]
卵巢癌的转移在腹部非常常见,并且通过剥脱发生,其中癌细胞通过卵巢囊破裂并且能够在整个腹膜腔中自由移动。卵巢癌转移通常生长在器官表面而不是内部;它们在网膜和腹膜衬里也很常见。癌细胞也可以穿过淋巴系统并通过血管转移到与卵巢相连的淋巴结;即沿着infundibulopelvic韧带,阔韧带和圆韧带的淋巴结。最常见的受影响组包括主动脉旁,腹下,髂外,闭孔和腹股沟淋巴结。通常,卵巢癌不会转移到肝脏,肺脏,大脑或肾脏,除非它是复发性疾病;这可以将卵巢癌与许多其他形式的癌症区分开来。[19]
筛选
对于没有任何体征或症状的女性,没有简单可靠的方法来检测卵巢癌。对于平均风险的女性,不建议进行筛查,因为证据不支持减少死亡,并且高误报率可能导致不必要的手术,伴随着自身的风险。[14]巴氏试验不能筛查卵巢癌。[17]
卵巢癌通常只能在晚期发现。[19]对于平均风险的女性,不建议使用CA-125测量,HE4水平,超声波或附件触诊进行筛查。可以减少遗传因素患者患卵巢癌的风险。那些具有遗传倾向的人可能会受益于筛查。这个高风险群体受益于早期发现。[18] [16] [51]
卵巢癌的患病率很低,即使在50至60岁的高风险组中(2000年约为1例),对平均风险的女性进行筛查比发现需要治疗的问题更容易产生模棱两可的结果。 。由于模糊结果比检测可治疗问题更可能,并且因为对模糊结果的通常反应是侵入性干预,对于具有平均风险的女性,没有指示的筛查的潜在危害大于潜在的益处。筛查的目的是在早期阶段诊断卵巢癌,因为卵巢癌更容易被成功治疗。[16] [51]
对于有BRCA1或BRCA2突变的女性,可以使用经阴道超声,盆腔检查和CA-125水平筛查代替预防性手术。这一战略取得了一些成功。[19]
预防
卵巢癌遗传风险较高的人可能会考虑手术切除卵巢作为预防措施。这通常在育龄期结束后进行。这降低了高风险人群患乳腺癌(约50%)和卵巢癌(约96%)的可能性。患有BRCA基因突变的女性通常也会同时切除输卵管(输卵管卵巢切除术),因为它们也会增加输卵管癌的风险。然而,由于研究方式,这些统计数据可能会高估风险降低。[16] [51]
有卵巢癌家族史的人通常会被提交给遗传咨询师,看看BRCA突变检测是否有益。[19]口服避孕药的使用,月经周期中没有“期间”以及输卵管结扎可降低风险。[52]在不孕症治疗期间可能存在发展卵巢癌和卵巢刺激的关联。子宫内膜异位症与卵巢癌有关。人乳头瘤病毒感染,吸烟和滑石粉尚未被确定为增加患卵巢癌的风险[18]。
管理
一旦确定存在卵巢,输卵管或原发性腹膜癌,由妇科肿瘤学家(经过训练以治疗女性生殖系统癌症的医生)安排治疗。妇科肿瘤科医生可以对卵巢癌妇女进行手术并给予化疗。制定了治疗计划。[53]
无论卵巢癌的亚型如何,治疗通常包括手术和化疗,有时还需要放疗。[45] [54]对于分化良好的恶性肿瘤并且局限于卵巢的手术治疗可能是足够的。对于局限于卵巢的更具侵袭性的肿瘤,可能需要加入化学疗法。对于患有晚期疾病的患者,手术减少与联合化疗方案的组合是标准的。边缘肿瘤,即使在卵巢外扩散,也可以通过手术很好地进行治疗,并且化疗不被视为有用。[55]第二次手术和维持化疗尚未显示出有益效果。[19]自2019年起,Lynparza(olaparib)将在英格兰推出,以帮助患有卵巢癌遗传形式的女性。[56]
手术
几十年来,手术一直是护理的标准,可能是获得诊断标本所必需的。手术取决于癌症在诊断时附近侵入其他组织的程度。通过将癌症指定为阶段,推定类型和癌症等级来描述这种程度的癌症。妇科外科医生可以切除一个(单侧卵巢切除术)或两个卵巢(双侧卵巢切除术)。也可以去除输卵管(输卵管切除术),子宫(子宫切除术)和网膜(卵巢切除术)。通常,所有这些器官都被移除。[57]
对于低度,单侧IA期癌症,仅切除涉及的卵巢(必须未破裂)和输卵管。这尤其适用于希望保持生育能力的年轻人。然而,存在微观转移的风险并且必须完成分期。[18]如果发现任何转移,则需要进行第二次手术以切除剩余的卵巢和子宫。[55]可以在手术前给予传明酸,以减少因手术过程中失血而输血的需要。[21]
如果绝经前妇女的肿瘤在手术期间被确定为低恶性潜在肿瘤,并且显然是I期癌症,则仅移除受影响的卵巢。对于具有低恶性潜在肿瘤的绝经后妇女,双侧输卵管卵巢切除术的子宫切除术仍然是首选方案。在分期期间,可以检查或移除附录。这对粘液性肿瘤尤其重要。[19]在患有卵巢癌的儿童或青少年中,外科医生通常会尝试保留一个卵巢以便完成青春期,但如果癌症已经扩散,这并不总是可行的。特别是无性细胞瘤往往会影响两个卵巢:两个卵巢中都存在8-15%的无性细胞瘤。[23]患有低度(分化良好)肿瘤的人通常只接受手术治疗[16],这通常是治愈性的。[45]一般而言,生殖细胞肿瘤可以用单侧手术治疗,除非癌症普遍存在或生育不是一个因素。[22]
在晚期癌症中,完全切除不是一种选择,尽可能多的肿瘤在称为减积手术的过程中被移除。这种手术并不总是成功,并且在腹膜,IV期疾病,肝脏横切裂,肠系膜或膈肌以及大面积腹水中广泛转移的女性中成功的可能性较小。消肿手术通常只进行一次。[18]更完全的减瘤与更好的结果相关:减数后没有肉眼可见疾病证据的女性中位生存期为39个月,相比之下,17个月手术完成较少[16]。通过去除转移,许多对化疗具有抗性的细胞被移除,并且任何已经死亡的细胞团块也被移除。这使得化疗可以更好地到达剩余的癌细胞,这些癌细胞更可能是快速生长的,因此也是化学敏感的。[19]
间期减瘤手术是另一种使用的方案,其中给予新辅助化疗,进行减瘤手术,并在减瘤后完成化疗。[55]虽然没有完成确定的研究,但在生存方面,它显示出大致相当于原发性减瘤手术,并且发病率略低。[19]
有几种不同的外科手术可用于治疗卵巢癌。对于I期和II期癌症,可以使用腹腔镜(锁孔)手术,但可能未发现转移。对于晚期癌症,不使用腹腔镜检查,因为切除转移需要进入整个腹膜腔。根据癌症的程度,手术可能包括双侧输卵管卵巢切除术,整个腹膜和腹部淋巴系统活检,卵巢切除术,脾切除术,肠切除术,膈肌剥离术或切除术,阑尾切除术,甚至骨盆后切除术[19]。
为了完全分期卵巢癌,淋巴结切除术可以包括在手术中,但这种做法可能不会发生显着的生存获益。[18]这在生殖细胞肿瘤中尤其重要,因为它们经常转移到附近的淋巴结。[16]
如果卵巢癌复发,二次手术有时是一种治疗选择。这取决于肿瘤切除的容易程度,腹部积液量和整体健康状况。[18]对于那些由多面手和上皮性卵巢癌进行第一次手术的人来说,这可能会有所帮助。[21]二次手术可以有效治疗弥漫性疾病和未成熟的畸胎瘤[22]。
卵巢切除术对年轻女性的主要副作用是早期绝经,这可能导致骨质疏松症。手术后,可考虑使用激素替代疗法,尤其是年轻女性。该疗法可以由雌激素和孕酮或单独的雌激素组合而成。子宫切除术后单独使用雌激素是安全的;当子宫仍然存在时,无对抗的雌激素会显着增加子宫内膜癌的风险。[18]手术后的雌激素治疗不会改变生存率。[21]患有卵巢癌手术的人通常在住院治疗3-4天,并在家中恢复一个月左右。[58]手术结果最适合做大量卵巢癌手术的医院。[19]
目前尚不清楚FIGO I期卵巢癌的腹腔镜检查或剖腹手术是更好还是更差。[59]对于晚期癌症,全腹子宫切除术和子宫上子宫切除术之间也没有明显差异。首次手术治疗晚期卵巢癌的人中约有2.8%在手术后两周内死亡(围手术期死亡率为2.8%)。[21]更积极的手术与晚期(III期或IV期)卵巢癌的更好结果相关[19]。
化疗
几十年来,化疗一直是卵巢癌护理的一般标准,尽管有不同的方案。如果合适,在手术后使用化疗来治疗任何残留的疾病。在某些情况下,可能有理由首先进行化疗,然后进行手术。这被称为“新辅助化疗”,并且当肿瘤不能通过手术完全去除或最佳地减压时是常见的。虽然没有显示它可以提高生存率,但它可以降低手术后并发症的风险。如果进行单侧输卵管卵巢切除术或其他手术,可以给予额外的化疗,称为“辅助化疗”。[18] [21]如果肿瘤具有高组织学分级(3级)或最高分期(1c期),则辅助化疗用于1期癌症,前提是癌症已在手术期间进行了最佳分期[21] [55]。如果在手术期间肿瘤未完全切除或癌症是IV期,Bevacizumab可用作辅助化疗;它可以延长无进展生存期,但尚未证明可以延长总生存期。[21]大约20%的晚期卵巢癌化疗是有疗效的[19],它对恶性生殖细胞肿瘤的治疗效果往往高于上皮性肿瘤[22]。
卵巢癌的化疗通常由铂类,一组铂类药物和非铂类药物组成。常用疗法可包括紫杉醇,顺铂,托泊替康,阿霉素,表柔比星和吉西他滨。卡铂通常与紫杉醇或多西紫杉醇联合给药;典型的组合是卡铂与紫杉醇。[18] [21]卡铂优于顺铂,因为它毒性较小,副作用较少,相比之下通常可以提高生活质量,尽管两者同样有效。[21]尚未发现三种药物治疗方案更为有效[18],单独使用铂类药物或单独使用非药物治疗方案的效果不如铂类药物和非药物联合药物有效。[21]化疗可以静脉注射或腹腔注射[16]。虽然腹腔内化疗与较长的无进展生存期和总生存期相关,但它也会导致比静脉化疗更多的不良副作用[21]。它主要用于癌症最佳消除时。腹腔内化疗可能非常有效,因为卵巢癌主要在腹腔内扩散,更高剂量的药物可以通过这种方式到达肿瘤。[19]
化疗可导致贫血;在减少输血需求方面,人们发现静脉注射铁比口服铁补充剂更有效。[21]典型的治疗周期包括每3周一次治疗,重复6周或更长时间。[60]少于6周(周期)的治疗效果不如6周或更长时间。[21]生殖细胞恶性肿瘤的治疗方法与其他卵巢癌的治疗方法不同 - 使用博来霉素,依托泊苷和顺铂(BEP)治疗,每3周进行5天化疗,持续3到4个周期[16] [22]。生殖细胞肿瘤的化学疗法尚未被证实可引起闭经,不孕,出生缺陷或流产。[22]维持化疗尚未证实有效。[21]
在患有BRCA突变的人群中,铂类化疗更有效。[18]生殖细胞肿瘤和恶性性索/间质肿瘤用化学疗法治疗,虽然无性细胞瘤和性索肿瘤通常不是非常敏感。[16] [23]
铂金敏感或铂金抗性
如果卵巢癌复发,则根据自铂类治疗的最后一次复发后的时间被认为是部分铂敏感或铂抗性:在最后一次治疗后6-12个月复发部分铂敏感的癌症,并且铂抗性癌症具有间隔不到6个月。在癌症出现症状后可以给予二线化疗,因为在治疗无症状(CA-125升高)和症状复发之间没有存活差异。
对于铂敏感性肿瘤,铂类是二线化疗的首选药物,与其他细胞毒性药物联合使用。方案包括卡铂联合聚乙二醇化脂质体多柔比星,吉西他滨或紫杉醇。[16]在某些情况下,卡铂 - 双联疗法可与紫杉醇联合使用以提高疗效。对铂敏感性复发的另一种潜在辅助治疗是奥拉帕尼,它可以改善无进展生存期,但尚未显示可提高总体生存率。[21] (美国FDA批准Olaparib用于先前接受过化疗的BRCA相关卵巢癌。[61])对于复发性生殖细胞肿瘤,另外4个周期的BEP化疗是第一个 - 对于那些已经接受手术或铂类治疗的患者进行治疗。
如果确定肿瘤是铂抗性的,则长春新碱,放线菌素和环磷酰胺(VAC)或紫杉醇,吉西他滨和奥沙利铂的某种组合可用作二线疗法。[22]
对于铂类耐药肿瘤,没有高效的化疗方案。单药方案(多柔比星或托泊替康)的反应率不高,[18]但在某些情况下使用托泊替康,聚乙二醇化脂质体多柔比星或吉西他滨的单药方案[16] [21]。拓扑替康不能用于肠梗阻患者。单独使用紫杉醇是另一种可能的方案,或者它可以与脂质体多柔比星,吉西他滨,顺铂,托泊替康,依托泊苷或环磷酰胺联合使用。[60] (另见下文的姑息治疗。)
放射治疗
无性细胞瘤最有效地用放射治疗,[23]虽然这可能导致不孕,并且正在逐步淘汰,有利于化疗。[16]放射治疗并不能改善分化良好的肿瘤患者的生存率[16]。
在阶段1c和2期癌症中,如果骨盆中可能存在残留疾病但腹部无癌症,则在手术后使用放射疗法。放射疗法也可用于晚期癌症的姑息治疗。卵巢癌的典型放疗过程是每周5天,持续3-4周。放射治疗的常见副作用包括腹泻,便秘和尿频。[62]
荷尔蒙疗法
尽管60%的卵巢肿瘤具有雌激素受体,但卵巢癌对激素治疗的反应很少。单独使用雌激素对癌症没有影响,而他莫昔芬和来曲唑很少有效。[18] “一些患有恶性肿瘤卵巢癌和间质性卵巢癌的妇女可能接受激素治疗。”[57]
免疫治疗
免疫疗法是目前卵巢癌研究的一个主题。在某些情况下,抗体药物贝伐单抗虽然仍然是一个活跃的研究课题,但它被用于治疗晚期癌症以及化疗。[55]它已在欧盟批准用于此用途。[63]
随访
具体的随访取决于例如卵巢癌的类型和阶段,治疗和任何症状的存在。通常,最初每2至3个月进行一次检查,然后每年进行两次,最多5年。[64]对于上皮性卵巢癌,随访时最常见的检查是CA-125水平。然而,仅基于升高的CA-125水平而不是任何症状的治疗可以增加副作用而不会延长寿命,因此CA-125测试结果的含义可以在服用之前进行讨论。[65]如果CA-125水平是正常水平的两倍,那么截至2014年的建议是可能存在复发性癌症。[18]治疗CA-125检测到的复发并不能提高生存率。[21]
对于患有生殖细胞肿瘤的女性,随访试验通常包括甲胎蛋白(AFP)和/或人绒毛膜促性腺激素。对于患有间质性癌症的女性,对雌激素,睾丸激素和抑制素等激素的检测有时会有所帮助。[65]抑制素也可用于监测性索肿瘤的进展,以及苗勒抑制物质。 AFP也可用于监测Sertoli-Leydig肿瘤。[16]在无性细胞瘤,乳酸脱氢酶及其两种同工酶(LDH-1和LDH-2)用于检测复发。[22]
患有卵巢癌的妇女可能不需要常规监测成像来监测癌症,除非出现新症状或肿瘤标志物开始上升。[66]没有这些适应症的成像是不鼓励的,因为它不太可能发现复发,提高生存率,因为它有自己的成本和副​​作用。[66]但是,如果需要,可以使用CT成像,尽管这并不常见。[18]如果肿瘤容易成像,可以使用成像来监测治疗进展。[67]
姑息治疗
姑息治疗的重点是缓解症状,提高或保持生活质量。这种治疗的目的不是为了治愈癌症,而是为了让女性在患有无法治愈的癌症时更加舒适。对于任何患有晚期卵巢癌的患者或有明显症状的患者,建议将其作为治疗计划的一部分。[68]在铂类难治性和铂类耐药病例中,其他姑息性化疗是主要治疗方法。[19] [57]
姑息治疗可能需要治疗癌症的症状和并发症,包括疼痛,恶心,便秘,腹水,肠梗阻,水肿,胸腔积液和粘膜炎。特别是如果癌症进展并变得无法治愈,症状的治疗成为治疗的主要目标之一。姑息治疗还可能需要帮助做出决策,例如临终关怀是否适当,何时适当,以及患者在临终关怀时的首选地点。[21]
肠梗阻可以通过姑息性手术(结肠造口术,回肠造口术或内部旁路术)或药物治疗,但手术已被证明可以延长生存时间。[18] [21]姑息性手术可能导致短肠综合征,肠外瘘或再梗阻;或由于阻碍的程度而可能无法实现。[19]其他并发症的治疗方法包括全胃肠外营养,低残留饮食,姑息性胃造口术和足够的疼痛控制。[18]当姑息性手术不可行时,也可以用奥曲肽治疗肠梗阻。癌症也可以阻塞输尿管,可以通过肾造口术或输尿管支架来缓解输尿管。腹水可以通过反复腹腔穿刺或放置引流管来缓解,以增加舒适度。[69]胸腔积液可以类似方式进行治疗,反复胸腔穿刺,胸膜固定术或置换引流管[19]。
放射治疗可以作为晚期卵巢癌姑息治疗的一部分,因为它可以帮助缩小导致症状的肿瘤。[57]姑息性放疗通常仅持续几次治疗,疗程比非姑息性放疗短得多。[62]它还用于缓解化疗耐药的生殖细胞肿瘤。[22]
心理社会关怀
卵巢癌对生活质量,心理健康和幸福感有显着影响。干预措施可以帮助满足需求和社会支持。许多卵巢癌幸存者报告了良好的生活质量和乐观情绪。其他人报告了一种“精神变化”,帮助他们在经历中找到了意义。其他人描述了他们在诊断卵巢癌后失去信心。那些经历过治疗的人有时会经历社会隔离,但从与其他幸存者的关系中受益。一些表示无法照顾家庭的人已经描述了挫折感和内疚感。[70]
由于脱发,卵巢和其他生殖结构的去除以及疤痕,可能会出现自尊和身体形象的变化。头发生长后有一些改善。性问题可能会发展。卵巢切除导致手术引起的绝经,可导致性交疼痛,阴道干涩,性欲丧失和疲倦。虽然对于年轻的幸存者来说预后更好,但对性行为的影响仍然很大。[70]
存活卵巢癌的焦虑,抑郁和痛苦的发生率高于普通人群。[70] [71]家庭成员可能会出现同样的社会心理问题。情绪影响可能包括对死亡的恐惧,悲伤,记忆问题和集中注意力的困难。当他们在治疗开始时采用乐观态度时,他们就不太可能患上痛苦。那些担心癌症复发的人即使在没有疾病的情况下也可能难以表达喜悦。女性接受的治疗越多,表达失去希望的可能性就越大。妇女通常可以通过一系列策略来应对和减少消极的心理社会影响。诸如旅行,与家人和朋友共度额外时间,忽视统计数据,日记和越来越多地参与基于精神的活动等活动都是适应性的。[70]
预测
![Relative five-year survival of invasive epithelial ovarian cancer by stage[72].png Relative five-year survival of invasive epithelial ovarian cancer by stage[72].png](data/attachment/forum/201907/27/120816az2x55h2og2grxxx.png)
分期侵袭性上皮性卵巢癌的相对五年生存率[72]
卵巢癌通常预后相对较差。它不成比例地致命,因为它缺乏任何明确的早期检测或筛查测试,这意味着大多数病例在达到晚期阶段之前不会被诊断出来。[66] [18]
卵巢癌在其发展的早期就会转移,通常在它被诊断出来之前。高级别肿瘤比低级别肿瘤更容易转移。通常,肿瘤细胞通过在腹膜腔内生长而开始转移[16]。超过60%的卵巢癌患者在已经扩散到卵巢之外时患有III期或IV期癌症。卵巢癌将细胞分解到腹腔内的天然存在的液体中。然后这些细胞可以植入其他腹部(腹膜)结构,包括子宫,膀胱,肠,肠壁衬里和网膜,甚至在癌症被怀疑之前形成新的肿瘤生长。
卵巢癌各阶段的五年存活率为46%;一年生存率为72%,十年生存率为35%。[73]对于在疾病早期进行诊断的病例,当癌症仍局限于原发部位时,五年生存率为92.7%。[74]大约70%的晚期疾病女性对初始治疗有反应,其中大多数达到完全缓解,但这些女性中有一半在治疗后1 - 4年内复发[16]。脑转移在III / IV期癌症中更常见,但仍可发生在I / II阶段的癌症中。虽然手术,化疗和全脑放射治疗可以提高生存率,但脑转移患者的中位生存时间为8.2个月[21]。
卵巢癌的存活率随着亚型的不同而显着不同。 无性细胞瘤具有非常有利的预后。在早期阶段,他们的五年生存率为96.9%。[23]大约三分之二的无性细胞瘤在第一阶段被诊断出来。[22] III期念珠菌病的五年生存率为61%;在不完全手术切除后进行BEP化疗时,无性细胞瘤的两年生存率为95%。性索间质恶性肿瘤也有良好的预后;因为它们生长缓慢,即使患有转移性疾病的人也可以存活十年或更长时间。[16]当在腹膜腔中发现侵入性肿瘤植入物时,低恶性潜在肿瘤通常仅具有不良预后。[19]
卵巢癌的并发症可包括癌症扩散到其他器官,各种器官的进行性功能丧失,腹水和肠梗阻,这可能是致命的。多个部位的肠梗阻是最常见的致死原因。[18]当肿瘤阻止正常蠕动时,卵巢癌的肠梗阻可能是真正的阻塞,肿瘤阻塞肠腔,或假性阻塞。[75]可以通过放置可以自行排水的排水管来治疗腹水的持续积聚。[18]
预后因素
卵巢癌有许多预后因素。阳性预后因素 - 那些表明存活率更高的因素 - 包括术后无残留疾病(III / IV期),完全肉眼切除术(IV期),BRCA2突变,年龄小(45岁以下),非真性类型,低组织学分级,早期,与子宫内膜癌同时发生,CA-125水平低。 BRCA1作为预后因素存在相互矛盾的证据。相反,阴性预后因素 - 那些表明生存机会较差的因素 - 包括手术期间卵巢囊破裂,年龄较大(45岁以上),粘液型,IV期,组织学分级高,透明细胞类型,上腹部受累,高CA-125水平,血液中存在肿瘤细胞,环氧合酶-2升高。[21]
各种mRNA的表达也可以预测卵巢癌。高水平的Drosha和Dicer与改善的存活率相关,而高水平的let-7b,HIF1A,EphA1和聚(ADP-核糖)聚合酶与较差的存活率相关。对WT1呈阳性的癌症预后较差;雌激素受体阳性的癌症预后较好。[21]
生存率
根据美国癌症协会的数据,下面给出的存活率是针对不同类型的卵巢癌。[72]他们来自SEER国家癌症研究所,基于2004年至2010年诊断出的患者。
侵袭性上皮性卵巢癌
复发率
卵巢癌经常在治疗后复发。总体而言,在5年期间,20%的I期和II期癌症复发。大多数复发都在腹部。[19]如果晚期疾病复发,通常在初始治疗后18个月内发生(18个月无进展生存期)。可以治疗复发,但随着每次复发,无病间隔趋于缩短,化疗耐药性也会增加。[18]当无性细胞瘤复发时,最有可能在诊断后一年内复发,其他恶性生殖细胞肿瘤在90%的时间内在2年内复发。除了弥漫性疾病之外的生殖细胞肿瘤在复发时预后不良,长期存活率为10%[22]。低恶性潜在肿瘤很少复发,即使保留生育能力的手术是首选治疗方法。在先前未受影响的卵巢中,15%的LMP肿瘤在单侧手术后复发,并且它们通常易于通过手术治疗。更高级的肿瘤可能需要长达20年才能复发,如果它们完全复发,并且只能通过手术治疗,除非肿瘤已改变其组织学特征或非常快速地生长。在这些情况下,当存在显着的腹水时,也可以使用化学疗法。复发通常表现为CA-125水平升高,然后在2-6个月内发展为症状性复发[19]。复发性性索间质肿瘤通常对治疗无反应但不具有攻击性。[22]
它是最致命的妇科癌症。[19]
流行病学
2014年,发达国家发生的新病例数约为每10万人9.4例,而发展中国家则为每10万人5.0例。[18]在全球范围内,2010年约有160,000人死于卵巢癌。这比1990年的113,000人增加。[77]欧洲每年新发病例数约为每10万名妇女5-15例。[21]在欧洲,立陶宛,拉脱维亚,爱尔兰,斯洛伐克和捷克共和国的卵巢癌发病率最高,而葡萄牙和塞浦路斯的发病率最低。[21] 2008年,五年生存率为44%。自1977年存活率为36%以来,情况有所增加。[70]
美国
![Age-standardized death from ovarian cancer per 100,000 inhabitants in 2004[76].jpg Age-standardized death from ovarian cancer per 100,000 inhabitants in 2004[76].jpg](data/attachment/forum/201907/27/120811umrmkq4jfv74ov4h.jpg)
2004年每10万居民死于卵巢癌的年龄标准化死亡率[76]
![Ovarian cancer cases diagnosed by age group in the US[74].png Ovarian cancer cases diagnosed by age group in the US[74].png](data/attachment/forum/201907/27/120815l22xxzvqlrdzcf7r.png)
美国按年龄组诊断的卵巢癌病例[74]
2010年,在美国,估计有21,880个新病例被诊断出来,13,850个女性死于卵巢癌。大约1,800个新诊断是性索或间质肿瘤。[16]
2014年,每年制造超过220,000例上皮性卵巢癌诊断。[18]美国的整体终身风险约为1.6%[16] [21]在美国,卵巢癌影响1.3-1.4%,是约1%女性死亡的原因。[19] [78]在美国,它也是女性中第五大常见癌症,但却是癌症死亡的第四大常见原因。[21]这种下降使其成为女性中第九位最常见的癌症。[19]
发展特定类型的卵巢癌的风险各不相同。生殖细胞肿瘤和性索间质肿瘤不如上皮肿瘤常见。美国每年新发病例数分别为每10万名女性0.4名,每10万名女性0.2名。在年轻人中,性索间质肿瘤和生殖细胞肿瘤占总卵巢癌的1%[22]。卵巢癌约占女性诊断癌症的4%。[21]
英国
它是英国女性中第5位最常见的癌症。[21] [24]在英国,整个人口的发病率为每10万人21.6。
截至2014年,在英国,每年诊断约7,000-7,100人,死亡人数为4,200人。[18] [24]英国的风险相似,为1.7%。 Ashkenazi犹太妇女携带突变的BRCA等位基因的频率是其他人群的五倍,这使她们患上卵巢癌的风险更高。[18]它是2008年美国癌症相关死亡人数的第五大原因,估计为15,000人。[16] [78]卵巢癌是英国女性中第五大常见癌症(2011年约有7,100名女性被诊断患有该病),并且是女性癌症死亡的第五大常见原因(2012年约有4,300名女性死亡)。 [79]
种族
与非黑人女性相比,黑人女性患有性索间质肿瘤的风险是其两倍。[22]
老年妇女
在美国,50岁以上女性的发病率约为每10万人中有33人。[80]在40-49岁年龄组和50-64岁年龄组的女性中,1993年至2008年的卵巢癌发病率下降[18]。卵巢癌最常见于绝经后,[24]年龄在60到64岁之间.90%的卵巢癌发生在45岁以上的女性中,80%发生在50岁以上的女性中[21]。老年女性更容易患上晚期卵巢癌。[15]
在怀孕期间
恶性生殖细胞肿瘤是最可能在怀孕期间发生的卵巢癌类型。它们通常在检查时发现附件包块(占所有妊娠的1-2%),超声检查肿瘤或父母甲胎蛋白水平升高时被诊断出来。皮样囊肿和无性细胞瘤是妊娠期间最常见的生殖细胞肿瘤。在怀孕期间诊断出的生殖细胞肿瘤不太可能已经转移,并且可以通过手术治疗,并且在某些情况下,可以通过化学治疗,其具有出生缺陷的风险。卵黄囊肿瘤和未成熟畸胎瘤的生长特别快,通常甚至在怀孕期间接受化疗;然而,经过最佳减效的dysgermino可以在分娩后进行治疗。[22]
其他动物
在马母马中已经报道了卵巢肿瘤。报告的肿瘤类型包括畸胎瘤,[81] [82]囊腺癌,[83]尤其是颗粒细胞瘤。[84] [85] [86] [87] [88]
研究
筛选
通过宫腔镜筛查获得用于组织学检查的细胞样品正在开发中。这类似于目前用于检测宫颈癌的子宫颈抹片检查。[89]英国卵巢癌筛查合作试验正在测试一种结合CA-125血液检测和经阴道超声检查的筛查技术[18]。其他研究表明,这种筛查程序可能有效。[63]尽管2015年公布的结果尚无定论,但有证据表明,筛查可以长期挽救生命。[90]结果,该试验已经延长,并将在2019年底公布确定的结果。筛查的一个主要问题是没有明显的疾病进展从第一阶段(非侵入性)到第三阶段(侵入性),并且可能在达到第三阶段之前无法找到癌症。另一个问题是筛查方法往往发现太多可疑病变,其中大多数不是癌症,但恶性肿瘤只能通过手术评估。[18] ROCA方法结合经阴道超声检查正在高风险女性中进行研究,以确定它是否是一种可行的筛查方法。正在对正常风险的妇女进行调查,因为它已在更广泛的人群中显示出希望。[19]目前正在进行研究以确定筛查是否有助于早期发现BRCA突变患者的癌症。[63]
预后研究
对卵巢癌的各种预后因素的研究也在进行中。最近的研究表明,血小板增多症预示着较低的生存率和较高的癌症阶段[18]。正在进行的研究还在研究手术治疗复发性卵巢癌的益处。[63]
免疫治疗
虽然是一个活跃的研究领域,但自2018年以来,没有任何免疫疗法被证明是有效的。[91]然而,抗体和VEGF抑制剂bevacizumab的试验,可以减缓癌症中新血管的生长,已经显示出有希望的结果,特别是与帕唑帕尼组合,这也减缓了血管生长的过程。贝伐单抗在III期和-IV期癌症的初步研究中特别有效[18],并被引用至少有15%的反应率。[16]目前正在研究粘液性卵巢癌。[63]
药理
mTOR抑制剂是在2000年代和2010年代被高度研究的潜在治疗方法,但这些药物的副作用(特别是高血糖和高脂血症)没有得到很好的耐受,并且未证实存活益处。 PI3激酶抑制剂一直备受关注,但它们往往具有高毒性并导致腹泻。另一种被研究的药物是selumetinib,一种MAPK抑制剂。它提高了存活率,但与肿瘤中发现的任何突变无关。[18]
贝伐单抗还可以与铂类化疗联合使用,这种组合在PFS中具有积极的初步结果,但在整体存活方面具有可疑结果。这些治疗的一个缺点是副作用特征,其包括高血压和蛋白尿。该药还可以加剧肠道疾病,导致瘘管或肠穿孔。 Vintafolide,由与长春碱结合的抗叶酸组成,也在临床试验中;它可能证明是有益的,因为叶酸受体在许多卵巢癌中过度表达。[18]另一种潜在的免疫疗法是曲妥珠单抗,其对Her2 / neu突变阳性的肿瘤具有活性[16]。其他血管生成抑制剂也正在作为潜在的卵巢癌治疗进行研究。 Combretastatin和pazopanib正在联合研究用于复发性卵巢癌。 Trebananib和tasquinimod是正在研究的其他血管生成抑制剂。正在研究单克隆抗体farletuzumab作为传统化学疗法的佐剂。另一种类型的免疫疗法涉及疫苗,包括TroVax。[63]
BEP化疗的替代方案,卡铂和依托泊苷的3个周期的方案,是生殖细胞恶性肿瘤研究的当前主题。[22]
在2000年代和2010年期间,腹膜内化疗也有可能向肿瘤提供更高剂量的细胞毒剂。顺铂和紫杉醇的初步试验表明它不能很好地耐受,但确实可以提高生存率,并且正在研究更多可耐受的治疗方案。[18]顺铂和紫杉醇都被研究为腹膜内化疗药物。针对罕见透明细胞癌的特定化疗方案也在研究中:伊立替康联合顺铂[63]。
PARP抑制剂在早期试验中也显示出前景,特别是在BRCA基因突变的人群中,因为BRCA蛋白与PARP途径相互作用。一般来说,它也在复发性卵巢癌中进行研究,初步研究显示PFS较长。具体而言,与多柔比星相比,奥拉帕尼显示出更高的存活率,尽管这种治疗方法仍在研究中。目前尚不清楚哪种生物标志物可预测对PARP抑制剂的反应性。[18] Rucaparib是另一种PARP抑制剂,正在研究BRCA阳性和BRCA阴性复发性晚期卵巢癌。 Niraparib是一种PARP抑制剂,用于检测BRCA阳性的复发性卵巢癌。[63]
酪氨酸激酶抑制剂是另一种可用于卵巢癌的研究药物。受体酪氨酸激酶抑制剂组中的血管生成抑制剂,包括帕唑帕尼,西地尼布和nintedanib,也已被证明可以提高无进展生存期(PFS),但截至2015年尚未对其总生存期的益处进行调查。[18]初步研究表明,西地尼布联合铂类复发卵巢癌可使第二次复发的时间延长3-4个月,并使存活率提高3个月。[63] MK-1775是一种酪氨酸激酶抑制剂,与铂类敏感的p53突变癌症患者联合使用紫杉醇和卡铂。正在研究Nintedanib作为复发患者与环磷酰胺联合使用的潜在疗法。[63]
组蛋白去乙酰化酶抑制剂(HDACi)是另一个研究领域。
激素和辐射
激素疗法是目前卵巢癌研究的一个主题,特别是用于治疗乳腺癌的某些药物的价值。这些包括他莫昔芬,来曲唑和阿那曲唑。初步研究表明,少数晚期卵巢癌患者可使用他莫昔芬。来曲唑可能有助于减缓或阻止雌激素受体阳性卵巢癌的生长。正在对患有雌激素受体阳性癌症的绝经后人群进行阿那曲唑的研究。[63]
减少卵巢癌治疗副作用的研究也在进行中。放射性纤维化,在放射治疗的区域中形成瘢痕组织,可以通过高压氧疗法缓解,但是在该领域尚未完成研究。卵巢癌的治疗也可能导致人们经历精神障碍,包括抑郁症。目前正在进行研究,以确定咨询和心理治疗如何帮助治疗期间患卵巢癌的人。[63]
炎症
有一些迹象表明盆腔炎可能与卵巢癌有关,特别是在非西方国家。这可能是由于炎症过程与盆腔炎有关。[92]
临床试验
临床试验由美国政府组织监测和资助,以测试治疗方案,以确定它们是否安全有效。这些包括美国国立卫生研究院临床研究试验和你(国立卫生研究院),[93]了解临床试验(国家癌症研究所),[94]寻找临床试验(国家癌症研究所),[95] ClinicalTrials.gov(国立研究院)健康)。[96] [53]临床试验也在加拿大进行。[97]
参考:
"Ovarian Epithelial Cancer Treatment (PDQ®)". NCI. 2014-05-12. Archived from the original on 5 July 2014. Retrieved 1 July 2014.
"What are the risk factors for ovarian cancer?". www.cancer.org. 2016-02-04. Archived from the original on 17 May 2016. Retrieved 18 May 2016.
World Cancer Report 2014. World Health Organization. 2014. Chapter 5.12. ISBN 978-9283204299. Archived from the original on 2016-09-19.
"Ovarian Cancer Prevention (PDQ®)". NCI. December 6, 2013. Archived from the original on 6 July 2014. Retrieved 1 July 2014.
"Ovarian Cancer Prevention (PDQ®)". NCI. 2014-06-20. Archived from the original on 6 July 2014. Retrieved 1 July 2014.
"SEER Stat Fact Sheets: Ovary Cancer". NCI. Archived from the original on 6 July 2014. Retrieved 18 June 2014.
GBD 2015 Disease and Injury Incidence and Prevalence Collaborators (8 October 2016). "Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990–2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1545–1602. doi:10.1016/S0140-6736(16)31678-6. PMC 5055577. PMID 27733282.
GBD 2015 Mortality and Causes of Death Collaborators (8 October 2016). "Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980–2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1459–1544. doi:10.1016/S0140-6736(16)31012-1. PMC 5388903. PMID 27733281.
Seiden, Michael (2015). "Gynecologic Malignancies, Chapter 117". MGraw-Hill Medical. Archived from the original on September 10, 2017. Retrieved June 24, 2017.
"Defining Cancer". National Cancer Institute. 2007-09-17. Archived from the original on 25 June 2014. Retrieved 10 June 2014.
Ebell, MH; Culp, MB; Radke, TJ (March 2016). "A Systematic Review of Symptoms for the Diagnosis of Ovarian Cancer". American Journal of Preventive Medicine. 50 (3): 384–94. doi:10.1016/j.amepre.2015.09.023. PMID 26541098.
Ruddon, Raymond W. (2007). Cancer biology (4th ed.). Oxford: Oxford University Press. p. 223. ISBN 9780195175431. Archived from the original on 2015-09-15.
Piek JM, van Diest PJ, Verheijen RH (2008). Ovarian carcinogenesis: an alternative hypothesis. Adv. Exp. Med. Biol. Advances in Experimental Medicine and Biology. 622. pp. 79–87. doi:10.1007/978-0-387-68969-2_7. ISBN 978-0-387-68966-1. PMID 18546620.closed access
Grossman, David C.; Curry, Susan J.; Owens, Douglas K.; Barry, Michael J.; Davidson, Karina W.; Doubeni, Chyke A.; Epling, John W.; Kemper, Alex R.; Krist, Alex H.; Kurth, Ann E.; Landefeld, C. Seth; Mangione, Carol M.; Phipps, Maureen G.; Silverstein, Michael; Simon, Melissa A.; Tseng, Chien-Wen (13 February 2018). "Screening for Ovarian Cancer". JAMA. 319 (6): 588–594. doi:10.1001/jama.2017.21926. PMID 29450531.
Gibson, Steven J.; Fleming, Gini F.; Temkin, Sarah M.; Chase, Dana M. (2016). "The Application and Outcome of Standard of Care Treatment in Elderly Women with Ovarian Cancer: A Literature Review over the Last 10 Years". Frontiers in Oncology. 6: 63. doi:10.3389/fonc.2016.00063. PMC 4805611. PMID 27047797.
Seiden MV (2012). "Gynecologic Malignancies". In Longo DL, Kasper DL, Jameson JL, Fauci AS, Hauser SL, Loscalzo J (eds.). Harrison's Principles of Internal Medicine (18th ed.). McGraw-Hill. ISBN 978-0-07-174889-6.
"Ovarian Cancer, Inside Knowledge, Get the Facts about Gynecological Cancer" (PDF). Centers for Disease Control and Prevention. September 2016. Archived (PDF) from the original on June 16, 2017. Retrieved June 17, 2017. This article incorporates public domain material from websites or documents of the Centers for Disease Control and Prevention.
Jayson GC, Kohn EC, Kitchener HC, Ledermann JA (October 2014). "Ovarian cancer". Lancet. 384 (9951): 1376–88. doi:10.1016/S0140-6736(13)62146-7. PMID 24767708.
Hoffman, Barbara L.; Schorge, John O.; Schaffer, Joseph I.; Halvorson, Lisa M.; Bradshaw, Karen D.; Cunningham, F. Gary (2012). "Epithelial Ovarian Cancer". Williams Gynecology (2nd ed.). McGraw Hill Medical. pp. 853–878. ISBN 978-0-07-171672-7.
"Ovarian cancer symptoms". www.cancerresearchuk.org. Archived from the original on 2015-05-12. Retrieved 2015-05-16.
"Ovarian cancer". DynaMed. June 18, 2015. Archived from the original on June 21, 2015.
Williams Gynecology 2012
DeCherney, Alan; Nathan, Lauren; Goodwin, T. Murphy; Laufer, Neri; Roman, Ashley (2012). "Pediatric and Adolescent Gynecology". Current Diagnosis & Treatment Obstetrics & Gynecology (11th ed.). ISBN 978-0071638562.
"Ovarian cancer risks and causes". Cancer Research UK. 15 January 2014. Archived from the original on 21 February 2015. Retrieved 29 January 2015.
Gong, Ting-Ting; Wu, Qi-Jun; Vogtmann, Emily; Lin, Bei; Wang, Yong-Lai (2013-06-15). "Age at menarche and risk of ovarian cancer: a meta-analysis of epidemiological studies". International Journal of Cancer. 132 (12): 2894–2900. doi:10.1002/ijc.27952. ISSN 0020-7136. PMC 3806278. PMID 23175139.
Manson JE, Bassuk SS (2012). "The Menopause Transition and Postmenopausal Hormone Therapy". In Longo DL, Kasper DL, Jameson JL, Fauci AS, Hauser SL, Loscalzo J (eds.). Harrison's Principles of Internal Medicine (18th ed.). McGraw-Hill. ISBN 978-0-07-174889-6.
"Ovarian Cancer Prevention (PDQ®)". National Cancer Institute. 2013. Archived from the original on 2013-12-31. Retrieved 2013-12-30.
Kyriakidis I, Papaioannidou P (2016). "Estrogen receptor beta and ovarian cancer: a key to pathogenesis and response to therapy". Arch Gynecol Oncol. 293 (6): 1161–8. doi:10.1007/s00404-016-4027-8. PMID 26861465.
Norquist BM, Harrell MI, Brady MF, Walsh T, Lee MK, Gulsuner S, Bernards SS, Casadei S, Yi Q, Burger RA, Chan JK, Davidson SA, Mannel RS, DiSilvestro PA, Lankes HA, Ramirez NC, King MC, Swisher EM, Birrer MJ (2015). "Inherited mutations in women With ovarian carcinoma". JAMA Oncol. 30 (4): 1–9. doi:10.1001/jamaoncol.2015.5495. PMC 4845939. PMID 26720728.
Kuusisto KM, Bebel A, Vihinen M, Schleutker J, Sallinen SL (2011). "Screening for BRCA1, BRCA2, CHEK2, PALB2, BRIP1, RAD50, and CDH1 mutations in high-risk Finnish BRCA1/2-founder mutation-negative breast and/or ovarian cancer individuals". Breast Cancer Res. 13 (1): R20. doi:10.1186/bcr2832. PMC 3109589. PMID 21356067.
Salehi, Fariba; Dunfield, Lesley; Phillips, Karen P.; Krewski, Daniel; Vanderhyden, Barbara C. (1 March 2008). "Risk factors for ovarian cancer: an overview with emphasis on hormonal factors". Journal of Toxicology and Environmental Health, Part B. 11 (3–4): 301–321. doi:10.1080/10937400701876095. PMID 18368558.
"Do we know what causes ovarian cancer?". www.cancer.org. Archived from the original on 2016-11-10.
Hjartåker A, Meo MS, Weiderpass E (January 2010). "Alcohol and gynecological cancers: an overview". European Journal of Cancer Prevention. 19 (1): 1–10. doi:10.1097/CEJ.0b013e328333fb3a. PMID 19926999.
Zhang X, Nicosia SV, Bai W (2006). "Vitamin D receptor is a novel drug target for ovarian cancer treatment". Curr Cancer Drug Targets. 6 (3): 229–44. doi:10.2174/156800906776842939. PMID 16712459.
Biswas A, Oh PI, Faulkner GE, Bajaj RR, Silver MA, Mitchell MS, Alter DA (2015). "Sedentary Time and Its Association With Risk for Disease Incidence, Mortality, and Hospitalization in Adults: A Systematic Review and Meta-analysis". Annals of Internal Medicine. 162 (2): 123–32. doi:10.7326/M14-1651. PMID 25599350.
Odunsi, Kunle; Pejovic, Tanja; Anderson, Matthew L. (2011). Molecular Biology of Gynecologic Cancers. DeVita, Hellman, and Rosenberg's Cancer: Principles and Practice of Oncology. Wolters Kluwer/Lippincott Williams & Wilkins. pp. 1302–1310. ISBN 978-1-4511-0545-2.
"Genetics of Breast and Ovarian Cancer (PDQ®)". National Cancer Institute. 2 October 2014. Archived from the original on 22 October 2014. Retrieved 27 October 2014.
Rossing MA, Wicklund KG, Cushing-Haugen KL, Weiss NS (2010-01-28). "Predictive Value of Symptoms for Early Detection of Ovarian Cancer". J Natl Cancer Inst. 102 (4): 222–9. doi:10.1093/jnci/djp500. PMC 2826180. PMID 20110551.
Miller RW, Ueland FR (March 2012). "Risk of malignancy in sonographically confirmed ovarian tumors". Clinical Obstetrics and Gynecology. 55 (1): 52–64. doi:10.1097/GRF.0b013e31824970cf. PMID 22343229.
"Ovarian cancer tests". www.cancerresearchuk.org. Archived from the original on 2015-05-18. Retrieved 2015-05-16.
"Guideline CG122. Ovarian cancer: The recognition and initial management of ovarian cancer, Appendix D: Risk of malignancy index (RMI I)". NICE clinical guidelines. April 2011. Archived from the original on 2013-09-22.
Geomini, Peggy; Kruitwagen, Roy; Bremer, Gérard L.; Cnossen, Jeltsje; Mol, Ben W. J. (Feb 2009). "The accuracy of risk scores in predicting ovarian malignancy: a systematic review". Obstetrics and Gynecology. 113 (2 Pt 1): 384–394. doi:10.1097/AOG.0b013e318195ad17. ISSN 0029-7844. PMID 19155910.
Kaijser, Jeroen; Bourne, Tom; De Rijdt, Sylvie; Van Holsbeke, Caroline; Sayasneh, Ahmad; Valentin, Lil; Van Calster, Ben; Timmerman, Dirk (August 2012). "Key findings from the International Ovarian Tumor Analysis (IOTA) study: an approach to the optimal ultrasound based characterisation of adnexal pathology". Australasian Journal of Ultrasound in Medicine. 15 (3): 82–86. doi:10.1002/j.2205-0140.2012.tb00011.x. ISSN 1836-6864. PMC 5025098. PMID 28191150.
Kosary, Carol L. (2007). "Chapter 16: Cancers of the Ovary" (PDF). In Baguio, RNL; Young, JL; Keel, GE; Eisner, MP; Lin, YD; Horner, M-J (eds.). SEER Survival Monograph: Cancer Survival Among Adults: US SEER Program, 1988–2001, Patient and Tumor Characteristics. SEER Program. NIH Pub. No. 07-6215. Bethesda, MD: National Cancer Institute. pp. 133–144. Archived from the original on 2013-10-10.
"Types of ovarian cancer". www.cancerresearchuk.org. Archived from the original on 2015-05-18. Retrieved 2015-05-16.
Levy, Gary; Purcell; Karen (2013). DeCherney, AH; Nathan, L; Laufer, N; et al. (eds.). Premalignant & Malignant Disorders of the Ovaries & Oviducts. CURRENT Diagnosis & Treatment: Obstetrics & Gynecology, 11e. McGraw-Hill. ISBN 978-0-07-163856-2. Archived from the original on 2017-09-10.
"Primary peritoneal carcinoma". www.cancerresearchuk.org. Archived from the original on 2015-05-20. Retrieved 2015-05-16.
"Ovarian Cancer Staging" (PDF). Society for Gynecologic Oncology. 1 January 2014. Archived (PDF) from the original on 5 November 2014.
"How is ovarian cancer staged?". American Cancer Society. Archived from the original on November 24, 2016. Retrieved June 17, 2017.
"Stages of ovarian cancer". www.cancerresearchuk.org. Archived from the original on 2015-05-18. Retrieved 2015-05-16.
Croswell JM, Brawley OW, Kramer BS (2012). "Prevention and Early Detection of Cancer". In Longo DL, Kasper DL, Jameson JL, Fauci AS, Hauser SL, Loscalzo J (eds.). Harrison's Principles of Internal Medicine (18th ed.). McGraw-Hill. ISBN 978-0-07-174889-6.
Cibula, D.; Widschwendter, M.; Majek, O.; Dusek, L. (2010). "Tubal ligation and the risk of ovarian cancer: review and meta-analysis". Human Reproduction Update. 17 (1): 55–67. doi:10.1093/humupd/dmq030. PMID 20634209.
"How Is Ovarian Cancer Treated?". Centers for Disease Control and Prevention. February 13, 2017. Archived from the original on June 16, 2017. Retrieved June 17, 2017. This article incorporates public domain material from websites or documents of the Centers for Disease Control and Prevention.
Marchetti, C; Pisano, C; Facchini, G (2010). "First line treatment of ovarian cancer: current research and perspectives". Expert Rev Anticancer Ther (10): 47–60.
"Types of treatment for ovarian cancer". www.cancerresearchuk.org. Archived from the original on 2015-05-12. Retrieved 2015-05-16.
"'Game-changing' drug for ovarian cancer approved on NHS". Retrieved 2019-07-26.
"Treatment of ovarian cancer". Canadian Cancer Society. Archived from the original on 26 October 2016. Retrieved 17 June 2017.
"Surgery for ovarian cancer". www.cancerresearchuk.org. Archived from the original on 2015-05-18. Retrieved 2015-05-16.
Falcetta, Frederico S.; Lawrie, Theresa A.; Medeiros, Lídia Rf; da Rosa, Maria Ines; Edelweiss, Maria I.; Stein, Airton T.; Zelmanowicz, Alice; Moraes, Anaelena B.; Zanini, Roselaine R. (2016-10-13). "Laparoscopy versus laparotomy for FIGO stage I ovarian cancer". The Cochrane Database of Systematic Reviews. 10: CD005344. doi:10.1002/14651858.CD005344.pub4. ISSN 1469-493X. PMID 27737492.
"Drugs used for ovarian cancer". www.cancerresearchuk.org. Archived from the original on 2015-05-18. Retrieved 2015-05-16.
Yao, Stephanie (19 December 2014). "FDA approves Lynparza to treat advanced ovarian cancer: First LDT companion diagnostic test also approved to identify appropriate patients". U.S. Food and Drug Administration. Archived from the original on 14 September 2015.
"Radiotherapy for ovarian cancer". www.cancerresearchuk.org. Archived from the original on 2015-05-18. Retrieved 2015-05-16.
"Ovarian cancer research". www.cancerresearchuk.org. Archived from the original on 2015-05-09. Retrieved 2015-05-16.
"Follow up for ovarian cancer". Cancer Research UK. 2017-08-30. Archived from the original on 2014-08-29.
Follow-up care Archived 2013-12-25 at the Wayback Machine from American Cancer Society. Last Medical Review: 03/21/2013. Last Revised: 02/06/2014
Society of Gynecologic Oncology (February 2014), "Five Things Physicians and Patients Should Question", Choosing Wisely: an initiative of the ABIM Foundation, Society of Gynecologic Oncology, archived from the original on 1 December 2013, retrieved 19 February 2013, which cites
Bhosale P, Peungjesada S, Wei W, Levenback CF, Schmeler K, Rohren E, Macapinlac HA, Iyer RB (August 2010). "Clinical Utility of Positron Emission Tomography/Computed Tomography in the Evaluation of Suspected Recurrent Ovarian Cancer in the Setting of Normal CA-125 Levels". International Journal of Gynecological Cancer. 20 (6): 936–944. doi:10.1111/IGC.0b013e3181e82a7f. PMID 20683399.
"Chemotherapy for ovarian cancer". www.cancerresearchuk.org. Archived from the original on 2015-05-18. Retrieved 2015-05-16.
"ASCO Provisional Clinical Opinion: The Integration of Palliative Care into Standard Oncology Care". ASCO. Archived from the original on 21 August 2014. Retrieved 20 August 2014.
"Treating advanced ovarian cancer". www.cancerresearchuk.org. Archived from the original on 2015-05-19. Retrieved 2015-05-16.
Roland, Katherine B.; Rodriguez, Juan L.; Patterson, Jennifer Rees; Trivers, Katrina F. (2013-11-01). "A literature review of the social and psychological needs of ovarian cancer survivors". Psycho-Oncology. 22 (11): 2408–2418. doi:10.1002/pon.3322. ISSN 1099-1611. PMID 23760742.
Watts, Sam; Prescott, Philip; Mason, Jessica; McLeod, Natalie; Lewith, George (2015-11-01). "Depression and anxiety in ovarian cancer: a systematic review and meta-analysis of prevalence rates". BMJ Open. 5 (11): e007618. doi:10.1136/bmjopen-2015-007618. ISSN 2044-6055. PMC 4679843. PMID 26621509.
"Survival rates for ovarian cancer, by stage". American Cancer Society. Archived from the original on 29 October 2014. Retrieved 29 October 2014.
"Statistics and outlook for ovarian cancer". www.cancerresearchuk.org. Archived from the original on 2015-05-18. Retrieved 2015-05-16.
Survival rates based on SEER incidence and NCHS mortality statistics, as cited by the National Cancer Institute in SEER Stat Fact Sheets — Cancer of the Ovary Archived 2014-07-06 at the Wayback Machine
Gucalp R, Dutcher J (2012). "Oncologic Emergencies". In Longo DL, Kasper DL, Jameson JL, Fauci AS, Hauser SL, Loscalzo J (eds.). Harrison's Principles of Internal Medicine (18th ed.). McGraw-Hill. ISBN 978-0-07-174889-6.
"WHO Disease and injury country estimates". World Health Organization. 2009. Retrieved June 15, 2017. The statistics are from 2004. This weblink opens up with an automatic Excel file download
Lozano R, Naghavi M, Foreman K, Lim S, Shibuya K, Aboyans V, Abraham J, Adair T, Aggarwal R, Ahn SY, et al. (15 December 2012). "Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010". Lancet. 380 (9859): 2095–128. doi:10.1016/S0140-6736(12)61728-0. PMID 23245604.
Ramirez, Pedro T.; Gershenson, David M. (September 2013). "Ovarian Cancer". The Merck Manual for Health Care Professionals.open access
"Ovarian cancer statistics". Cancer Research UK. Archived from the original on 6 October 2014. Retrieved 28 October 2014.
Hennessy, Bryan T.; Suh, Grace K.; Markman, Maurie (2011). Kantarjian, HM; Wolff, RA; Koller, CA (eds.). Ovarian Cancer. The MD Anderson Manual of Medical Oncology (2e ed.). McGraw-Hill. ISBN 978-0-07-170106-8. Archived from the original on 2017-09-10.
Catone G, Marino G, Mancuso R, Zanghì A (April 2004). "Clinicopathological features of an equine ovarian teratoma". Reprod. Domest. Anim. 39 (2): 65–9. doi:10.1111/j.1439-0531.2003.00476.x. PMID 15065985.
Lefebvre R, Theoret C, Doré M, Girard C, Laverty S, Vaillancourt D (November 2005). "Ovarian teratoma and endometritis in a mare". Can. Vet. J. 46 (11): 1029–33. PMC 1259148. PMID 16363331.
Son YS, Lee CS, Jeong WI, Hong IH, Park SJ, Kim TH, Cho EM, Park TI, Jeong KS (May 2005). "Cystadenocarcinoma in the ovary of a Thoroughbred mare". Aust. Vet. J. 83 (5): 283–4. doi:10.1111/j.1751-0813.2005.tb12740.x. PMID 15957389.
Frederico LM, Gerard MP, Pinto CR, Gradil CM (May 2007). "Bilateral occurrence of granulosa-theca cell tumors in an Arabian mare". Can. Vet. J. 48 (5): 502–5. PMC 1852596. PMID 17542368.
Hoque S, Derar RI, Osawa T, Taya K, Watanabe G, Miyake Y (June 2003). "Spontaneous repair of the atrophic contralateral ovary without ovariectomy in the case of a granulosa theca cell tumor (GTCT) affected mare". J. Vet. Med. Sci. 65 (6): 749–51. doi:10.1292/jvms.65.749. PMID 12867740.
Sedrish SA, McClure JR, Pinto C, Oliver J, Burba DJ (November 1997). "Ovarian torsion associated with granulosa-theca cell tumor in a mare". J. Am. Vet. Med. Assoc. 211 (9): 1152–4. PMID 9364230.
Moll HD, Slone DE, Juzwiak JS, Garrett PD (1987). "Diagonal paramedian approach for removal of ovarian tumors in the mare". Vet Surg. 16 (6): 456–8. doi:10.1111/j.1532-950X.1987.tb00987.x. PMID 3507181. Archived from the original on 2012-10-10.
Doran R, Allen D, Gordon B (January 1988). "Use of stapling instruments to aid in the removal of ovarian tumours in mares". Equine Vet. J. 20 (1): 37–40. doi:10.1111/j.2042-3306.1988.tb01450.x. PMID 2835223.
Gizzo, Salvatore; Noventa, Marco; Quaranta, Michela; Vitagliano, Amerigo; Saccardi, Carlo; Litta, Pietro; Antona, Donato (2016). "A novel hysteroscopic approach for ovarian cancer screening/early diagnosis (Review)". Oncology Letters. 13 (2): 549–553. doi:10.3892/ol.2016.5493. PMC 5351187. PMID 28356928. subscription required
Jacobs IJ, Menon U, Ryan A, Gentry-Maharaj A, Burnell M, Kalsi JK, Amso NN, Apostolidou S, Benjamin E, Cruickshank D, Crump DN, Davies SK, Dawnay A, Dobbs S, Fletcher G, Ford J, Godfrey K, Gunu R, Habib M, Hallett R, Herod J, Jenkins H, Karpinskyj C, Leeson S, Lewis SJ, Liston WR, Lopes A, Mould T, Murdoch J, Oram D, Rabideau DJ, Reynolds K, Scott I, Seif MW, Sharma A, Singh N, Taylor J, Warburton F, Widschwendter M, Williamson K, Woolas R, Fallowfield L, McGuire AJ, Campbell S, Parmar M, Skates SJ (2016). "Ovarian cancer screening and mortality in the UK Collaborative Trial of Ovarian Cancer Screening (UKCTOCS): a randomised controlled trial". Lancet. 387 (10022): 945–56. doi:10.1016/S0140-6736(15)01224-6. PMC 4779792. PMID 26707054.
Paijens ST, Leffers N, Daemen T, Helfrich W, Boezen HM, Cohlen BJ, Melief CJ, de Bruyn M, Nijman HW (September 2018). "Antigen-specific active immunotherapy for ovarian cancer". Cochrane Database Syst Rev. 9: CD007287. doi:10.1002/14651858.CD007287.pub4. PMID 30199097.
Ingerslev, Kasper; Hogdall, Estrid; Schnack, Tine Henrichsen; Skovrider-Ruminski, Wojciech; Hogdall, Claus; Blaakaer, Jan (2017). "The potential role of infectious agents and pelvic inflammatory disease in ovarian carcinogenesis". Infectious Agents and Cancer. 12 (1): 25. doi:10.1186/s13027-017-0134-9. ISSN 1750-9378. PMC 5437405. PMID 28529540.
"NIH Clinical Research Trials and You". Archived from the original on 8 June 2017. Retrieved 17 June 2017.
"Clinical Trials Information for Patients and Caregivers". National Cancer Institute. Archived from the original on 16 June 2017. Retrieved 17 June 2017.
"Find NCI-Supported Clinical Trials". National Cancer Institute. 2016-06-23. Archived from the original on 1 July 2017. Retrieved 17 June 2017.
"Home — ClinicalTrials.gov". www.clinicaltrials.gov. Archived from the original on 16 June 2017. Retrieved 17 June 2017.
"Home - Canadian Cancer Trials". www.canadiancancertrials.ca. Archived from the original on 26 June 2017. Retrieved 17 June 2017. |