小脑(拉丁语为“小脑”)是所有脊椎动物后脑的主要特征。虽然通常比大脑小,但在一些动物如mormyrid鱼类中它可能大到甚至更大。[1]在人类中,小脑在运动控制中起重要作用。它也可能涉及一些认知功能,如注意力和语言,以及调节恐惧和快乐反应,[2]但其运动相关的功能是最稳固的。人类小脑不会引发运动,但有助于协调,精确和准确的计时:它接收来自脊髓感觉系统和大脑其他部分的输入,并整合这些输入以微调运动活动。[3 ]小脑损伤会导致人类精细运动,平衡,姿势和运动学习障碍。[3]
在解剖学上,人类小脑具有附着于大脑底部的独立结构的外观,隐藏在大脑半球的下方。它的皮质表面覆盖着精细间隔的平行凹槽,与大脑皮质的宽广不规则旋圈形成鲜明对比。这些平行凹槽掩盖了这样的事实:小脑皮层实际上是一个连续的薄层组织,紧密折叠成手风琴式。在这个薄层内有几种类型的神经元,具有高度规则的排列,最重要的是浦肯野细胞和颗粒细胞。这种复杂的神经组织产生了巨大的信号处理能力,但几乎所有来自小脑皮层的输出都通过位于小脑白质内部的一组小的深核。[4]
除了在运动控制中的直接作用外,小脑对于几种类型的运动学习是必要的,最明显的是学习如何适应感觉运动关系的变化。已经开发了几种理论模型来解释在小脑内突触可塑性方面的感觉运动校准。这些模型来自David Marr和James Albus制定的模型,基于观察到每个小脑浦肯野细胞接受两种截然不同的输入类型:一种包含来自颗粒细胞的平行纤维的数千个弱输入;另一种是来自单根攀爬纤维的极强输入。[5] Marr-Albus理论的基本概念是攀爬纤维作为“教学信号”,引起平行纤维输入强度的持久变化。平行纤维输入中长期抑郁症的观察结果为这类理论提供了支持,但其有效性仍存在争议。[6]
视频:↓ 2分钟神经科学_小脑
https://cache.tv.qq.com/qqplayerout.swf?vid=s0868ac202z
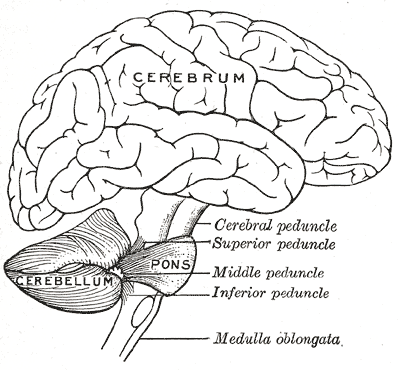
绘制的人类大脑,显示小脑和脑桥
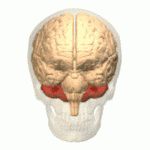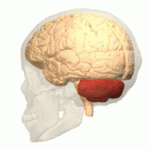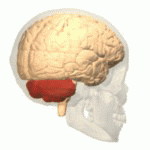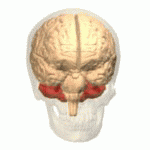
人类小脑的位置(红色)
目录
1 结构
1.1 大体解剖学
1.2 显微解剖
2 功能
2.1 原则
2.2 学习
2.3 理论和计算模型
3 血液供应
4 临床意义
4.1 老化
4.2 发育和退行性疾病
4.3 疼痛
5 比较解剖和进化
5.1 小脑样结构
6 历史
6.1 说明
6.2 词源
7 参考
结构
主要文章:小脑解剖学
在大体解剖学水平上,小脑由紧密折叠的皮层组成,下面是白质,底部是充满液体的心室。四个深小脑核嵌入白质中。皮质的每个部分由相同的一小组神经元组成,以高度刻板的几何形状排列。在中间水平,小脑及其辅助结构可以被分成几十万个独立的功能模块,称为“微区”或“微室”。
大体解剖
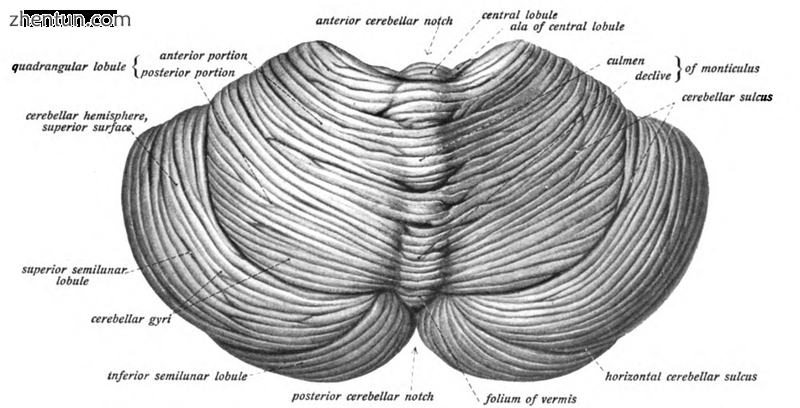
从上面和后面的小脑的视图
小脑位于后颅窝。第四脑室,脑桥和髓质位于小脑前方。[7]它与上覆的大脑分开一层革质硬脑膜,即小脑幕;它与大脑其他部分的所有联系都通过脑桥。解剖学家将小脑分类为脑膜的一部分,其中还包括脑桥;脑膜是菱形脑或“后脑”的上半部分。像大脑皮层一样,小脑分为两个半球;它还包含一个狭窄的中线区域(蚓部)。按照惯例,一组大褶皱用于将整体结构分成10个较小的“小叶”。由于其大量的微小颗粒细胞,小脑包含的神经元数量超过了大脑其他部分的总数,但只占总脑容量的10%。[8]小脑中神经元的数量与新皮质中神经元的数量有关。小脑中的神经元数量是新皮质的3.6倍,这一比例在许多不同的哺乳动物物种中是保守的。[9]
小脑不寻常的表面外观掩盖了这样一个事实,即它的大部分体积都由一个非常紧密折叠的灰质层组成:小脑皮层。该层中的每个脊或脑都称为叶。据估计,如果人类小脑皮层完全展开,它将产生一层约1米长的神经组织,平均宽度为5厘米 - 总表面积约为500平方厘米,包装在一定体积的尺寸内6厘米×5厘米×10厘米。[8]在皮质的灰质下面是白质,主要由有髓神经纤维组成,进出皮质。嵌入白质中 - 有时被称为乔木(生命之树),因为它的横截面呈分枝状,树状外观 - 是由灰质组成的四个深小脑核。[10]
将小脑连接到神经系统的不同部位是三对小脑脚。这些是优越的小脑花梗,中小脑花梗和小脑下部花梗,以它们相对于蚓部的位置命名。小脑上部的小脑主要是大脑皮层的输出,通过丘脑核向大脑皮层的上运动神经元传递传出纤维。纤维来自深小脑核。中间小脑的花梗与脑桥连接,并且主要从脑桥核接收来自脑桥的所有输入。对脑桥的输入来自大脑皮层,并通过横向脑桥纤维从脑桥核传递到小脑。中间的花序梗是三者中最大的,它的传入纤维被分成三个独立的分支,将它们的输入带到小脑的不同部位。下小脑梗接受来自前庭核,脊髓和被盖的传入纤维的输入。下足的输出是通过传出纤维到前庭核和网状结构。整个小脑通过下小脑脚接受来自下橄榄核的调节输入。[4]
细分
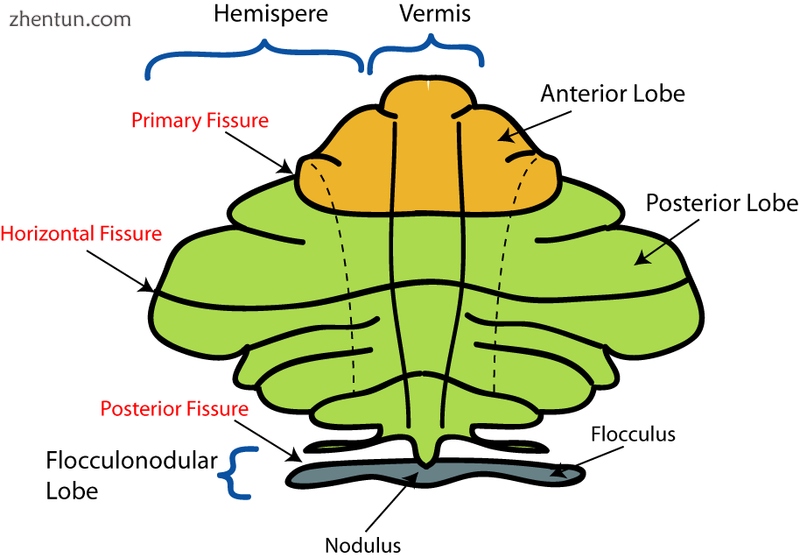
小脑主要解剖学细分的示意图。 “展开”小脑的优越视图,将蚓部放在一个平面上。
根据表面外观,可以在小脑内区分出三个叶:前叶(主裂缝上方),后叶(主裂缝下方)和絮状结节叶(后裂缝下方)。这些裂片将小脑从嘴侧到尾侧(人类,从上到下)分开。然而,就功能而言,沿着内侧到外侧的维度存在更重要的区别。留下具有明显连接和功能的絮状结节叶,小脑可在功能上解析为一个称为脊髓小脑的内侧部分和一个更大的侧脑室,称为脑小脑。[10]沿中线的狭窄条带突出组织称为小脑蚓部。 (Vermis是拉丁文的“蠕虫”。)[10]
最小的区域,即絮状结节叶,通常被称为前庭小脑。它是进化术语(archicerebellum)中最古老的部分,主要参与平衡和空间定位;它的主要连接是前庭核,虽然它也接收视觉和其他感觉输入。对该区域的伤害会导致平衡和步态的干扰。[10]
前叶和后叶的内侧区域构成脊髓小脑,也称为古脑小脑。小脑的这个部分主要用于微调身体和肢体运动。它接受来自脊髓背侧(包括脊髓小脑束)和颅三叉神经以及视觉和听觉系统的本体感受输入。它将纤维传递到深小脑核,然后进入大脑皮层和脑干,从而调节下行运动系统。[10]
横向区域,在人类中是迄今为止最大的部分,构成脑小脑,也称为新脑小脑。它通过脑桥核(形成皮质 - 小脑 - 小脑通路)专门从大脑皮层(特别是顶叶)接收输入,并且主要将输出发送到腹外侧丘脑(进而连接到前运动皮层和初级运动的运动区域)大脑皮层区域和红核。[10]关于描述侧小脑功能的最佳方式存在分歧:人们认为它涉及计划即将发生的运动,[11]在评估行动的感觉信息时,[10]以及一些纯粹的认知功能,例如确定最适合某个名词的动词(如“坐”为“椅子”)。[12] [13] [14] [15]
显微解剖
两种类型的神经元在小脑回路中起主要作用:浦肯野细胞和颗粒细胞。三种类型的轴突也起主要作用:苔藓纤维和攀缘纤维(从外部进入小脑)和平行纤维(它们是颗粒细胞的轴突)。小脑回路有两条主要通路,源自苔藓纤维和攀缘纤维,最终都终止于深小脑核。[8]
苔藓纤维直接投射到深核,但也产生以下途径:苔藓纤维→颗粒细胞→平行纤维→浦肯野细胞→深核。攀缘纤维向Purkinje细胞投射,并将侧枝直接传递到深部核。[8]苔藓纤维和攀爬纤维输入每个都带有纤维特定的信息;小脑还接受多巴胺能,5-羟色胺能,去甲肾上腺素能和胆碱能输入,可能会进行全局调节。[16]
小脑皮层分为三层。在底部是厚的颗粒层,密集的颗粒细胞,以及中间神经元,主要是高尔基细胞,但也包括Lugaro细胞和单极刷细胞。 Purkinje层位于中间,是一个狭窄的区域,包含浦肯野细胞和Bergmann神经胶质细胞的细胞体。顶部是分子层,其中包含浦肯野细胞的扁平树枝状系统,以及大量平行纤维以直角穿透浦肯野细胞树枝状树木。小脑皮层的最外层还含有两种类型的抑制性中间神经元:星状细胞和篮细胞。星状细胞和篮细胞在Purkinje细胞树突上形成GABA能神经突触。[8]
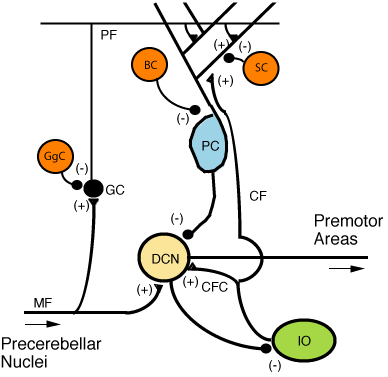
小脑微电路
缩写和表示
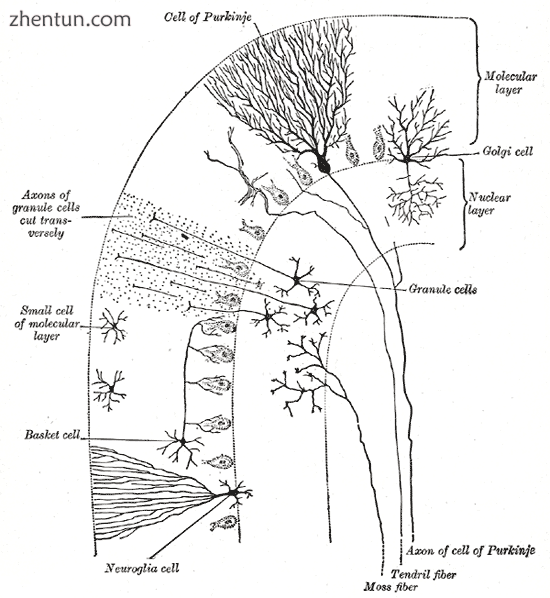
小脑叶的横切面,显示主要的细胞类型和连接
浦肯野细胞
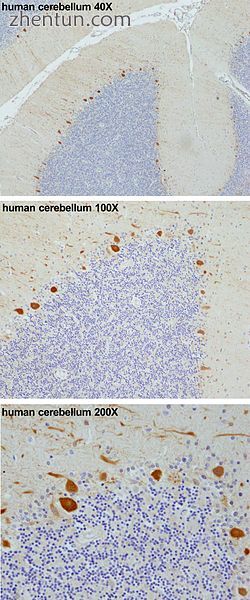
人类小脑中的浦肯野细胞(橙色,从上到下40倍,100倍和200倍放大)根据已发表的方法染色[17]
浦肯野细胞是大脑中最独特的神经元之一,也是最早被认可的类型之一 - 它们最早由捷克解剖学家JanEvangelistaPurkyně于1837年描述。它们以树枝状树的形状为特征:树枝状枝非常丰富,但在垂直于小脑褶皱的平面上严重变平。因此,浦肯野细胞的树突形成一个致密的平面网,平行纤维以直角通过。[8]树突上覆盖着树突棘,每个树枝刺都接收来自平行纤维的突触输入。 Purkinje细胞比大脑中任何其他类型的细胞接受更多的突触输入 - 估计单个人Purkinje细胞上的刺数量高达200,000 [8]。浦肯野细胞的大的球形细胞体被包装成小脑皮质的狭窄层(一个细胞厚),称为浦肯野层。在发射影响皮层附近部分的侧枝后,它们的轴突进入深小脑核,在那里它们产生大约1000个接触,每个接触具有几种类型的核细胞,所有这些都在一个小的区域内。 Purkinje细胞使用GABA作为其神经递质,因此对其靶标发挥抑制作用。[8]
浦肯野细胞形成小脑回路的核心,它们的大尺寸和独特的活动模式使得使用细胞外记录技术研究它们在行为动物中的反应模式相对容易。即使在没有突触输入的情况下,浦肯野细胞通常也以高速率发射动作电位。在清醒的表现动物中,平均大约40赫兹的平均速率是典型的。穗列车显示出所谓的简单和复杂尖峰的混合物。一个简单的尖峰是一个动作电位,然后是一个约10毫秒的不应期;复杂的尖峰是一种刻板的动作电位序列,具有非常短的尖峰间隔和不断下降的振幅。[18]生理学研究表明,复杂的尖峰(以1Hz左右的基线速率发生,绝不会高于10Hz的速率)与攀爬光纤激活可靠地相关联,而基线活动和平行光纤输入的组合产生简单的尖峰。复杂的峰值之后通常会暂停几百毫秒,在此期间可以抑制简单的尖峰活动。[19]
Purkinje神经元的一个特定的,可识别的特征是calbindin的表达。[20]单侧慢性坐骨神经损伤后大鼠脑的钙结合蛋白染色表明,Purkinje神经元可能在成人大脑中新生成,开始组织新的小脑小叶。[21]
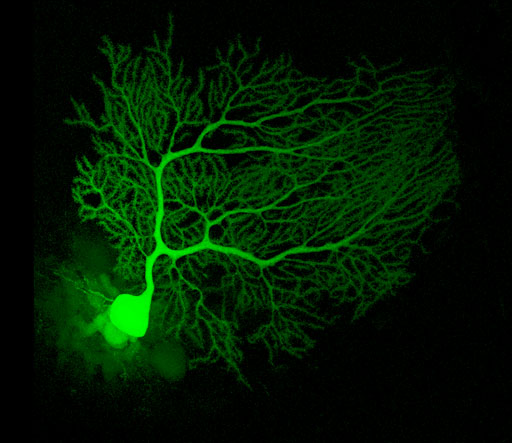
注射荧光染料的小鼠浦肯野细胞
颗粒细胞
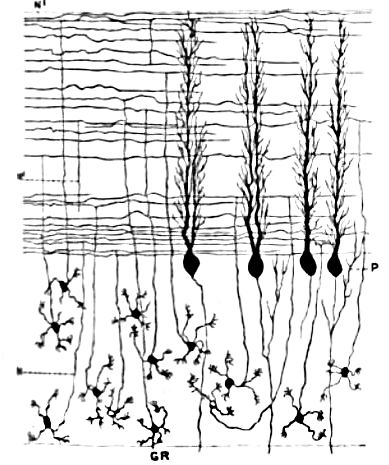
颗粒细胞(GR,底部),平行纤维(水平线,顶部)和Purkinje细胞(P,中部),具有扁平的树枝状树
与Purkinje细胞相反,小脑颗粒细胞是大脑中最小的神经元之一。它们也很容易成为大脑中最多的神经元:在人类中,估计它们的总数平均约为500亿,这意味着大约3/4的大脑神经元是小脑颗粒细胞。[8]它们的细胞体被包裹在小脑皮质底部的厚层中。颗粒细胞仅发出四到五个树突,每个树突以称为树枝状爪的扩大结束。[8]这些扩大是苔藓纤维的兴奋性输入和高尔基细胞抑制性输入的部位。[8]
颗粒细胞的薄的,无髓鞘的轴突垂直上升到皮层的上(分子)层,在那里它们分成两部分,每个分支水平移动形成平行纤维;将垂直分支分成两个水平分支,产生独特的“T”形状。人体平行纤维在分裂的每个方向上平均运行3毫米,总长度约为6毫米(约为皮质层总宽度的1/10)。[8]当它们一起运行时,平行纤维穿过浦肯野细胞的树枝状树木,接触它们经过的3-5个中的一个,与浦肯野细胞树突棘共有80-100个突触连接。[8]颗粒细胞使用谷氨酸作为其神经递质,因此对其靶标产生兴奋作用。[8]
颗粒细胞从苔藓纤维中获得所有输入,但是数量超过200比1(在人类中)。因此,颗粒细胞群活动状态中的信息与苔藓纤维中的信息相同,但以更广泛的方式重新编码。由于颗粒细胞如此小且密集,因此很难在行为动物中记录其穗活动,因此几乎没有数据可用作理论化的基础。最受欢迎的功能概念是由David Marr在1969年提出的,他建议他们可以对苔藓纤维输入的组合进行编码。这个想法是,每个颗粒细胞只接受4-5根苔藓纤维的输入,如果只有一个输入是活跃的,颗粒细胞就不会响应,但如果有多个输入是活跃的,它会响应。这种组合编码方案可能允许小脑在输入模式之间进行更细微的区分,而不仅仅是苔藓纤维所允许的。[22]
苔藓纤维
苔藓纤维从其起源点进入颗粒层,许多来自脑桥核,其他来自脊髓,前庭核等。在人类小脑中,苔藓纤维的总数估计约为2亿[8]。 ]这些纤维与颗粒细胞和深小脑细胞核形成兴奋性突触。在颗粒层内,苔藓纤维产生一系列称为玫瑰花结的放大物。苔藓纤维和颗粒细胞树突之间的接触发生在称为肾小球的结构内。每个肾小球的中心都有一个长满苔藓的纤维莲座丛,最多20个颗粒状细胞树枝状爪与它接触。来自高尔基体细胞的末端渗入结构并在颗粒细胞树突上产生抑制性突触。整个组合被神经胶质细胞包围。[8]每根苔藓纤维将侧枝分支发送到几个小脑叶片,产生总共20-30个玫瑰花结;因此,单根苔藓纤维与估计的400-600颗粒细胞接触。[8]
攀爬纤维
浦肯野细胞还通过攀爬纤维接收来自脑干对侧的下橄榄核的输入。虽然下部橄榄位于延髓中并且接受来自脊髓,脑干和大脑皮层的输入,但其输出完全进入小脑。攀爬纤维在进入小脑皮质之前向深小脑核发出侧支,在那里它分裂成大约10个末端分支,每个分支为单个浦肯野细胞提供输入。[8]与平行光纤的100,000多输入形成鲜明对比的是,每个Purkinje单元都接收来自一根攀爬光纤的输入;但这条单根纤维“攀爬”浦肯野细胞的树突,缠绕在它们周围,最多可形成300个突触。[8]净输入是如此之强,以至于攀爬光纤的单一动作电位能够在浦肯野细胞中产生延长的复杂尖峰:连续几次尖峰突发,幅度减小,然后暂停,在此期间活动被抑制。攀缘纤维突触覆盖细胞体和近端树突;这个区域没有平行光纤输入。[8]
爬升纤维以低速率发射,但单个攀爬纤维动作电位在目标浦肯野细胞(复杂的尖峰)中引起几个动作电位的爆发。浦肯野细胞的平行纤维和攀爬纤维输入之间的对比(一种类型超过100,000种而非另一种类型)可能是小脑解剖学中最具挑衅性的特征,并且推动了大部分理论化。事实上,攀爬纤维的功能是关于小脑的最有争议的话题。有两种思想流派,其中一种是Marr和Albus认为攀爬纤维输入主要用作教学信号,另一种认为其功能是直接塑造小脑输出。许多出版物都对这两种观点进行了长时间的辩护。用一篇评论的话来说,“在试图综合关于攀爬纤维功能的各种假设时,人们有一种看待埃舍尔绘画的感觉。每个观点似乎都是某些研究结果的集合,但是当人们尝试将不同的视图放在一起时,就不会出现攀爬光纤正在做什么的连贯画面。对于大多数研究人员来说,攀爬光纤通过放电频率调制的常规方式或者以通常的方式表示运动性能的误差。一个“突发事件”的单一宣告。对于其他调查人员来说,信息在于攀爬纤维群体的整体同步和节奏程度。“[19]
深核
主要文章:深小脑核
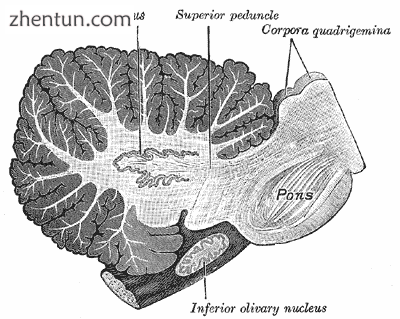
人小脑的矢状横截面,显示齿状核,以及脑桥和下橄榄核
小脑的深核是位于小脑核心的白质内的灰质簇。除了附近的前庭核外,它们是小脑输出的唯一来源。这些细胞核受到来自苔藓纤维和攀缘纤维的附带投射以及来自小脑皮层浦肯野细胞的抑制性输入。四个核(齿状,球状,栓状和顶端)各自与大脑和小脑皮质的不同部分相通。 (球状核和栓塞核也称为在插入的核中组合)。小脑和插入的细胞核属于脊髓小脑。齿状核在哺乳动物中比其它的大得多,形成为一层薄而复杂的灰质层,并且仅与小脑皮质的外侧部分相通。絮状结节叶是小脑皮质中唯一不会向深核突出的部分 - 它的输出会转移到前庭核。[8]
深核中的大多数神经元具有大的细胞体和半径为约400μm的球形树突树,并且使用谷氨酸作为它们的神经递质。这些细胞投射到小脑外的各种目标。与它们混合的是较少数量的小细胞,其使用GABA作为神经递质并且专门用于下部橄榄核,即攀爬纤维的来源。因此,核 - 橄榄形投影提供抑制反馈以匹配攀爬纤维对细胞核的兴奋性投射。有证据表明,每个小核细胞簇都投射到同一组橄榄细胞上,这些橄榄细胞将攀爬纤维传递给它;两个方向都有强大而匹配的地形。[8]
当浦肯野细胞轴突进入深核之一时,它分支与大核小细胞和小核细胞接触,但接触的细胞总数仅约35只(在猫中)。相反,单个深核细胞接收来自大约860个浦肯野细胞的输入(再次在猫中)。[8]
隔室
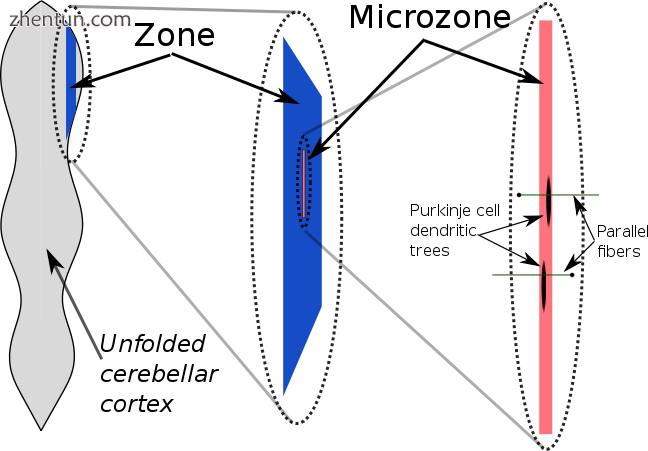
小脑皮层区域和微区结构的示意图
从大体解剖学的角度来看,小脑皮质看起来是均匀的组织片,并且从显微解剖学的观点来看,该片的所有部分看起来具有相同的内部结构。然而,在许多方面,小脑的结构被划分。有大的隔间通常被称为区域;这些可以分为较小的区域,称为微区。[23]
区室结构的第一个迹象来自对小脑皮层不同部位细胞的感受区的研究。[23]每个身体部位都映射到小脑中的特定点,但是基本地图有很多重复,形成了一种被称为“破碎的生长”的安排。[24]通过对小脑免疫染色某些类型的蛋白质,可以获得更明确的区室化指示。这些标记中最着名的被称为“zebrins”,因为它们的染色会产生一种复杂的图案,让人联想到斑马上的条纹。由zebrins和其他区室化标记产生的条纹垂直于小脑褶皱定向 - 也就是说,它们在中间方向上是窄的,但在纵向方向上更加延伸。不同的标记产生不同的条纹组,宽度和长度随位置而变化,但它们都具有相同的一般形状。[23]
20世纪70年代后期的奥斯卡森提出,这些皮层区域可以划分为更小的单位,称为微区。[25]微区被定义为一组浦肯野细胞,它们都具有相同的躯体感受野。微区被发现每个包含1000个Purkinje细胞,排列成一条长而窄的条带,垂直于皮质褶皱。[23]因此,如相邻图所示,浦肯野细胞枝晶在与微区延伸的方向相同的方向上变平,而平行纤维以直角交叉它们。[8]
不仅是定义微区结构的感受野:来自下橄榄核的攀爬纤维输入同样重要。攀爬纤维的分支(通常约10个)通常激活属于同一微区的浦肯野细胞。此外,将攀爬纤维送到同一微区的橄榄核神经元倾向于通过间隙连接耦合,这使得它们的活动同步,导致微区内的浦肯野细胞在毫秒时间尺度上显示相关的复杂尖峰活动。[23]此外,属于微区的浦肯野细胞都将它们的轴突送到深小脑核内的同一小组输出细胞中。[23]最后,篮细胞的轴突在纵向方向上比在中间方向上长得多,导致它们主要局限于单个微区。[23]所有这些结构的结果是微区内的细胞相互作用比不同微区之间的相互作用强得多。[23]
2005年,Richard Apps和Martin Garwicz总结证据表明微区本身是一个更大的实体的一部分,他们称之为多区域微复杂。这样的微复合体包括几个空间上分离的皮质微区,所有这些微区都投射到同一组深小脑神经元,加上一组耦合的橄榄核神经元投射到所有包含的微区以及深核区域。[23]
功能
小脑功能的最强线索来自于检查其损伤的后果。具有小脑功能障碍的动物和人类首先表现出与小脑受损部位在身体同侧的运动控制问题。它们继续能够产生运动活动但却失去精确度,产生不稳定,不协调或不正确的定时运动。小脑功能的标准测试是用手指的尖端到达手臂的目标:健康的人将以快速的直线轨迹移动指尖,而患有小脑损伤的人将缓慢且不规律地到达,许多中期 - 纠正。非运动功能中的缺陷更难以检测。因此,几十年前达成的一般结论是,小脑的基本功能是校准运动的详细形式,而不是启动运动或决定执行哪些运动。[10]
在20世纪90年代之前,小脑的功能几乎普遍被认为纯粹与运动相关,但较新的发现使这种观点受到质疑。功能成像研究表明,与语言,注意力和心理意象相关的小脑激活;相关性研究显示大脑皮质的小脑和非运动区域之间的相互作用;并且在似乎仅限于小脑的损伤患者中已经识别出各种非运动症状。[26] [27]特别是小脑认知情感综合征或Schmahmann综合征[28]已在成人[29]和儿童[30]中有所描述。基于使用功能性MRI的小脑功能映射的估计表明,超过一半的小脑皮质与大脑皮质的关联区相互连接。[31]
Kenji Doya认为小脑的功能最好不是根据它影响的行为来理解,而是它所执行的神经计算;小脑由大量或多或少独立的模块组成,所有模块都具有相同的几何规则内部结构,因此假定所有模块执行相同的计算。如果模块的输入和输出连接与电机区域(尽可能多),则模块将参与电机行为;但是,如果连接涉及非运动认知的区域,则模块将显示其他类型的行为相关性。因此,小脑涉及许多不同功能特征的调节,如情感,情感和行为。[32] [33] Doya提出的小脑最好被理解为基于环境的“内部模型”或监督学习装置的预测行动选择,与执行强化学习的基底神经节和执行无监督学习的大脑皮层相反。 [27] [34]
原则
小脑解剖学的比较简单性和规律性导致了早期的希望,它可能意味着计算功能的类似简单性,正如在小脑电生理学的第一本书中所表达的那样,作为神经元机器的小脑由John C. Eccles,Masao表达。 Ito和JánosSzentágothai。[35]虽然对小脑功能的充分理解仍然难以捉摸,但至少有四个原则被认为是重要的:(1)前馈处理,(2)分歧和收敛,(3)模块化,以及(4)可塑性。
前馈处理:小脑与大脑的其他部分(特别是大脑皮层)的区别在于,信号处理几乎完全是前馈的 - 也就是说,信号从输入到输出单向地通过系统移动,内部传输很少。确实存在的少量复发包括相互抑制;没有相互兴奋的电路。这种前馈操作模式意味着与大脑皮层相比,小脑不能产生自我维持的神经活动模式。信号进入电路,按顺序由每个阶段处理,然后离开。正如Eccles,Ito和Szentágothai写道的那样,“设计神经元激发反射链的所有可能性的这种消除无疑是小脑作为计算机表现的一个巨大优势,因为神经系统的其他部分需要来自小脑可能不是表达小脑中复杂反射电路操作的一些输出,而是对任何特定信息集的输入作出快速而明确的反应。“[36]
分歧和收敛:在人类小脑中,来自2亿个苔藓纤维输入的信息被扩展到400亿个颗粒细胞,其平行纤维输出然后会聚到1500万个浦肯野细胞上。[8]由于它们纵向排列的方式,属于微区的1000个左右的浦肯野细胞可以接收多达1亿个平行纤维的输入,并将它们自己的输出集中到一组小于50个深的核细胞。 [23]因此,小脑网络接收适量的输入,通过其严格结构的内部网络非常广泛地处理它们,并通过非常有限数量的输出单元发送结果。
模块化:小脑系统在功能上被划分为或多或少独立的模块,其数量可能达到数百到数千。所有模块都具有类似的内部结构,但输入和输出不同。一个模块(Apps和Garwicz术语中的多区域微区)由下橄榄核中的一小组神经元,小脑皮质中的一组长的Purkinje细胞(微区)和一小群神经元组成。在一个深小脑核。不同的模块共享来自苔藓纤维和平行纤维的输入,但在其他方面它们似乎独立运作 - 一个模块的输出似乎不会显着影响其他模块的活动。[23]
可塑性:平行纤维和浦肯野细胞之间的突触,以及苔藓纤维和深核细胞之间的突触,都易于改变其强度。在单个小脑模块中,来自多达十亿个平行纤维的输入会聚到一组小于50个深的核细胞上,并且每个平行纤维对这些核细胞的影响是可调节的。这种安排为微调小脑输入和输出之间的关系提供了极大的灵活性。[37]
学习
有大量证据表明小脑在某些类型的运动学习中起着重要作用。小脑最明显发挥作用的任务是必须对行动方式进行微调。然而,关于学习是否发生在小脑本身,或者它是否仅仅用于提供促进其他大脑结构学习的信号,存在很多争议。[37]将大脑电路学习分配的大多数理论都源于David Marr [22]和James Albus [5]的观点,他们假设攀爬纤维提供了一种教导信号,可诱导平行纤维 - 浦肯野细胞突触的突触修饰。 [38] Marr假设攀爬光纤输入会导致同步激活的并行光纤输入得到加强。然而,大多数随后的小脑学习模型都遵循Albus假设攀爬纤维活动将是一个误差信号,并且会导致同步激活的平行光纤输入被削弱。其中一些后来的模型,如Fujita [39]的自适应滤波器模型,尝试用最优控制理论来理解小脑功能。
在许多实验研究中已经研究了攀爬纤维活动作为误差信号的想法,有些人支持它,但其他人则怀疑。[19]在Gilbert和Thach从1977年进行的一项开创性研究中,来自猴子的Purkinje细胞学习到达任务表明复杂的尖峰活动 - 已知能够可靠地指示细胞攀爬纤维输入的活动 - 在表现不佳的时期。[40]对于猫的运动学习的一些研究观察到当预期的运动与实际执行的运动之间存在不匹配时的复杂的尖峰活动。对前庭眼反射的研究(当头部转动时稳定视网膜上的视觉图像)发现攀爬纤维活动表明“视网膜滑动”,尽管不是非常直接的方式。[19]
最广泛研究的小脑学习任务之一是眨眼调节范例,其中中性条件刺激(CS)(例如音调或光)与无条件刺激(US)重复配对,例如吹气,引发眨眼反应。在对CS和US进行如此反复的介绍之后,CS最终将在US之前引发眨眼,条件反应或CR。实验表明,局限于插入的细胞核(小脑深层核之一)或小脑皮质中的一些特定点的病变将消除对条件定时眨眼反应的学习。如果小脑输出在药理学上失活,同时使输入和细胞内回路保持完整,即使动物未能显示任何反应也会发生学习,而如果小脑内电路中断,则不会发生任何学习 - 这些事实合在一起构成了一个强有力的证据。事实上,学习发生在小脑内部。[41]
理论和计算模型
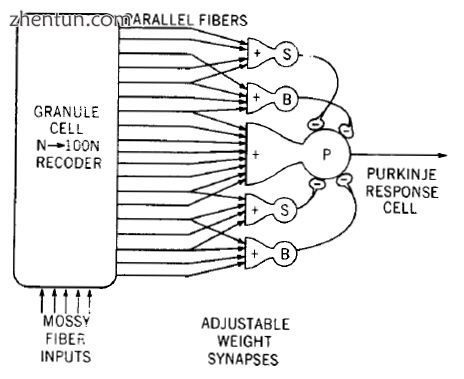
由James Albus制定的小脑感知器模型
关于小脑的解剖结构和行为功能的大量知识使其成为理论化的肥沃土壤 - 可能有更多关于小脑功能的理论而不是大脑的任何其他部分。它们之间最基本的区别在于“学习理论”和“表现理论” - 即利用小脑内的突触可塑性来解释其在学习中的作用的理论,而不是解释其在学习中持续行为方面的理论。小脑信号处理的基础。这两种类型的几种理论已被制定为数学模型并使用计算机进行模拟。[38]
也许最早的“表演”理论是华伦天奴Braitenberg的“延迟线”假设。 Braitenberg和Roger Atwood在1958年提出的原始理论提出,信号沿平行光纤的缓慢传播会产生可预测的延迟,使小脑能够在某个窗口内检测时间关系。[42]实验数据不支持该理论的原始形式,但Braitenberg继续争论修改版本。[43]理查德·伊里(Richard Ivry)也提倡小脑作为计时系统起作用的假设。[44]另一个有影响力的“表现”理论是Pellionisz和Llinás的Tensor网络理论,它提供了一种先进的数学公式,即小脑进行的基本计算是将感觉转化为运动坐标。[45]
“学习”类别中的理论几乎全部来自Marr和Albus的出版物。马尔1969年的论文提出,小脑是一种学习将攀爬纤维编码的元素运动与编码感官背景的苔藓纤维输入联系起来的装置。[22] Albus在1971年提出,小脑浦肯野细胞起着感知器的作用,是一种神经启发的抽象学习装置。[5] Marr和Albus理论之间最基本的区别在于Marr认为攀爬纤维活动会导致平行纤维突触得到加强,而Albus则认为它们会被削弱。 Albus还将他的版本作为一种软件算法制定,他称之为CMAC(小脑模型关节控制器),已经在许多应用中进行了测试。[46]
血液供应
小脑提供来自三对成对主要动脉的血液:小脑上动脉(SCA),小脑前下动脉(AICA)和小脑后下动脉(PICA)。 SCA供应小脑的上部区域。 它在上表面和分支处分成软脑膜,其中分支与小脑前后动脉的分支吻合。 AICA供应小脑下表面的前部。 PICA到达下表面,在那里它分为内侧分支和侧向分支。 内侧分支向后延伸至小脑两个半球之间的小脑切口; 而侧支供给小脑的下表面,直至其外侧边界,在那里它与AICA和SCA吻合。
临床意义
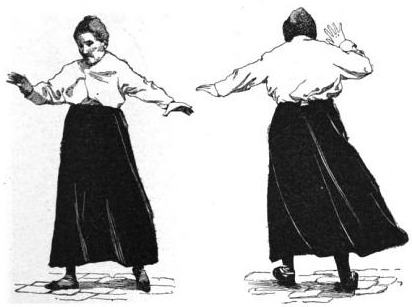
从1912年的插图改变行走步态的一名妇女患有小脑疾病

下部迹线显示患有小脑疾病的患者尝试再现上部迹线。
主要文章:小脑性共济失调
小脑损伤经常引起运动相关症状,其细节取决于所涉及的小脑部分及其受损情况。絮状结节叶的损伤可能表现为失去平衡,尤其是行走步态改变,不规则步态,平衡困难导致的宽阔姿势。[10]横向区域的损坏通常在熟练的自愿和计划运动中引起问题,这可能导致运动的力,方向,速度和幅度的误差。其他表现包括张力减退(肌张力降低),构音障碍(言语清晰度问题),dysmetria(判断距离或运动范围的问题),dysdiadochokinesia(无法进行快速交替运动,如行走),检查反射或反弹现象受损,以及意向震颤(由对立肌群交替收缩引起的不自主运动)。[47] [48]中线部分的损伤可能会扰乱全身运动,而局部更侧向的损伤更可能破坏手或肢体的精细运动。小脑上部的损伤往往会导致步态障碍和腿部协调的其他问题;下部的损坏更可能导致手臂和手的不协调或目标不良,以及速度上的困难。[10]这种运动症状的复杂称为共济失调。
为了识别小脑问题,神经系统检查包括评估步态(基于广泛的步态指示共济失调),指点测试和姿势评估。[3]如果指出小脑功能障碍,可以使用磁共振成像扫描来获得可能存在的任何结构改变的详细图片。[49]
可能产生小脑损伤的医疗问题清单很长,包括中风,出血,脑肿胀(脑水肿),肿瘤,酒精中毒,枪伤或爆炸物等创伤,以及慢性退行性疾病如橄榄脑小脑萎缩[ 50] [51]某些形式的偏头痛也可能导致小脑暂时性功能障碍,其严重程度不同。[52]在朊病毒疾病[53]和米勒费舍尔综合征(格林 - 巴利综合征的一种变体)等病症中,感染可导致小脑损伤。
老化
人类小脑随着年龄而变化。 这些变化可能与大脑其他部分的变化不同。 小脑是百岁老人中最年轻的大脑区域(和身体部位),根据组织年龄称为表观遗传时钟的表观遗传生物标志物:它比百岁老人的年龄小约15岁。[54] 此外,人类小脑中的基因表达模式显示出与大脑皮层相比较年龄相关的改变[55]。 一些研究报告称细胞数量或组织数量减少,但与此问题相关的数据量并不是很大。[56] [57]
发育和退行性疾病
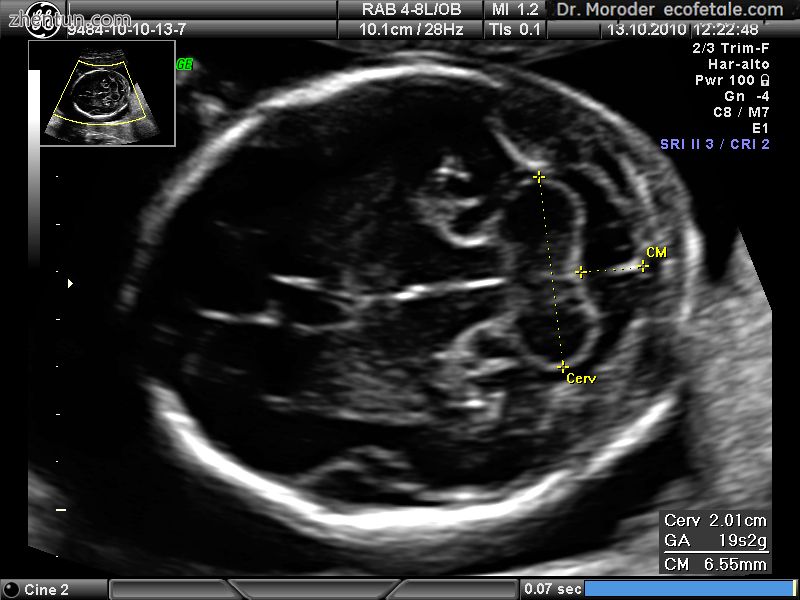
妊娠19周胎儿头部超声图像改良轴位,显示正常胎儿小脑和小脑池
先天性畸形,遗传性疾病和后天性疾病可影响小脑结构,从而影响小脑功能。除非致病条件是可逆的,否则唯一可能的治疗方法是帮助人们解决他们的问题。[58]在怀孕18至20周时通过超声扫描可视化胎儿小脑,可用于筛查胎儿神经管缺陷,敏感率高达99%。[59]
在正常发育中,内源性声波刺猬蛋白信号刺激外部颗粒层(EGL)中小脑颗粒神经元祖细胞(CGNP)的快速增殖。小脑发育发生在胚胎发育晚期和出生后早期,在早期发育期间(小鼠出生后第7天),EGL达到CGNP增殖。[60]由于CGNP最终分化为小脑颗粒细胞(也称为小脑颗粒神经元,CGN),它们迁移到内部颗粒层(IGL),形成成熟小脑(在小鼠的出生后第20天)。[60]异常激活Sonic hedgehog信号的突变易患Gorlin综合征和基因工程小鼠模型的小脑癌(成神经管细胞瘤)。[61] [62]
小脑蚓部的先天性畸形或发育不全(发育不全)是Dandy-Walker综合征和Joubert综合征的特征[63] [64]。在极少数情况下,整个小脑可能缺席。[65]遗传性神经系统疾病马查多 - 约瑟夫病,共济失调性毛细血管扩张症和弗里德赖希氏共济失调引起进行性神经变性,与小脑缺失有关[50] [58]。小脑外的先天性脑畸形反过来会导致小脑组织的突出,如某些形式的Arnold-Chiari畸形所见。[66]
与小脑变性密切相关的其他病症包括特发性进行性神经系统疾病多系统萎缩和Ramsay Hunt综合征I型[67] [68]和自身免疫性疾病副肿瘤性小脑变性,其中身体其他部位的肿瘤引发自身免疫反应这导致小脑神经元损失。[69]小脑萎缩可能是由于脚气病和Wernicke-Korsakoff综合征[70]或维生素E缺乏引起的维生素B1(硫胺素)急性缺乏所致。[58]
在许多其他神经系统疾病中观察到小脑萎缩,包括亨廷顿舞蹈病,多发性硬化症,[53]特发性震颤,进行性肌阵挛性癫痫和尼曼 - 皮克病。小脑萎缩也可能因接触毒素(包括重金属或药物或娱乐性药物)而发生。[58]
疼痛
人们普遍认为小脑参与疼痛处理。[71] [72] 小脑接受来自下行皮质 - 小脑通路和上行脊柱 - 小脑通路,通过脑桥核和下橄榄的疼痛输入。 这些信息中的一部分被转移到运动系统,诱导有意识的运动避免疼痛,根据疼痛强度进行分级。
这些直接疼痛输入以及间接输入被认为会引起长期疼痛避免行为,导致慢性姿势改变,从而导致前庭和本体感受核的功能和解剖学重塑。 因此,慢性神经性疼痛可以诱导后脑的宏观解剖重塑,包括小脑。[73] 这种重塑的程度和神经元祖细胞标记物的诱导表明成体神经发生对这些变化的贡献。
比较解剖和进化
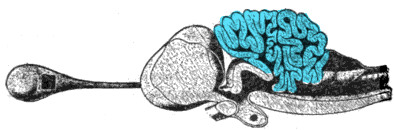
大斑鲨大脑的横截面,小脑以蓝色突出显示
小脑中的所有脊椎动物类似,包括鱼类,爬行动物,鸟类和哺乳动物。[74]在头足类动物中也存在类似的脑结构,其具有发育良好的大脑,例如章鱼。[75]这已被视为小脑对所有具有大脑的动物物种起重要作用的证据。
不同脊椎动物物种的小脑大小和形状存在相当大的差异。在两栖动物中,它几乎没有发育,在灯盏和ha鱼中,小脑几乎与脑干无法区分。虽然脊髓小脑存在于这些组中,但主要结构是小的,成对的核对应于前庭小脑。[76]爬行动物的小脑有点大,鸟类的大小要大,而哺乳动物的大小要大。在人类中发现的大的成对和复杂的叶是典型的哺乳动物,但小脑通常是其他组中的单个中叶,并且是平滑的或仅略微凹槽。在哺乳动物中,新生小脑是大脑中小脑的主要部分,但在其他脊椎动物中,它通常是脊髓小脑。[76]
软骨和骨鱼的小脑非常大而复杂。在至少一个重要方面,它在内部结构上与哺乳动物小脑不同:鱼小脑不包含离散的深小脑核。相反,浦肯野细胞的主要目标是分布在小脑皮质上的一种独特类型的细胞,这种类型在哺乳动物中未见。在mormyrid鱼(一种弱电敏感的淡水鱼)中,小脑比大脑的其他部分大得多。其中最大的部分是一种称为瓣膜的特殊结构,它具有异常规则的结构,并从电感觉系统获得大量输入。[77]
哺乳动物小脑的标志是侧叶的扩张,其主要相互作用与新皮质有关。当猴子进化成大猿时,侧叶的扩张继续,同时新皮质的额叶扩张。在祖先的原始人类和直到中更新世时期的智人中,小脑继续扩张,但额叶扩张得更快。然而,最近的人类进化时期实际上可能与小脑相对大小的增加有关,因为新小脑在小脑扩张时有所减小。[78]与大脑其他部分相比,人类小脑的大小一直在增加,而大脑的大小减小[79]随着运动任务的发展和实施,视觉空间技能和学习在小脑中发生,小脑的生长被认为与更高的人类认知能力有某种形式的相关性。[80]小脑的外侧半球现在是人类和猿类的2.7倍,而不是猴子。[79]小脑尺寸的这些变化不能通过更大的肌肉质量来解释。他们表明,小脑的发育与大脑其他部分的发育紧密相关,或者在人类进化过程中发生在小脑中的神经活动是重要的。由于小脑在认知功能中的作用,其大小的增加可能在认知扩张中发挥作用。[79]
小脑样结构
大多数脊椎动物物种都有小脑和一个或多个小脑样结构,大脑区域在细胞结构和神经化学方面类似于小脑。[74]在哺乳动物中发现的唯一小脑样结构是背侧耳蜗核(DCN),它是直接从听觉神经接收输入的两个主要感觉核之一。 DCN是一种分层结构,底层含有类似于小脑的颗粒细胞,产生平行的纤维,这些纤维上升到表层并横向穿过它。浅层包含一组称为车轮细胞的GABAergic神经元,它们在解剖学和化学上类似于浦肯野细胞 - 它们接收平行纤维输入,但没有任何类似攀爬纤维的输入。 DCN的输出神经元是锥体细胞。它们是谷氨酸能的,但在某些方面也类似于浦肯野细胞 - 它们具有刺状,扁平的表面树突树,它们接受平行纤维输入,但它们也具有基底树突,其接收来自听觉神经纤维的输入,其沿着DCN方向穿过DCN。与平行纤维成直角。 DCN在啮齿动物和其他小动物中最为发达,并且在灵长类动物中大大减少。其功能尚不清楚;最流行的猜测以某种方式将其与空间听觉联系起来。[81]
大多数鱼类和两栖动物都有侧线系统,可以感知水中的压力波。从侧线器官(内侧八边形核)接收初级输入的大脑区域之一具有小脑样结构,具有颗粒细胞和平行纤维。在电敏感鱼中,来自电感觉系统的输入进入背侧八边形核,其也具有小脑样结构。在鳍翅鱼(迄今为止最大的一组)中,视顶盖有一层 - 边缘层 - 类似于小脑。[74]
所有这些小脑样结构似乎主要与感觉有关,而不是与运动有关。它们都具有颗粒细胞,这些细胞产生平行纤维,连接到具有可修饰突触的浦肯野样神经元,但没有一个具有与小脑相当的攀爬纤维 - 相反,它们从外周感觉器官接收直接输入。没有一个具有证明功能,但最有影响力的推测是它们用于以某种复杂的方式改变感官输入,也许是为了补偿身体姿势的变化。[74]事实上,James M. Bower和其他人一直认为,部分是基于这些结构,部分是基于小脑研究,小脑本身基本上是一种感觉结构,它通过移动身体来促进运动控制。一种控制感觉信号的方法。[82]尽管有Bower的观点,但也有强有力的证据表明小脑直接影响哺乳动物的运动产量。[83] [84]
历史
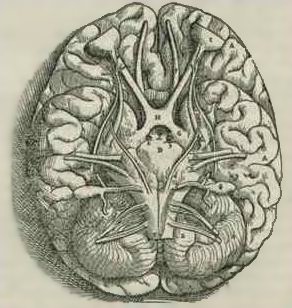
人类大脑的基础,由Andreas Vesalius在1543年绘制
说明
即便是最早的解剖学家也能通过其独特的外观来识别小脑。亚里士多德和Herophilus(引自Galen)称它为παρεγκεφαλίς(paregkephalis),而不是ἐγκέφαλος(egkephalos)或脑本身。盖伦的广泛描述是最早存活下来的。他推测小脑是运动神经的来源。[85]
直到文艺复兴时期才有进一步的重大发展。 Vesalius简要地讨论了小脑,并且在1664年托马斯·威利斯更详细地描述了解剖学。在18世纪进行了更多的解剖学工作,但直到19世纪早期才开始对小脑功能的第一次见解是获得。 Luigi Rolando于1809年确立了一项重要发现,即对小脑的损伤会导致运动障碍。 Jean Pierre Flourens在19世纪上半叶进行了详细的实验工作,揭示了小脑损伤的动物仍然可以移动,但失去协调(奇怪的动作,笨拙的步态和肌肉无力),以及之后的恢复除非病变非常广泛,否则病变几乎可以完成。[86]到20世纪初,人们普遍认为小脑的主要功能与运动控制有关; 20世纪上半叶对人类小脑疾病的临床症状进行了几次详细描述。[3]
词源
小脑这个名字是大脑(脑)的缩小; [87]它可以被翻译成小脑。拉丁文名称是古希腊语παρεγκεφαλίς(paregkephalis)的直接翻译,用于亚里士多德的作品,亚里士多德是第一个描述结构的着名作家。[88]在英语文献中没有使用其他名称,但历史上使用了各种希腊语或拉丁语名称,包括大脑小脑,[89] encephalion,[90] encranion,[89] cerebrum posterius,[91]和parencephalis。[89]
参考:
Journal
The 2016 version of this article has passed academic peer review (here) and was published in WikiJournal of Medicine.
It can be cited as: Wright M, Skaggs W, Nielsen FA, et al. (2016). "The Cerebellum". WikiJournal of Medicine. 3 (1). doi:10.15347/wjm/2016.001. open access publication
Hodos, William (2009), "Evolution of Cerebellum", Encyclopedia of Neuroscience, Springer, pp. 1240–1243, doi:10.1007/978-3-540-29678-2_3124, ISBN 978-3-540-23735-8
Wolf U, Rapoport MJ, Schweizer TA (2009). "Evaluating the affective component of the cerebellar cognitive affective syndrome". Journal of Neuropsychiatry and Clinical Neurosciences. 21 (3): 245–53. doi:10.1176/jnp.2009.21.3.245. PMID 19776302.
Fine EJ, Ionita CC, Lohr L (December 2002). "The history of the development of the cerebellar examination". Seminars in Neurology. 22 (4): 375–84. doi:10.1055/s-2002-36759. PMID 12539058.
Purves, Dale (2011). Dale Purves (ed.). Neuroscience (5th ed.). Sunderland, Mass.: Sinauer. pp. 417–423. ISBN 978-0-87893-695-3.
Albus JS (1971). "A theory of cerebellar function". Math. Biosciences. 10 (1–2): 25–61. CiteSeerX 10.1.1.14.7524. doi:10.1016/0025-5564(71)90051-4.
Purves, Dale Purves (2007). Neuroscience (4th ed.). New York: W. H. Freeman. pp. 197–200. ISBN 978-0-87893-697-7.
Susan Standring; Neil R. Borley; et al., eds. (2008). "Chapter 20". Gray's anatomy : the anatomical basis of clinical practice (40th ed.). London: Churchill Livingstone. p. 297. ISBN 978-0-8089-2371-8.
Llinas RR, Walton KD, Lang EJ (2004). "Ch. 7 Cerebellum". In Shepherd GM (ed.). The Synaptic Organization of the Brain. New York: Oxford University Press. ISBN 978-0-19-515955-4.
Herculano-Houzel S (2010). "Coordinated scaling of cortical and cerebellar numbers of neurons". Frontiers in Neuroanatomy. 4: 12. doi:10.3389/fnana.2010.00012. PMC 2839851. PMID 20300467.
Ghez C, Fahn S (1985). "The cerebellum". In Kandel ER, Schwartz JH (eds.). Principles of Neural Science, 2nd edition. New York: Elsevier. pp. 502–522.
Kingsley RE (2000). Concise Text of Neuroscience (2nd ed.). Lippincott Williams & Wilkins. ISBN 978-0-683-30460-2.
Petersen SE, Fox PT, Posner MI, Mintun M, Raichle ME (1989). "Positron emission tomographic studies of the processing of single words". Journal of Cognitive Neuroscience. 1 (2): 153–70. doi:10.1162/jocn.1989.1.2.153. PMID 23968463.
Timmann D, Daum I (2007). "Cerebellar contributions to cognitive functions: a progress report after two decades of research". Cerebellum. 6 (3): 159–62. doi:10.1080/14734220701496448. PMID 17786810.
Strick PL, Dum RP, Fiez JA (2009). "Cerebellum and nonmotor function". Annual Review of Neuroscience. 32: 413–34. doi:10.1146/annurev.neuro.31.060407.125606. PMID 19555291.
Buckner RL (October 2013). "The cerebellum and cognitive function: 25 years of insight from anatomy and neuroimaging". Neuron. 80 (3): 807–15. doi:10.1016/j.neuron.2013.10.044. PMID 24183029.
Schweighofer N, Doya K, Kuroda S (March 2004). "Cerebellar aminergic neuromodulation: towards a functional understanding". Brain Research. Brain Research Reviews. 44 (2–3): 103–16. doi:10.1016/j.brainresrev.2003.10.004. PMID 15003388.
Felizola SJ, Nakamura Y, Ono Y, Kitamura K, Kikuchi K, Onodera Y, Ise K, Takase K, Sugawara A, Hattangady N, Rainey WE, Satoh F, Sasano H (April 2014). "PCP4: a regulator of aldosterone synthesis in human adrenocortical tissues". Journal of Molecular Endocrinology. 52 (2): 159–67. doi:10.1530/JME-13-0248. PMC 4103644. PMID 24403568.
Eccles JC, Llinás R, Sasaki K (January 1966). "The excitatory synaptic action of climbing fibres on the Purkinje cells of the cerebellum". Journal of Physiology. 182 (2): 268–96. doi:10.1113/jphysiol.1966.sp007824. PMC 1357472. PMID 5944665.
Simpson JI, Wylie DR, De Zeeuw CI (1996). "On climbing fiber signals and their consequence(s)". Behav. Brain Sci. 19 (3): 384–398. doi:10.1017/S0140525X00081486.
Whitney ER, Kemper TL, Rosene DL, Bauman ML, Blatt GJ (February 2008). "Calbindin-D28k is a more reliable marker of human Purkinje cells than standard Nissl stains: a stereological experiment". Journal of Neuroscience Methods. 168 (1): 42–7. doi:10.1016/j.jneumeth.2007.09.009. PMID 17961663.
Rusanescu G, Mao J (February 2017). "Peripheral nerve injury induces adult brain neurogenesis and remodelling". Journal of Cellular and Molecular Medicine. 21 (2): 299–314. doi:10.1111/jcmm.12965. PMC 5264155. PMID 27665307.
Marr D (June 1969). "A theory of cerebellar cortex". Journal of Physiology. 202 (2): 437–70. doi:10.1113/jphysiol.1969.sp008820. PMC 1351491. PMID 5784296.
Apps R, Garwicz M (April 2005). "Anatomical and physiological foundations of cerebellar information processing". Nature Reviews. Neuroscience. 6 (4): 297–311. doi:10.1038/nrn1646. PMID 15803161.
Manni E, Petrosini L (March 2004). "A century of cerebellar somatotopy: a debated representation". Nature Reviews. Neuroscience. 5 (3): 241–9. doi:10.1038/nrn1347. PMID 14976523.
Oscarsson O (1979). "Functional units of the cerebellum-sagittal zones and microzones". Trends Neurosci. 2: 143–145. doi:10.1016/0166-2236(79)90057-2.
Rapp B (2001). The Handbook of Cognitive Neuropsychology: What Deficits Reveal about the Human Mind. Psychology Press. p. 481. ISBN 978-1-84169-044-5.
Doya K (December 2000). "Complementary roles of basal ganglia and cerebellum in learning and motor control". Current Opinion in Neurobiology. 10 (6): 732–9. doi:10.1016/S0959-4388(00)00153-7. PMID 11240282.
Manto M, Mariën P (2015). "Schmahmann's syndrome - identification of the third cornerstone of clinical ataxiology". Cerebellum & Ataxias. 2: 2. doi:10.1186/s40673-015-0023-1. PMC 4552302. PMID 26331045.
Schmahmann JD, Sherman JC (April 1998). "The cerebellar cognitive affective syndrome". Brain. 121 ( Pt 4) (4): 561–79. doi:10.1093/brain/121.4.561. PMID 9577385.
Levisohn L, Cronin-Golomb A, Schmahmann JD (May 2000). "Neuropsychological consequences of cerebellar tumour resection in children: cerebellar cognitive affective syndrome in a paediatric population". Brain. 123 ( Pt 5) (5): 1041–50. doi:10.1093/brain/123.5.1041. PMID 10775548.
Buckner RL, Krienen FM, Castellanos A, Diaz JC, Yeo BT (November 2011). "The organization of the human cerebellum estimated by intrinsic functional connectivity". Journal of Neurophysiology. 106 (5): 2322–45. doi:10.1152/jn.00339.2011. PMC 3214121. PMID 21795627.
Hernáez-Goñi P, Tirapu-Ustárroz J, Iglesias-Fernández L, Luna-Lario P (November 2010). "Participación del cerebelo en la regulación del afecto, la emoción y la conducta" [The role of the cerebellum in the regulation of affection, emotion and behavior]. Revista de Neurologia (in Spanish). 51 (10): 597–609. PMID 21069639. Archived from the original on 2014-08-19.
Turner BM, Paradiso S, Marvel CL, Pierson R, Boles Ponto LL, Hichwa RD, Robinson RG (March 2007). "The cerebellum and emotional experience". Neuropsychologia. 45 (6): 1331–41. doi:10.1016/j.neuropsychologia.2006.09.023. PMC 1868674. PMID 17123557.
Doya K (October 1999). "What are the computations of the cerebellum, the basal ganglia and the cerebral cortex?". Neural Networks. 12 (7–8): 961–974. doi:10.1016/S0893-6080(99)00046-5. PMID 12662639.
Eccles JC, Ito M, Szentágothai J (1967). The Cerebellum as a Neuronal Machine. Springer-Verlag.
The Cerebellum as a Neuronal Machine, p. 311
Boyden ES, Katoh A, Raymond JL (2004). "Cerebellum-dependent learning: the role of multiple plasticity mechanisms". Annual Review of Neuroscience. 27: 581–609. doi:10.1146/annurev.neuro.27.070203.144238. PMID 15217344.
Houk JC, Buckingham JT, Barto AG (1996). "Models of the cerebellum and motor learning" (PDF). Behav. Brain Sci. 19 (3): 368–383. CiteSeerX 10.1.1.118.2997. doi:10.1017/S0140525X00081474. Archived from the original (PDF) on 2017-08-09.
Fujita M (1982). "Adaptive filter model of the cerebellum". Biological Cybernetics. 45 (3): 195–206. doi:10.1007/BF00336192. PMID 7171642.
Gilbert PF, Thach WT (June 1977). "Purkinje cell activity during motor learning". Brain Research. 128 (2): 309–28. doi:10.1016/0006-8993(77)90997-0. PMID 194656.
Christian KM, Thompson RF (2003). "Neural substrates of eyeblink conditioning: acquisition and retention". Learning & Memory. 10 (6): 427–55. doi:10.1101/lm.59603. PMID 14657256.
Braitenberg V, Atwood RP (February 1958). "Morphological observations on the cerebellar cortex". Journal of Comparative Neurology. 109 (1): 1–33. doi:10.1002/cne.901090102. PMID 13563670.
Braitenberg V, Heck D, Sultan F (June 1997). "The detection and generation of sequences as a key to cerebellar function: experiments and theory". Behavioral and Brain Sciences. 20 (2): 229–45, discussion 245–77. doi:10.1017/s0140525x9700143x. PMID 10096998.
Ivry RB, Spencer RM, Zelaznik HN, Diedrichsen J (December 2002). "The cerebellum and event timing". Annals of the New York Academy of Sciences. 978 (1): 302–17. Bibcode:2002NYASA.978..302I. doi:10.1111/j.1749-6632.2002.tb07576.x. PMID 12582062.
Pellionisz A, Llinás R (1982). "Space-time representation in the brain. The cerebellum as a predictive space-time metric tensor". Neuroscience. 7 (12): 2949–70. doi:10.1016/0306-4522(82)90224-X. PMID 7162624.
Horváth G (2003). "CMAC: Reconsidering an old neural network" (PDF). Intelligent Control Systems and Signal Processing. Retrieved 2009-12-24.
Schmitz TJ (2007). "Examination of Coordination". In O'Sullivan SB, Schmitz TJ (eds.). Physical Rehabilitation. Philadelphia: F. A. Davis. pp. 193–225.
Mariën P, Manto M (2016). The linguistic cerebellum. London, UK: Academic Press. pp. 337–351. ISBN 978-0-12-801608-4.
Gilman S (March 1998). "Imaging the brain. Second of two parts". New England Journal of Medicine. 338 (13): 889–96. doi:10.1056/NEJM199803263381307. PMID 9516225.
"NINDS Ataxias and Cerebellar or Spinocerebellar Degeneration Information Page". National Institutes of Health. 16 April 2014. Archived from the original on 9 February 2015. Retrieved 2 February 2015.
Yuhas D (January 15, 2016). "Veterans of Iraq, Afghanistan Show Brain Changes Related to Explosion Exposure". Scientific American. Archived from the original on January 20, 2016. Retrieved January 21, 2016.
Vincent M, Hadjikhani N (June 2007). "The cerebellum and migraine". Headache. 47 (6): 820–33. doi:10.1111/j.1526-4610.2006.00715.x. PMC 3761082. PMID 17578530.
"NINDS Cerebellar Degeneration Information Page". National Institutes of Health. 28 February 2014. Archived from the original on 18 February 2015. Retrieved 2 February 2015.
Horvath S, Mah V, Lu AT, Woo JS, Choi OW, Jasinska AJ, Riancho JA, Tung S, Coles NS, Braun J, Vinters HV, Coles LS (May 2015). "The cerebellum ages slowly according to the epigenetic clock" (PDF). Aging. 7 (5): 294–306. doi:10.18632/aging.100742. PMC 4468311. PMID 26000617. Archived (PDF) from the original on 2015-05-25.
Fraser HB, Khaitovich P, Plotkin JB, Pääbo S, Eisen MB (September 2005). "Aging and gene expression in the primate brain". PLoS Biology. 3 (9): e274. doi:10.1371/journal.pbio.0030274. PMC 1181540. PMID 16048372.
Andersen BB, Gundersen HJ, Pakkenberg B (November 2003). "Aging of the human cerebellum: a stereological study". Journal of Comparative Neurology. 466 (3): 356–65. doi:10.1002/cne.10884. PMID 14556293.
Raz N, Gunning-Dixon F, Head D, Williamson A, Acker JD (2001). "Age and sex differences in the cerebellum and the ventral pons: a prospective MR study of healthy adults" (PDF). American Journal of Neuroradiology. 22 (6): 1161–7. PMID 11415913. Archived (PDF) from the original on 2008-12-17.
Albert, Richard K.; Porter, Robert S., eds. (2006). The Merck Manual of Diagnosis and Therapy (18th ed.). Whitehouse Station, New Jersey: Merck Research Libraries. pp. 1886–1887.
Campbell J, Gilbert WM, Nicolaides KH, Campbell S (August 1987). "Ultrasound screening for spina bifida: cranial and cerebellar signs in a high-risk population". Obstetrics and Gynecology. 70 (2): 247–50. PMID 3299184.
Hatten ME, Heintz N (1995). "Mechanisms of neural patterning and specification in the developing cerebellum". Annual Review of Neuroscience. 18: 385–408. doi:10.1146/annurev.ne.18.030195.002125. PMID 7605067.
Polkinghorn WR, Tarbell NJ (May 2007). "Medulloblastoma: tumorigenesis, current clinical paradigm, and efforts to improve risk stratification". Nature Clinical Practice. Oncology. 4 (5): 295–304. doi:10.1038/ncponc0794. PMID 17464337.
Roussel MF, Hatten ME (2011). Cerebellum development and medulloblastoma. Current Topics in Developmental Biology. 94. pp. 235–82. doi:10.1016/B978-0-12-380916-2.00008-5. ISBN 9780123809162. PMC 3213765. PMID 21295689.
"NINDS Joubert Syndrome Information Page". National Institutes of Health. 23 December 2013. Archived from the original on 4 January 2015. Retrieved 9 January 2015.
"NINDS Dandy-Walker Information Page". National Institutes of Health. 14 February 2014. Archived from the original on 4 January 2015. Retrieved 9 January 2015.
"NINDS Cerebellar Hypoplasia Information Page". National Institutes of Health. 29 September 2011. Archived from the original on 4 January 2015. Retrieved 9 January 2015.
"Chiari Malformation Fact Sheet". National Institutes of Health. 10 December 2014. Archived from the original on 27 October 2011. Retrieved 9 January 2015.
"NINDS Dyssynergia Cerebellaris Myoclonica Information Page". National Institutes of Health. 14 February 2011. Archived from the original on 16 February 2015. Retrieved 1 February 2015.
"NINDS Olivopontocerebellar Atrophy Information Page". National Institutes of Health. 16 April 2014. Archived from the original on 27 January 2012. Retrieved 9 January 2015.
"NINDS Paraneoplastic Syndromes Information Page". National Institutes of Health. 12 March 2009. Archived from the original on 4 January 2015. Retrieved 9 January 2015.
"NINDS Wernicke-Korsakoff Syndrome Information Page". National Institutes of Health. 14 February 2007. Archived from the original on 4 January 2015. Retrieved 9 January 2015.
Moulton EA, Schmahmann JD, Becerra L, Borsook D (October 2010). "The cerebellum and pain: passive integrator or active participator?". Brain Research Reviews. 65 (1): 14–27. doi:10.1016/j.brainresrev.2010.05.005. PMC 2943015. PMID 20553761.
Baumann O, Borra RJ, Bower JM, Cullen KE, Habas C, Ivry RB, Leggio M, Mattingley JB, Molinari M, Moulton EA, Paulin MG, Pavlova MA, Schmahmann JD, Sokolov AA (April 2015). "Consensus paper: the role of the cerebellum in perceptual processes". Cerebellum. 14 (2): 197–220. doi:10.1007/s12311-014-0627-7. PMC 4346664. PMID 25479821.
Rusanescu G, Mao J (February 2017). "Peripheral nerve injury induces adult brain neurogenesis and remodelling". Journal of Cellular and Molecular Medicine. 21 (2): 299–314. doi:10.1111/jcmm.12965. PMC 5264155. PMID 27665307.
Bell CC, Han V, Sawtell NB (2008). "Cerebellum-like structures and their implications for cerebellar function". Annual Review of Neuroscience. 31: 1–24. doi:10.1146/annurev.neuro.30.051606.094225. PMID 18275284.
Woodhams PL (July 1977). "The ultrastructure of a cerebellar analogue in octopus". Journal of Comparative Neurology. 174 (2): 329–45. doi:10.1002/cne.901740209. PMID 864041.
Romer AS, Parsons TS (1977). The Vertebrate Body. Philadelphia: Holt-Saunders International. p. 531. ISBN 978-0-03-910284-5.
Shi Z, Zhang Y, Meek J, Qiao J, Han VZ (August 2008). "The neuronal organization of a unique cerebellar specialization: the valvula cerebelli of a mormyrid fish". Journal of Comparative Neurology. 509 (5): 449–73. doi:10.1002/cne.21735. PMC 5884697. PMID 18537139.
Weaver AH (March 2005). "Reciprocal evolution of the cerebellum and neocortex in fossil humans". Proceedings of the National Academy of Sciences of the United States of America. 102 (10): 3576–80. Bibcode:2005PNAS..102.3576W. doi:10.1073/pnas.0500692102. PMC 553338. PMID 15731345.
Schoenemann PT (December 1, 2009). "Evolution of Brain and Language". Language Learning. 59: 162–186. doi:10.1111/j.1467-9922.2009.00539.x.
MacLeod CE, Zilles K, Schleicher A, Rilling JK, Gibson KR (April 2003). "Expansion of the neocerebellum in Hominoidea". Journal of Human Evolution. 44 (4): 401–29. doi:10.1016/S0047-2484(03)00028-9. PMID 12727461.
Roberts PD, Portfors CV (June 2008). "Design principles of sensory processing in cerebellum-like structures. Early stage processing of electrosensory and auditory objects". Biological Cybernetics. 98 (6): 491–507. doi:10.1007/s00422-008-0217-1. PMID 18491162.
Bower JM (1997). Is the cerebellum sensory for motor's sake, or motor for sensory's sake: the view from the whiskers of a rat?. Progress in Brain Research. 114. pp. 463–96. doi:10.1016/S0079-6123(08)63381-6. ISBN 978-0-444-82313-7. PMID 9193161.
Heiney SA, Kim J, Augustine GJ, Medina JF (February 2014). "Precise control of movement kinematics by optogenetic inhibition of Purkinje cell activity". Journal of Neuroscience. 34 (6): 2321–30. doi:10.1523/JNEUROSCI.4547-13.2014. PMC 3913874. PMID 24501371.
Witter L, Canto CB, Hoogland TM, de Gruijl JR, De Zeeuw CI (2013). "Strength and timing of motor responses mediated by rebound firing in the cerebellar nuclei after Purkinje cell activation". Frontiers in Neural Circuits. 7: 133. doi:10.3389/fncir.2013.00133. PMC 3748751. PMID 23970855.
Clarke E, O'Malley CD (1996). "Ch. 11: Cerebellum". The Human Brain and Spinal Cord (2nd ed.). Norman Publishing. p. 629. ISBN 978-0-930405-25-0.
Ito M (December 2002). "Historical review of the significance of the cerebellum and the role of Purkinje cells in motor learning". Annals of the New York Academy of Sciences. 978 (1): 273–88. Bibcode:2002NYASA.978..273I. doi:10.1111/j.1749-6632.2002.tb07574.x. PMID 12582060.
Lewis CT, Short C (1879). A Latin dictionary founded on Andrews' edition of Freund's Latin dictionary. Oxford: Clarendon Press.
Marshall LH, Magoun HW (1998). Discoveries in the human brain. Neuroscience prehistory, brain structure, and function. Totowa: Humana Press.
Foster FD (1891). An illustrated medical dictionary. New York: D. Appleton and Company.
Kraus LA (1844). Kritisch-etymologisches medicinisches Lexikon (Dritte Auflage). Göttingen: Verlag der Deuerlich- und Dieterichschen Buchhandlung.
Schreger CH (1805). Synonymia anatomica. Synonymik der anatomischen Nomenclatur. Fürth. |