大脑是一种器官,在所有脊椎动物和大多数无脊椎动物中都是神经系统的中心。大脑位于头部,通常靠近感觉器官,用于视觉等感官。大脑是脊椎动物体内最复杂的器官。在人类中,大脑皮层包含大约140-16亿个神经元,[1]并且小脑中估计的神经元数量为55-70亿个。[2]每个神经元通过突触连接到数千个其他神经元。这些神经元通过称为轴突的长原生质纤维相互通信,这些纤维携带称为动作电位的信号脉冲序列到大脑的远端部分或靶向特定受体细胞的身体。
在生理上,大脑的功能是对身体的其他器官进行集中控制。大脑通过产生肌肉活动模式和驱动称为激素的化学物质的分泌,作用于身体的其他部分。这种集中控制可以快速,协调地响应环境变化。一些基本类型的反应性如反射可以由脊髓或外周神经节介导,但基于复杂感觉输入的复杂有目的的行为控制需要集中大脑的信息整合能力。
现在已经相当详细地了解了各个脑细胞的操作,但它们在数百万个集合中的合作方式尚未得到解决。[3]最近的现代神经科学模型将大脑视为一种生物计算机,其机制与电子计算机截然不同,但在某种意义上它类似于从周围世界获取信息,存储信息并以各种方式处理信息。
本文比较了整个动物物种的大脑属性,最关注脊椎动物。它涉及人脑,因为它与其他大脑共有属性。人类大脑文章涵盖了人类大脑与其他大脑的不同之处。这里可能涉及的几个主题被覆盖在那里,因为在人类背景下可以对它们进行更多的讨论。最重要的是人脑条款中涵盖的脑部疾病和脑损伤的影响。

一种常见的黑猩猩大脑
目录
1 解剖
1.1 蜂窝结构
1.2 进化
2 发展
3 生理学
3.1 神经递质和受体
3.2 活动
3.3 代谢
4 功能
4.1 知觉
4.2 运动控制
4.3 觉醒
4.4 动态平衡
4.5 动机
4.6 学习和记忆
5 研究
5.1 历史
6 其他用途
6.1 作为食物
6.2 在仪式中
7 参考
解剖学
中间有一块蓝色斑点的斑点,周围是白色区域,周围是一条深色材料
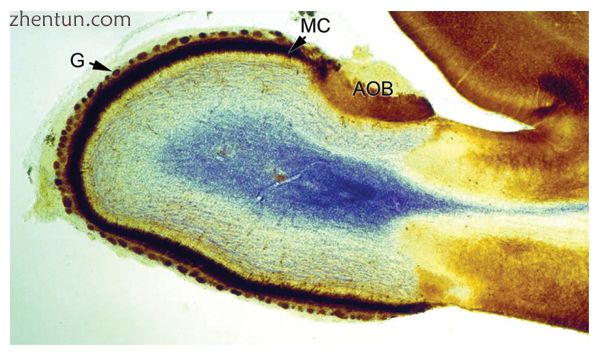
大鼠嗅球的横截面,同时以两种不同的方式染色:一种染色显示神经元细胞体,另一种染色显示神经递质GABA的受体。
大脑的形状和大小在不同物种之间差异很大,识别共同特征通常很困难。[4]然而,有许多适用于各种物种的大脑结构原理。[5]大脑结构的某些方面对于几乎所有动物物种都是常见的; [6]其他方面将“先进”大脑与更原始的大脑区分开来,或将脊椎动物与无脊椎动物区分开来。[4]
获取大脑解剖学信息的最简单方法是通过视觉检查,但已经开发了许多更复杂的技术。处于自然状态的脑组织太软而无法使用,但可以通过浸泡在酒精或其他固定剂中进行硬化,然后将其切片以检查内部。在视觉上,大脑的内部由所谓的灰质区域组成,具有深色,由白质区域分隔,具有较浅的颜色。通过用各种化学物质染色脑组织切片可以获得更多信息,这些化学物质可以产生高浓度存在特定类型分子的区域。还可以使用显微镜检查脑组织的微观结构,并追踪从一个脑区到另一个脑区的连接模式。[7]
细胞结构
图中显示了一个神经元,其中发出的纤维标记为“轴突”并与另一个细胞接触。插图显示了接触区的放大图。
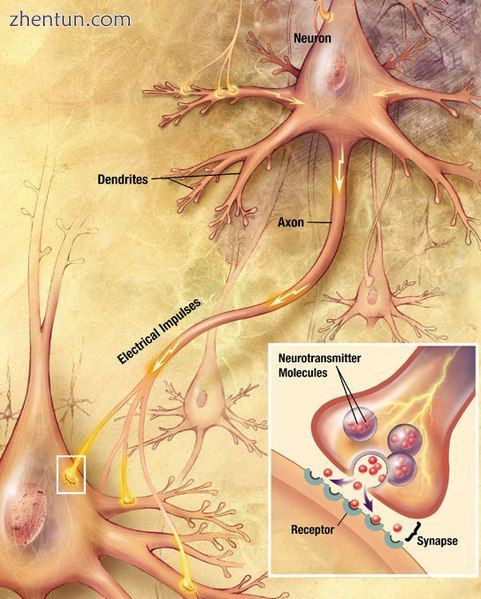
神经元产生沿其轴突传播的电信号。当电脉冲到达称为突触的连接处时,它会释放神经递质化学物质,这种化学物质与其他细胞上的受体结合,从而改变其电活动。
所有物种的大脑主要由两大类细胞组成:神经元和神经胶质细胞。胶质细胞(也称为神经胶质细胞或神经胶质细胞)有几种类型,并执行许多关键功能,包括结构支持,代谢支持,绝缘和发育指导。然而,神经元通常被认为是大脑中最重要的细胞。[8]使神经元独特的特性是它们能够长距离向特定目标细胞发送信号。[8]它们通过轴突发送这些信号,这是一种薄的原生质纤维,从细胞体延伸并通常有许多分支突出到其他区域,有时在附近,有时在大脑或身体的远处。轴突的长度可能非常特别:例如,如果大脑皮层的锥体细胞(兴奋性神经元)被放大以使其细胞体变成人体的大小,其轴突同样被放大,将成为电缆直径几厘米,延伸超过一公里。[9]这些轴突以称为动作电位的电化学脉冲的形式传输信号,其持续不到千分之一秒并沿着轴突以1-100米/秒的速度行进。一些神经元不断地以每秒10-100的速度发出动作电位,通常是不规则的模式;其他神经元大部分时间都很安静,但偶尔会发出一阵动作电位。[10]
轴突通过称为突触的特化连接将信号传递给其他神经元。单个轴突可能与其他细胞产生多达数千个突触连接。[8]当沿着轴突行进的动作电位到达突触时,它会释放一种称为神经递质的化学物质。神经递质与靶细胞膜中的受体分子结合[8]。
在红色和黑色背景下看到一个明亮的绿色细胞,长而高度分枝的绿色过程从多个方向延伸出来。
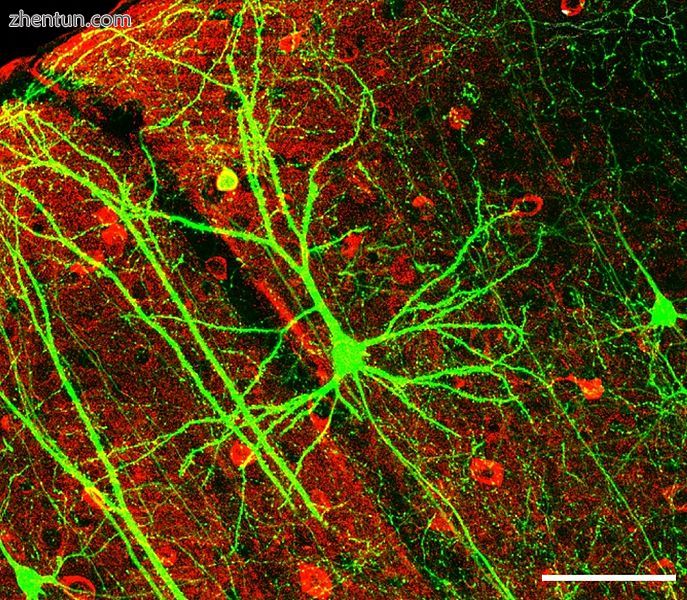
神经元通常具有广泛的树突网络,其接收突触连接。显示来自海马的锥体神经元,染色为绿色荧光蛋白。
突触是大脑的关键功能元素。[11]大脑的基本功能是细胞间通信,而突触是通信发生的点。人类的大脑估计含有大约100万亿个突触; [12]甚至果蝇的大脑也含有数百万个。[13]这些突触的功能非常多样化:一些是兴奋的(激发靶细胞);其他人都是抑制性的;其他人通过激活以复杂方式改变其靶细胞内部化学的第二信使系统来工作。[11]大量的突触是可动态修改的;也就是说,它们能够以通过它们的信号模式控制的方式改变强度。人们普遍认为,突触的活动依赖性修饰是大脑学习和记忆的主要机制。[11]
大脑中的大部分空间被轴突所占据,轴突通常被捆绑在一起,称为神经纤维束。髓鞘轴突包裹在髓鞘的脂肪绝缘鞘中,这有助于大大提高信号传播的速度。 (还有无髓鞘的轴突)。髓鞘是白色的,使得充满神经纤维的大脑部分看起来像浅色白质,而深色灰质则标志着神经细胞体密度高的区域。[8]
演化
主要文章:大脑的进化
通用的bilaterian神经系统
杆状体包含消化系统,该消化系统从一端的嘴部延伸到另一端的肛门。消化系统旁边是一条神经索,末端有一个大脑,靠近嘴巴。

一种普通双翅目动物的神经系统,具有节段性扩大的神经索形式,前面有“大脑”。
除了一些原始生物,如海绵(没有神经系统)[14]和刺胞动物(其神经系统由弥漫性神经网络组成[14]),所有活多细胞动物都是双向动物,意思是双侧动物对称的体形(即,左右两侧是彼此近似的镜像)。[15]所有的双字母都被认为是在485-540万年前的寒武纪早期出现的共同祖先的后裔,并且假设这个共同的祖先具有一个具有分割体的简单管虫的形状。[15]在示意图层面,基本的蠕虫形状继续反映在所有现代双性恋者的身体和神经系统结构中,包括脊椎动物。[16]基本的双侧体形式是具有从口到肛门的中空肠腔的管,以及用于每个身体部分的具有扩大(神经节)的神经索,在前部具有特别大的神经节,称为脑。在某些物种中,大脑很小而且很简单,例如线虫;在其他物种中,包括脊椎动物,它是体内最复杂的器官。[4]某些类型的蠕虫,如水蛭,在神经索的后端也有一个扩大的神经节,被称为“尾巴脑”。[17]
有一些类型的现有双声道缺乏可识别的大脑,包括棘皮动物和被子。尚未明确确定这些无脑物种的存在是否表明最早的双性恋者缺乏大脑,或者他们的祖先是否以导致先前存在的大脑结构消失的方式进化。
无脊椎动物
基于反射性表面的飞行。一个大的红眼睛面向相机。身体看起来是透明的,除了腹部末端的黑色素。
已经对果蝇(果蝇)进行了广泛的研究,以深入了解基因在大脑发育中的作用。
此类别包括缓动动物,节肢动物,软体动物和许多类型的蠕虫。无脊椎动物身体计划的多样性与大脑结构的相同多样性相匹配。[18]
两组无脊椎动物的脑部特别复杂:节肢动物(昆虫,甲壳动物,蜘蛛等)和头足类动物(章鱼,鱿鱼和类似的软体动物)。[19] 节肢动物和头足类动物的大脑来自延伸穿过动物体的双平行神经索。 节肢动物有一个中央大脑,即食管上神经节,在每只眼睛后面有三个分裂和大的光学瓣,用于视觉处理。[19] 章鱼和鱿鱼等头足类动物是所有无脊椎动物中最大的脑。[20]
有几种无脊椎动物物种的大脑已被密集研究,因为它们具有使其便于实验工作的特性:

由于可用于研究其遗传学的大量技术,果蝇(果蝇)已成为研究基因在大脑发育中的作用的自然主题。[21]尽管昆虫和哺乳动物之间存在很大的进化距离,但果蝇神经遗传学的许多方面已被证明与人类有关。例如,第一个生物钟基因是通过检测显示每日活动周期中断的果蝇突变体来鉴定的。[22]在脊椎动物的基因组中进行的搜索揭示了一组类似的基因,发现它们在小鼠生物钟中起着类似的作用 - 因此几乎可以肯定地在人类生物钟中也是如此。[23]对果蝇进行的研究也表明,大脑的大多数神经纤维区域在整个生命过程中不断重组,以应对特定的生活条件。[24]
线虫蠕虫秀丽隐杆线虫(Caenorhabditis elegans)与果蝇(Drosophila)一样,主要是因为它在遗传学中的重要性。[25]在20世纪70年代早期,悉尼布伦纳选择它作为模型生物来研究基因控制发育的方式。使用这种蠕虫的一个优点是身体计划非常刻板:雌雄同体的神经系统恰好包含302个神经元,总是在相同的位置,在每个蠕虫中形成相同的突触连接。[26] Brenner的团队将蠕虫切成数千个超薄切片并在电子显微镜下拍摄每个切片,然后在视觉上匹配各个部分的纤维,以绘制出整个身体中的每个神经元和突触。[27]实现了C.elegans的完整神经元接线图 - 它的连接组。[28]任何其他生物体都没有接近这种详细程度的信息,所获得的信息使得大量研究无法实现。[29]
由于其神经系统的简单性和可接近性,诺贝尔奖得主神经生理学家埃里克坎德尔选择了海slu Ap(Aplysia californica)作为研究学习和记忆的细胞基础的模型,并且已经在数百个实验中对其进行了检验。 30]
脊椎动物
T形物体由底部的绳索构成,该绳索进入下部中心质量。其顶部是较大的中央质量,臂从两侧延伸。
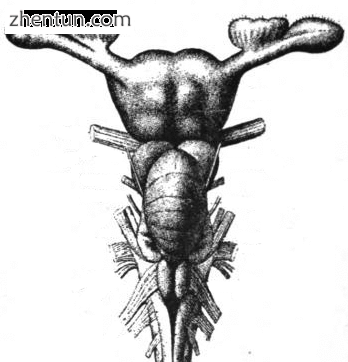
鲨鱼的大脑。
第一批脊椎动物出现在5亿年前(Mya),在寒武纪时期,可能与现代的hagfish类似。[31]鲨鱼出现约450 Mya,两栖动物约400 Mya,爬行动物约350 Mya,哺乳动物约200 Mya。每个物种都具有同样悠久的进化历史,但现代ha鱼,蝾螈,鲨鱼,两栖动物,爬行动物和哺乳动物的大脑表现出大小和复杂性的梯度,大致遵循进化序列。所有这些大脑都包含相同的基本解剖学组成部分,但许多大脑在ha鱼中是基本的,而在哺乳动物中,最重要的部分(端脑)被大大精心制作和扩展。[32]
大脑最容易根据它们的大小进行比较。已经在广泛的脊椎动物物种中研究了大脑大小,体型和其他变量之间的关系。通常,大脑尺寸随着体型的增加而增加,但不是简单的线性比例。一般来说,较小的动物往往有较大的大脑,以身体大小的一部分来衡量。对于哺乳动物,脑容量和体重之间的关系基本上遵循幂律,指数约为0.75。[33]这个公式描述了集中趋势,但每个哺乳动物家族都在某种程度上偏离了它,其方式部分反映了他们行为的复杂性。例如,灵长类动物的大脑比公式预测的大5至10倍。与体型相比,掠食者的大脑往往比猎物更大。[34]
神经系统显示为沿其长度具有突起的杆。底部的脊髓连接到后脑,后脑在变窄之前变宽。它连接到中脑,中脑再次凸出,并最终连接到具有两个大突起的前脑。
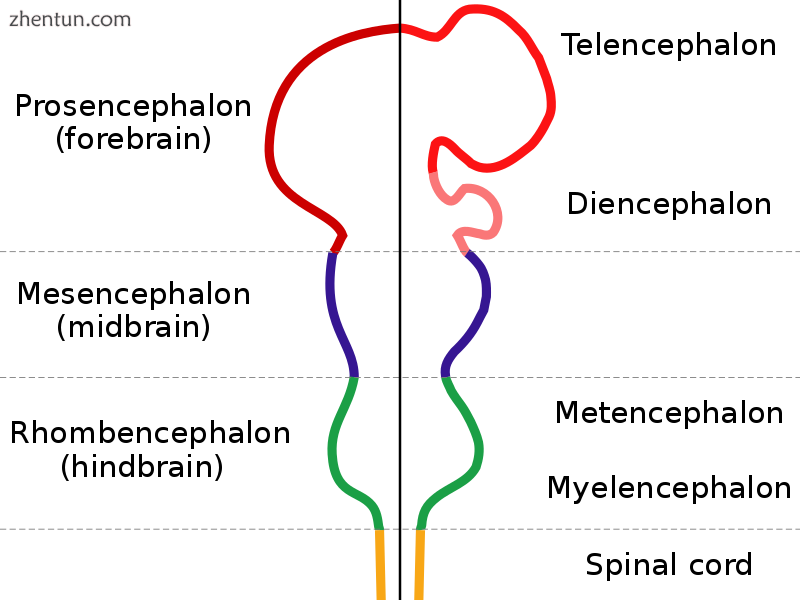
胚胎脊椎动物大脑的主要细分,后来分化为前脑,中脑和后脑。
所有脊椎动物的大脑都有一个共同的基础形式,在胚胎发育的早期阶段最明显。在其最早的形式中,大脑在神经管的前端出现三次肿胀;这些肿胀最终成为前脑,中脑和后脑(分别为前脑,中脑和菱形)。在大脑发育的最早阶段,这三个区域的大小大致相等。在许多类型的脊椎动物中,例如鱼类和两栖动物,这三个部分在成年人中大小相似,但在哺乳动物中,前脑变得比其他部分大得多,而中脑变得非常小。[8]
脊椎动物的大脑由非常软的组织制成。[8]活体脑组织外侧呈粉红色,内侧多为白色,颜色微妙变化。脊椎动物的大脑周围是一个结缔组织膜系统,称为脑膜,将头骨与大脑分开。血管通过脑膜层中的孔进入中枢神经系统。血管壁中的细胞彼此紧密连接,形成血脑屏障,阻止许多毒素和病原体的通过[35](虽然同时阻断抗体和一些药物,因此在治疗脑部疾病。)[36]
神经解剖学家通常将脊椎动物的大脑分成六个主要区域:端脑(脑半球),间脑(丘脑和下丘脑),中脑(中脑),小脑,脑桥和延髓(medulla oblongata)。这些区域中的每一个都具有复杂的内部结构。一些部分,例如大脑皮层和小脑皮质,由折叠或卷曲以适合可用空间的层组成。其他部分,如丘脑和下丘脑,由许多小核簇组成。基于神经结构,化学和连通性的精细区分,可以在脊椎动物大脑中识别出数以千计的可区分区域。[8]
尽管在所有脊椎动物大脑中都存在相同的基本成分,但脊椎动物进化的一些分支导致大脑几何形状的显著扭曲,尤其是在前脑区域。鲨鱼的大脑以直截了当的方式展示了基本成分,但是在硬骨鱼类(绝大多数现有的鱼类)中,前脑已经“外翻”,就像袜子里面翻出来一样。在鸟类中,前脑结构也有重大变化。[37]这些扭曲可能使一个物种的大脑成分与另一个物种的脑成分难以匹配。[38]
显示了人类和鲨鱼脑的相应区域。 鲨鱼的大脑是张开的,而人类的大脑更紧凑。 鲨鱼大脑从髓质开始,髓质被各种结构包围,并以端脑结束。 人脑的横截面显示底部的髓质被相同的结构包围,端脑厚厚地涂在脑的顶部。
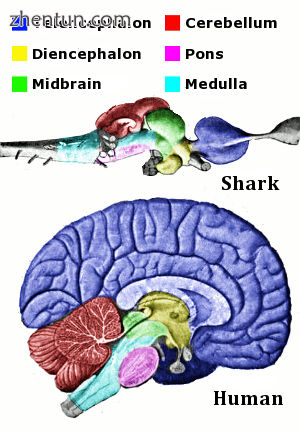
脊椎动物大脑的主要解剖区域,显示为鲨鱼和人类。存在相同的部件,但它们在尺寸和形状上有很大差异。
以下列出了一些最重要的脊椎动物大脑成分,以及目前所了解的功能简要说明:
另见:人脑中的区域列表
髓质与脊髓一起包含许多小核,这些小核涉及各种感觉和非自主运动功能,如呕吐,心率和消化过程。[8]
脑桥位于脑髓正上方的脑干中。除其他外,它包含控制通常是自愿但简单的行为的核,例如睡眠,呼吸,吞咽,膀胱功能,平衡,眼球运动,面部表情和姿势。[39]
下丘脑是前脑底部的一个小区域,其复杂性和重要性与其大小无关。它由许多小核组成,每个小核具有不同的连接和神经化学。下丘脑进行额外的非自愿或部分自愿行为,如睡眠和觉醒周期,进食和饮水,以及释放一些激素。[40]
丘脑是具有不同功能的核的集合:一些涉及向大脑半球传递信息和从大脑半球传递信息,而另一些则涉及动机。丘脑底区(zona incerta)似乎包含几种类型的“完成”行为的动作产生系统,如进食,饮酒,排便和交配。[41]
小脑调节其他脑系统的输出,无论是运动相关的还是与思想相关的,以使它们确定和精确。去除小脑不会阻止动物特别做任何事情,但它会使动作犹豫不决和笨拙。这种精度不是内置的,而是通过反复试验来学习的。骑自行车时学到的肌肉协调是一种神经可塑性的例子,可能主要发生在小脑内。[8]大脑总体积的10%由小脑组成,50%的神经元都在其结构内。[42]
光学顶盖允许动作指向空间中的点,最常见的是响应视觉输入。在哺乳动物中,它通常被称为上丘,其最佳研究功能是指导眼球运动。它还指导到达动作和其他面向对象的动作。它接收强大的视觉输入,但也有来自其他感官的输入,这些感觉可用于指导动作,例如猫头鹰的听觉输入和蛇的热敏坑器官的输入。在一些原始鱼类中,例如lampreys,这个区域是大脑的最大部分。[43]上丘是中脑的一部分。
大脑皮层是位于前脑表面的一层灰质,是大脑作为器官的最复杂和最近的进化发展。[44]在爬行动物和哺乳动物中,它被称为大脑皮层。多种功能涉及大脑皮层,包括气味和空间记忆。在哺乳动物中,它变得如此庞大以至于支配大脑,它接管来自许多其他大脑区域的功能。在许多哺乳动物中,大脑皮层由称为回旋的折叠凸起组成,形成深沟或称为沟的裂缝。褶皱增加了皮层的表面积,因此增加了灰质的数量和可以存储和处理的信息量。[45]
严格来说,海马只在哺乳动物中发现。然而,它来自内侧大脑皮层的区域在所有脊椎动物中都有对应物。有证据表明,这部分大脑涉及复杂事件,如鱼类,鸟类,爬行动物和哺乳动物的空间记忆和导航。[46]
基底神经节是前脑中的一组相互连接的结构。基底神经节的主要功能似乎是动作选择:它们将抑制信号发送到可以产生运动行为的大脑的所有部分,并且在适当的情况下可以释放抑制,从而动作生成系统能够执行他们的行为。奖励和惩罚通过改变基底神经节内的联系发挥其最重要的神经作用。[47]
嗅球是一种特殊结构,可处理嗅觉信号并将其输出发送到大脑皮层的嗅觉部分。它是许多脊椎动物的主要大脑成分,但在人类和其他灵长类动物中大大减少(其感官主要是通过视觉而非嗅觉获得的信息)。[48]
哺乳动物
哺乳动物和其他脊椎动物的大脑之间最明显的区别在于大小。平均而言,哺乳动物的大脑大约是相同体型大小的大脑的两倍,是相同体型的爬行动物的十倍大。[49]
然而,尺寸并不是唯一的区别:形状也存在很大差异。哺乳动物的后脑和中脑通常与其他脊椎动物的后脑和中脑相似,但前脑中出现了显著差异,前脑大大扩大,结构也发生了变化。[50]大脑皮层是大脑中最能区分哺乳动物的部分。在非哺乳动物的脊椎动物中,大脑表面衬有一种称为大脑皮层的相对简单的三层结构。在哺乳动物中,大脑皮层演变成一种复杂的六层结构,称为新皮质或同皮质。[51]新皮质边缘的几个区域,包括海马和杏仁核,在哺乳动物中也比其他脊椎动物更广泛地发展。[50]
大脑皮层的细化随着它的变化而变化到其他大脑区域。在大多数脊椎动物的视觉控制行为中起主要作用的上丘在哺乳动物中缩小到很小的尺寸,其大部分功能都被大脑皮层的视觉区域所接管。[49]哺乳动物的小脑包含大部分(新小脑),致力于支持大脑皮层,而其他脊椎动物则没有对应物。[52]
灵长类动物
脑化商数
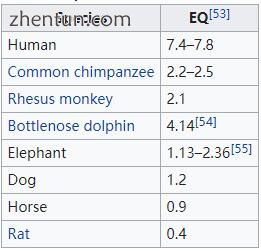
另见:人脑
人类和其他灵长类动物的大脑含有与其他哺乳动物大脑相同的结构,但通常与体型大小成比例。[56]脑化商(EQ)用于比较物种间的大脑尺寸。它考虑到了脑与身体关系的非线性。[53]人类的平均EQ在7到8的范围内,而大多数其他灵长类动物的EQ在2到3的范围内。海豚的价值高于人类以外的灵长类动物[54],但几乎所有其他哺乳动物的EQ值都要低得多。
灵长类动物大脑的大部分扩大来自大脑皮层的大量扩张,特别是前额叶皮层和参与视力的皮质部分。[57]灵长类动物的视觉处理网络包括至少30个可区分的脑区域,具有复杂的互连网络。据估计,视觉处理区域占灵长类动物新皮层总表面的一半以上。[58]前额皮质执行的功能包括计划,工作记忆,动机,注意力和执行控制。对于灵长类动物而言,它占据的大脑比例远远大于其他物种,占人类大脑的一大部分。[59]
发展
主要文章:神经发育
非常简单地绘制人类胚胎的前端,以不同的颜色显示发育中的大脑的每个囊泡。
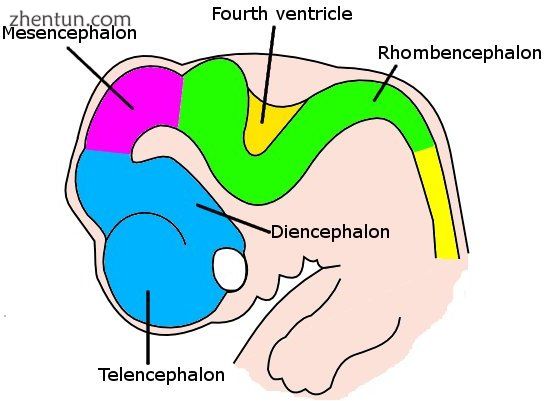
人类胚胎的大脑在发育的第六周。
大脑以错综复杂的精心安排的阶段发展。[60]它的形状从最早的胚胎阶段神经索前部的简单肿胀变为复杂的区域和连接。神经元在包含干细胞的特殊区域中产生,然后通过组织迁移到达其最终位置。一旦神经元定位自己,它们的轴突发芽并在大脑中导航,分支并随着它们一直延伸,直到尖端到达目标并形成突触连接。在神经系统的许多部分中,神经元和突触在早期阶段产生过多,然后将不需要的神经元和突触修剪掉。[60]
对于脊椎动物,神经发育的早期阶段在所有物种中都是相似的。[60]当胚胎从圆形细胞转变成蠕虫状结构时,沿着背部中线延伸的一条外胚层的狭窄条带被诱导成为神经板,神经系统的前体。神经板向内折叠以形成神经沟,然后将凹槽排列的唇部合并以包围神经管,神经管是一个中空的细胞绳,中心有充满液体的心室。在前端,心室和脐带膨胀形成三个囊泡,这些囊泡是前脑,中脑和后脑的前体。在下一阶段,前脑分裂成两个囊泡,称为端脑(包含大脑皮质,基底神经节和相关结构)和间脑(包含丘脑和下丘脑)。大约在同一时间,后脑分裂成脑膜(包含小脑和脑桥)和脑膜(包含延髓)。这些区域中的每一个都包含增生区,其中产生神经元和神经胶质细胞;然后,由此产生的细胞有时会长距离迁移到最终位置。[60]
一旦神经元到位,它就会将树突和轴突延伸到它周围的区域。轴突,因为它们通常延伸离细胞体很远,需要达到特定目标,以特别复杂的方式生长。生长轴突的尖端由称为生长锥的一团原生质组成,上面嵌有化学受体。这些受体感知局部环境,使生长锥被各种细胞元件吸引或排斥,从而沿着其路径在每个点处沿特定方向被拉动。这种寻路过程的结果是生长锥通过大脑导航直到它到达目的地区域,其中其他化学信号使其开始产生突触。考虑到整个大脑,成千上万的基因会产生影响轴突寻路的产物。[60]
最终出现的突触网络仅部分由基因决定。在大脑的许多部位,轴突最初“过度生长”,然后被依赖于神经活动的机制“修剪”。[60]例如,在从眼睛到中脑的投影中,成人中的结构包含非常精确的映射,将视网膜表面上的每个点连接到中脑层中的对应点。在发育的第一阶段,来自视网膜的每个轴突通过化学线索被引导到中脑的右侧一般附近,但随后分支非常大并且与大量中脑神经元初始接触。视网膜在出生之前包含特殊的机制,使其产生在随机点自发产生的活动波,然后缓慢地穿过视网膜层。这些波是有用的,因为它们会导致相邻神经元同时活跃;也就是说,它们产生一种神经活动模式,其中包含有关神经元空间排列的信息。如果轴突中的活性没有跟随靶细胞的活动,则通过导致突触减弱并最终消失的机制在中脑中利用该信息。这一复杂过程的结果是逐步调整和收紧地图,最终使其成为精确的成人形式。[61]
类似的事情发生在其他大脑区域:初始突触基质是由遗传决定的化学指导产生的,但随后通过活动依赖机制逐渐完善,部分由内部动力学驱动,部分由外部感觉输入驱动。在某些情况下,与视网膜 - 中脑系统一样,活动模式依赖于仅在发育中的大脑中起作用的机制,并且显然仅存在于指导发育。[61]
在人类和许多其他哺乳动物中,新生神经元主要在出生前产生,婴儿大脑比成年大脑含有更多的神经元。[60]然而,有一些领域会在整个生命过程中继续产生新的神经元。成人神经发生已经建立的两个区域是涉及嗅觉的嗅球和海马的齿状回,其中有证据表明新神经元在存储新获得的记忆中起作用。然而,除了这些例外,童年早期存在的一组神经元就是生命存在的集合。胶质细胞是不同的:与体内大多数类型的细胞一样,它们在整个生命周期中产生。[62]
长期以来一直在争论思维,人格和智慧的品质是否可归因于遗传或培养 - 这是自然和培育的争议。[63]虽然许多细节仍有待解决,但神经科学研究已经清楚地表明这两个因素都很重要。基因决定了大脑的一般形式,基因决定了大脑对经验的反应。然而,需要经验来改进突触连接的矩阵,其发展形式包含比基因组更多的信息。在某些方面,重要的是在关键的发展阶段是否存在经验。[64]在其他方面,经验的数量和质量很重要;例如,有大量证据表明,在富集环境中饲养的动物的脑皮质较厚,表明突触连接的密度高于刺激水平受限的动物。[65]
生理
大脑的功能取决于神经元将电化学信号传输到其他细胞的能力,以及它们对从其他细胞接收的电化学信号作出适当响应的能力。神经元的电学特性受到各种生化和代谢过程的控制,最显著的是神经递质和突触发生的受体之间的相互作用。[8]
神经递质和受体
神经递质是当动作电位激活它们时在突触处释放的化学物质 - 神经递质将它们自身附着到突触的靶细胞膜上的受体分子,从而改变受体分子的电学或化学性质。除了极少数例外,大脑中的每个神经元在与其他神经元形成的所有突触连接处释放相同的化学神经递质或神经递质的组合;这条规则被称为戴尔的原则。[8]因此,神经元可以通过它释放的神经递质来表征。绝大多数精神活性药物通过改变特定的神经递质系统发挥其作用。这适用于大麻素,尼古丁,海洛因,可卡因,酒精,氟西汀,氯丙嗪等许多药物。[66]
脊椎动物大脑中使用最广泛的两种神经递质是谷氨酸,几乎总是对靶神经元产生兴奋作用,而γ-氨基丁酸(GABA)几乎总是具有抑制作用。使用这些发射器的神经元几乎可以在大脑的每个部位找到。[67]由于它们无处不在,作用于谷氨酸或GABA的药物往往具有广泛而强大的作用。一些全身麻醉剂通过降低谷氨酸的作用起作用;大多数镇静剂通过增强GABA的作用来发挥其镇静作用。[68]
有许多其他化学神经递质用于大脑的更有限的区域,通常是专用于特定功能的区域。例如,血清素 - 抗抑郁药物和许多膳食辅助药物的主要目标 - 完全来自称为中缝核的小脑干区域。[69]参与唤醒的去甲肾上腺素来自附近的一个叫做蓝斑的小区域。[70]其他神经递质如乙酰胆碱和多巴胺在大脑中有多种来源,但不像谷氨酸和GABA那样普遍存在。[71]
电活动
图表显示了从左到右穿过页面的16条电压轨迹,每条电路都显示不同的信号。在页面的中间,所有的痕迹突然开始显示尖锐的生涩尖峰,这继续到情节的结尾。
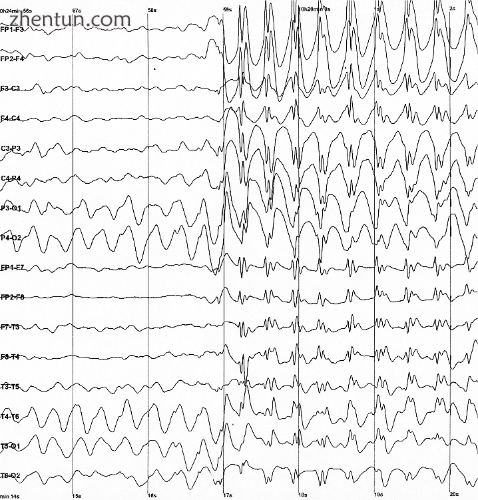
在癫痫发作期间从人类患者记录的脑电活动。
作为神经元用于信号传导的电化学过程的副作用,脑组织在其活跃时产生电场。当大量神经元显示同步活动时,它们产生的电场可以大到足以在头骨外部进行检测,使用脑电图(EEG)[72]或脑磁图(MEG)。脑电图记录以及植入大鼠等动物脑内电极的记录显示,即使在睡眠期间,活体动物的大脑也会持续活跃。[73]大脑的每个部分都显示出节律性和非节律性活动的混合,这可能根据行为状态而变化。在哺乳动物中,大脑皮层倾向于在睡眠期间显示出大的缓慢的δ波,当动物清醒但是注意力不集中时更快的α波,以及当动物积极地参与任务时看起来混乱的不规则活动。在癫痫发作期间,大脑的抑制控制机制无法发挥作用,电活动升至病理水平,产生脑电图痕迹,显示健康大脑中未见的大波和尖峰模式。将这些人口水平模式与个体神经元的计算功能联系起来是当前神经生理学研究的一个主要焦点。[73]
代谢
所有脊椎动物都有血脑屏障,允许大脑内的新陈代谢与身体其他部位的新陈代谢不同。胶质细胞通过控制神经元周围的液体的化学成分,包括离子和营养素的水平,在脑代谢中发挥重要作用。[74]
脑组织消耗大量的能量与其体积成比例,因此大脑对动物产生严重的代谢需求。例如,为了飞行,限制体重的需要显然导致选择减少某些物种(如蝙蝠)的大脑尺寸。[75]大脑的大部分能量消耗都会持续维持神经元的电荷(膜电位)。[74]大多数脊椎动物物种将2%至8%的基础代谢用于大脑。然而,在灵长类动物中,这个比例要高得多 - 在人类中它升高到20-25%。[76]大脑的能量消耗随时间变化不大,但大脑皮层的活跃区域比非活动区域消耗更多的能量;这形成了PET,fMRI,[77]和NIRS的功能性脑成像方法的基础。[78]大脑通常从葡萄糖的氧依赖性代谢(即血糖)获得大部分能量[74],但酮类提供了主要的替代来源,以及中链脂肪酸(辛酸和庚酸)的贡献[79]。 ] [80]乳酸,[81]乙酸,[82]和可能的氨基酸。[83]
功能
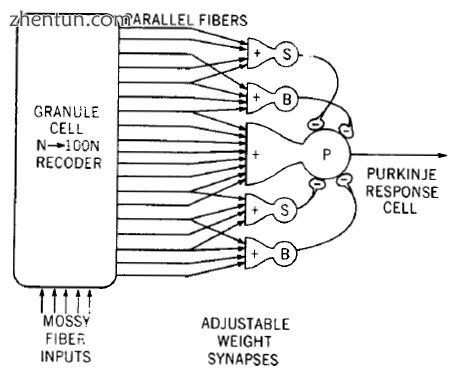
由James S. Albus提出的小脑神经回路模型。
来自感觉器官的信息被收集在大脑中。在那里它被用来确定有机体将采取什么行动。大脑处理原始数据以提取有关环境结构的信息。接下来,它将处理过的信息与有关动物当前需求的信息以及对过去环境的记忆相结合。最后,在结果的基础上,它产生运动反应模式。这些信号处理任务需要各种功能子系统之间错综复杂的相互作用。[84]
大脑的功能是提供对动物行为的连贯控制。集中的大脑允许肌肉群以复杂的模式共同激活;它还允许刺激身体一部分的刺激引起其他部分的反应,并且它可以防止身体的不同部分彼此交叉作用。[84]
知觉
绘图显示听力所涉及的耳朵,内耳和大脑区域。一系列浅蓝色箭头表示通过系统的信号流。
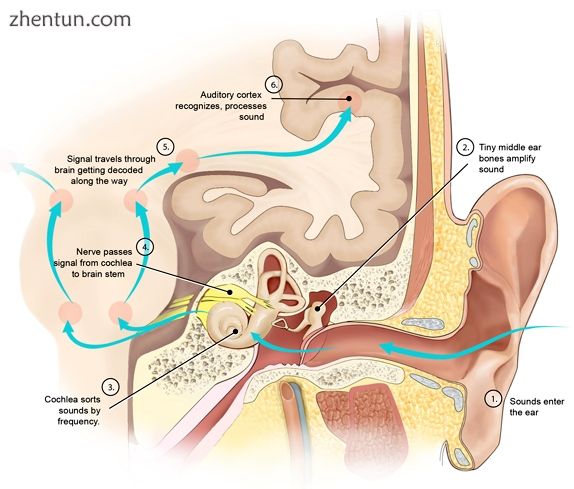
听觉系统中的信号处理图。
人脑提供有关光,声音,大气化学成分,温度,头部方向,肢体位置,血流化学成分等信息。在其他动物中,存在额外的感觉,例如蛇的红外热感,某些鸟类的磁场感,或某些类型的鱼的电场感。
每个感觉系统都以专门的受体细胞开始,[8]如眼睛视网膜中的光接收神经元,或耳朵耳蜗中的振动敏感神经元。感觉受体细胞的轴突进入脊髓或大脑,在那里它们将信号传递到专用于一种特定感觉方式的一级感觉核。该主要感觉核将信息发送到专用于相同模态的高阶感觉区域。最后,通过丘脑中的一个路站,信号被发送到大脑皮层,在那里它们被处理以提取相关特征,并与来自其他感觉系统的信号相结合。[8]
运动控制
运动系统是大脑中涉及引发身体运动的区域,即激活肌肉。除了由中脑细胞核驱动的控制眼睛的肌肉外,体内所有的随意肌肉都直接由脊髓和后脑中的运动神经元支配。[8]脊髓运动神经元由脊髓内在的神经回路和从大脑下降的输入控制。内在脊髓回路实现许多反射反应,并包含用于有节奏运动的模式发生器,例如步行或游泳。来自大脑的下行连接允许更复杂的控制。[8]
大脑包含几个直接投射到脊髓的运动区域。最低级别是髓质和脑桥中的运动区域,其控制诸如步行,呼吸或吞咽的定型运动。在较高水平的是中脑区域,例如红核,其负责协调手臂和腿的运动。在更高的水平还是初级运动皮层,位于额叶后缘的一条组织。初级运动皮层向皮质下运动区域发送投射,但也通过锥体束直接向脊髓发送大量投射。这种直接皮质脊柱投影允许精确自主控制运动的细节。其他与运动相关的脑区通过投射到主要运动区域而产生次要影响。最重要的次要区域是前运动皮质,基底神经节和小脑。[8]
涉及控制运动的主要领域
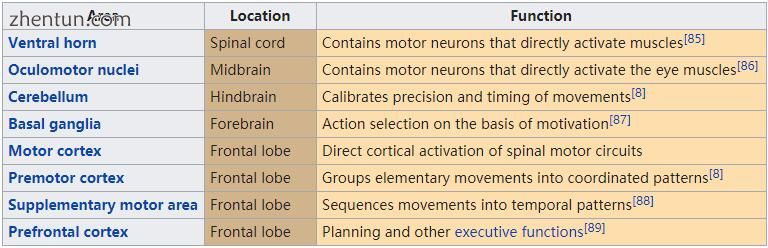
除了上述所有内容外,大脑和脊髓还含有广泛的控制自主神经系统的电路,通过分泌激素和调节肠道的“平滑”肌肉来发挥作用。[8]
觉醒
另见:睡眠
许多动物在每日周期中睡觉和醒来之间交替。唤醒和警觉性也通过大脑区域网络在更精细的时间尺度上进行调节。[8]
唤醒系统的一个关键组成部分是视交叉上核(SCN),它是下丘脑的一小部分,位于两只眼睛的视神经交叉点的正上方。 SCN包含身体的中心生物钟。那里的神经元显示活动水平上升和下降,持续约24小时,昼夜节律:这些活动波动是由一组“时钟基因”的表达的节律性变化驱动的。 SCN继续保持时间,即使它从大脑切除并置于温热营养液的盘子中,但它通常接收来自视神经的输入,通过视网膜下丘脑束(RHT),允许每日光暗周期到校准时钟。[90]
SCN投射到下丘脑,脑干和中脑的一组区域,这些区域参与实施睡眠 - 觉醒周期。该系统的一个重要组成部分是网状结构,一组神经元簇散布在下脑的核心。网状神经元将信号发送到丘脑,丘脑又将活动水平控制信号发送到皮质的每个部分。网状结构的损伤可以产生永久性的昏迷状态。[8]
睡眠涉及大脑活动的巨大变化。[8] 直到20世纪50年代,人们普遍认为大脑在睡眠期间基本上会关闭,[91]但现在已知这种情况远非如此; 活动仍在继续,但模式变得非常不同。 有两种类型的睡眠:REM睡眠(带有梦想)和NREM(非REM,通常没有做梦)睡眠,在整个睡眠期间以轻微变化的模式重复。 可以测量三种不同的大脑活动模式:REM,轻型NREM和深度NREM。 在深度NREM睡眠期间,也称为慢波睡眠,皮层中的活动采取大型同步波的形式,而在清醒状态下,它是嘈杂和不同步的。 慢波睡眠期间神经递质去甲肾上腺素和5-羟色胺的水平下降,在REM睡眠期间下降几乎为零; 乙酰胆碱水平显示出相反的模式。[8]
动态平衡
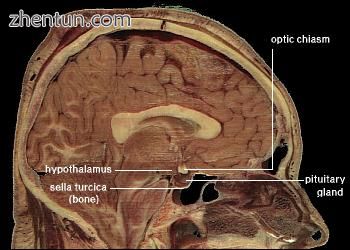
人体头部的横截面,显示下丘脑的位置。
对于任何动物,生存需要在有限的变异范围内保持身体状态的各种参数:这些参数包括温度,水含量,血液中的盐浓度,血糖水平,血氧水平等。[92]动物调节其身体内部环境的能力 - 环境生理学家克劳德伯纳德称之为环境 - 称为体内平衡(希腊语为“静止不动”)。[93]维持体内平衡是大脑的重要功能。归纳稳态的基本原则是负反馈:任何时候参数偏离其设定点,传感器都会产生一个错误信号,引起一个响应,导致参数转回其最佳值。[92] (该原理广泛用于工程,例如使用恒温器控制温度。)
在脊椎动物中,发挥最大作用的大脑部分是下丘脑,这是前脑基部的一个小区域,其大小不能反映其复杂性或其功能的重要性。[92]下丘脑是一个小核的集合,其中大部分参与基本的生物学功能。这些功能中的一些涉及唤醒或社交互动,如性,侵略或母性行为;但其中许多与体内平衡有关。几个下丘脑核接收来自位于血管内壁的传感器的输入,传达关于温度,钠水平,葡萄糖水平,血氧水平和其他参数的信息。这些下丘脑核将输出信号发送到运动区域,可以产生纠正缺陷的动作。一些输出物也会进入垂体腺,这是一个直接附着在下丘脑下方大脑的小腺体。垂体腺将激素分泌到血液中,在血液中循环,诱导细胞活动的变化。[94]
动机
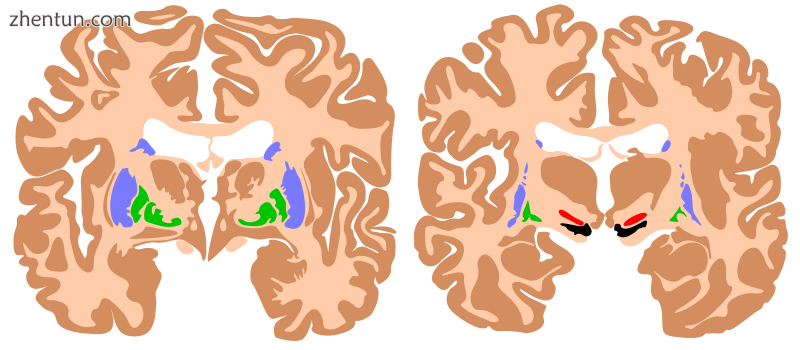
基底神经节的组成部分,显示在人脑的两个横截面中。蓝色:尾状核和壳核。绿色:苍白苍白球。红色:丘脑底核。黑色:黑色。
个体动物需要表达促进生存的行为,例如寻找食物,水,住所和配偶。[95]大脑中的激励系统监视这些目标的当前满意状态,并激活行为以满足任何出现的需求。激励制度主要通过奖惩机制起作用。当特定行为之后是有利的后果时,大脑中的奖励机制被激活,这引起大脑内部的结构变化,导致相同的行为在以后出现类似情况时重复。相反,当行为之后出现不利后果时,大脑的惩罚机制被激活,引发结构性变化,导致在未来出现类似情况时行为被抑制。[96]
迄今为止研究的大多数生物利用奖惩机制:例如,蠕虫和昆虫可以改变其行为以寻求食物来源或避免危险。[97]在脊椎动物中,奖惩系统由一组特定的脑结构实现,其核心位于基底神经节,即前脑底部的一组相互连接的区域。[47]基底神经节是作出决定的中心部位:基底神经节对大脑中的大多数运动系统施加持续的抑制控制;当释放该禁止时,允许电动机系统执行其编程执行的动作。奖励和惩罚通过改变基底神经节接收的输入与发射的决策信号之间的关系起作用。奖励机制比惩罚机制更好理解,因为它在滥用药物方面的作用使得它得到了非常密集的研究。研究表明,神经递质多巴胺起着重要作用:可卡因,安非他明和尼古丁等成瘾药物会导致多巴胺水平升高或导致大脑内多巴胺的作用增强。[98]
学习和记忆
几乎所有动物都能够根据经验改变它们的行为 - 即使是最原始的蠕虫类型。因为行为是由大脑活动驱动的,所以行为的变化必须以某种方式与大脑内部的变化相对应。已经在19世纪晚期,像圣拉莫·拉卡·卡哈尔这样的理论家认为,最合理的解释是学习和记忆表达为神经元之间突触联系的变化。[99]然而,直到1970年,缺乏支持突触可塑性假设的实验证据。 1971年,Tim Bliss和TerjeLømo发表了一篇关于现在称为长期增强的现象的论文:该论文显示了活动引起的突触变化的明确证据,持续至少数天。[100]从那时起,技术进步使得这些实验更容易实施,并且已经进行了数千项研究,阐明了突触变化的机制,并揭示了各种大脑区域中其他类型的活动驱动的突触变化,包括大脑皮质,海马,基底神经节和小脑。[101]脑源性神经营养因子(BDNF)和身体活动似乎在该过程中发挥了有益作用。[102]
神经科学家目前区分了以不同方式由大脑实现的几种类型的学习和记忆:
工作记忆是大脑保持关于动物当前所从事任务的信息的临时表示的能力。这种动态记忆被认为是由细胞集合的形成介导的 - 维持它们的活化神经元组。通过不断激励彼此的活动。[103]
情景记忆是记住特定事件细节的能力。这种记忆可以持续一生。许多证据表明海马体发挥了至关重要的作用:对海马体有严重损伤的人有时会表现出健忘症,即无法形成新的持久的情景记忆。[104]
语义记忆是学习事实和关系的能力。这种记忆可能主要存储在大脑皮质中,由代表特定类型信息的细胞之间的连接变化调节。[105]
器乐学习是奖励和惩罚行为的能力。它由以基底神经节为中心的大脑区域网络实施。[106]
运动学习是通过练习或更一般地通过重复来改善身体运动模式的能力。涉及许多大脑区域,包括前运动皮层,基底神经节,尤其是小脑,它们作为大型记忆库,用于微调运动参数。[107]
研究
主要文章:神经科学
人脑项目是一项大型科研项目,从2013年开始,旨在模拟完整的人类大脑。
神经科学领域包括所有寻求了解大脑和其他神经系统的方法。[8]心理学旨在了解心灵和行为,神经学是诊断和治疗神经系统疾病的医学学科。大脑也是精神病学研究中最重要的器官,精神病学是致力于研究,预防和治疗精神障碍的医学分支。[108]认知科学试图将神经科学和心理学与其他与大脑有关的领域统一起来,例如计算机科学(人工智能和类似领域)和哲学。[109]
最古老的大脑研究方法是解剖学的,直到20世纪中叶,神经科学的大部分进展来自于更好的细胞染色和更好的显微镜的发展。神经解剖学家研究大脑的大规模结构以及神经元及其组成部分的微观结构,特别是突触。在其他工具中,它们使用了大量的污渍,揭示了神经结构,化学和连接性。近年来,免疫染色技术的发展已经允许研究表达特定基因组的神经元。此外,功能性神经解剖学使用医学成像技术将人类大脑结构的变化与认知或行为的差异联系起来。[110]
神经生理学家研究大脑的化学,药理学和电学特性:他们的主要工具是药物和记录设备。成千上万的实验开发的药物影响神经系统,一些以非常特殊的方式。大脑活动的记录可以使用电极进行,如在脑电图研究中粘在头皮上,或者植入动物的脑内以进行细胞外记录,这可以检测单个神经元产生的动作电位。[111]因为大脑不含有疼痛感受器,所以可以使用这些技术来记录清醒和行为而不会引起痛苦的动物的大脑活动。在医疗需要植入电极来定位导致癫痫发作的大脑区域的情况下,偶尔也会使用相同的技术来研究患有顽固性癫痫的人类患者的大脑活动。[112]功能性成像技术如功能性磁共振成像也用于研究大脑活动;这些技术主要用于人类受试者,因为它们需要有意识的受试者长时间不动,但它们具有非侵入性的巨大优势。[113]
绘图显示一只猴子在克制椅子,计算机显示器,机器人手臂和三件计算机设备,它们之间用箭头显示信息流。
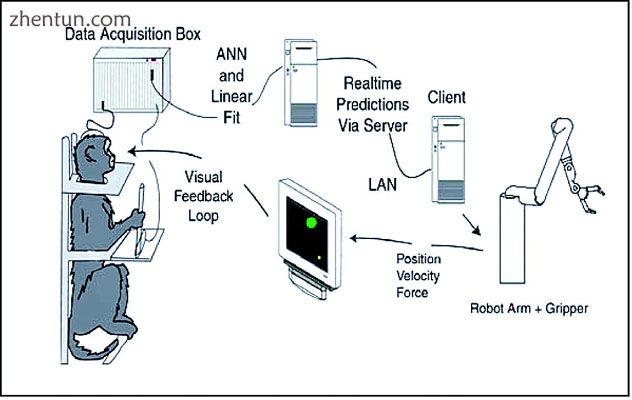
设计一个实验,其中猴子的大脑活动被用来控制机器人手臂。[114]
脑功能的另一种方法是检查特定脑区损伤的后果。即使它被头骨和脑膜保护,被脑脊液包围,并通过血脑屏障从血液中分离出来,大脑的微妙性质使其易受多种疾病和几种类型的损害。在人类中,中风和其他类型脑损伤的影响一直是关于大脑功能的重要信息来源。但是,由于无法通过实验控制损害的性质,因此这些信息通常难以解释。在动物研究中,最常见的是大鼠,可以使用电极或局部注射的化学物质来产生精确的损伤模式,然后检查行为的后果。[115]
计算神经科学包括两种方法:第一,使用计算机研究大脑;第二,研究大脑如何进行计算。一方面,可以通过利用描述其电化学活性的方程组来编写计算机程序来模拟一组神经元的操作;这种模拟被称为生物现实神经网络。另一方面,可以通过模拟或数学分析简化的“单元”的操作来研究神经计算的算法,这些“单元”具有神经元的一些特性但是抽象出它们的生物复杂性。计算机科学家和神经科学家研究了大脑的计算功能。[116]
计算神经发生模型涉及动态神经元模型的研究和开发,用于模拟基因和基因之间的动态相互作用的脑功能。
近年来,遗传和基因组技术在大脑研究中的应用越来越多[117],并且关注神经营养因子和身体活动在神经可塑性中的作用。[102] 由于技术工具的可用性,最常见的科目是老鼠。 现在可以相对容易地“敲除”或突变多种基因,然后检查对脑功能的影响。 还使用了更复杂的方法:例如,使用Cre-Lox重组,可以在特定时间激活或灭活大脑特定部位的基因。[117]
历史
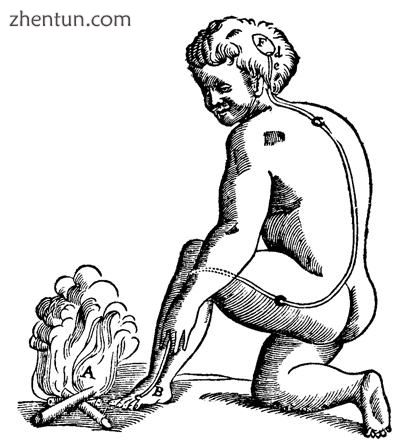
RenéDescartes关于大脑如何实现反射反应的插图。
另见:神经科学史
最古老的大脑是在亚美尼亚的Areni-1洞穴群中发现的。估计有5000多岁的大脑被发现在一个12到14岁的女孩的头骨上。虽然大脑萎缩,但由于洞穴内的气候,它们保存完好。[118]
早期哲学家对于灵魂的位置是在于大脑还是在心中存在分歧。亚里士多德赞成心脏,并认为大脑的功能仅仅是为了冷却血液。德谟克利特是物质原子理论的发明者,它主宰着一个由三部分组成的灵魂,头脑中有智力,心脏有情感,肝脏附近有欲望。[119] “神圣疾病”(The Sacred Disease)的未知作者,希波克拉底语语料库中的一篇医学论文,明确支持大脑,写道:
除了大脑,男人应该知道,除了大脑,快乐,欢乐,笑声和运动,以及悲伤,悲伤,沮丧和悲伤。 ......在同一个器官中,我们变得疯狂和神志不清,恐惧和恐惧袭击了我们,有些是夜晚,有些是白天,还有梦想和不合时宜的徘徊,以及不适合的关心,以及对当前情况的无知,解体和不熟练的。当它不健康的时候,我们忍受大脑所有这些东西......
关于神圣疾病,归功于希波克拉底[120]
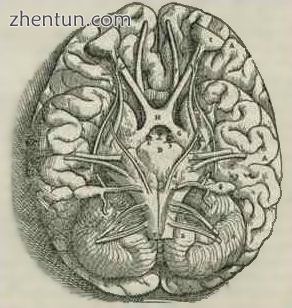
Andreas Vesalius'Fabrica,于1543年出版,展示了人类大脑的基础,包括视交叉,小脑,嗅球等。
罗马医生盖伦也主张大脑的重要性,并在一定程度上理论它如何起作用。盖伦追溯了大脑,神经和肌肉之间的解剖关系,证​​明身体的所有肌肉都通过分支的神经网络与大脑相连。他假定神经通过携带一种他称为pneumata psychikon的神秘物质机械地激活肌肉,通常被翻译为“动物精神”。[119]盖伦的思想在中世纪时期广为人知,但在文艺复兴时期,当详细的解剖学研究重新开始时,并没有取得太多进展,结合了勒内卡笛派和跟随他的人的理论推测。像盖伦一样,笛卡尔从水力学的角度思考神经系统。他认为,最高的认知功能是由非物质的res cogitans进行的,但人类的大部分行为以及动物的所有行为都可以用机械方式解释。[121]
然而,现代对神经功能的理解的第一个真正进展来自于Luigi Galvani(1737-1798)的调查,他发现施加在死青蛙暴露的神经上的静电冲击可能导致其腿收缩。从那时起,理解的每一次重大进步都或多或少直接来自于新的调查技术的发展。直到20世纪初,最重要的进展来自于染色细胞的新方法。[122]特别关键的是高尔基体染色的发明,其(当正确使用时)仅染色一小部分神经元,但整体染色它们,包括细胞体,树突和轴突。如果没有这样的染色,显微镜下的脑组织就会显示为原生质纤维的难以处理的混乱,其中不可能确定任何结构。在Camillo Golgi,特别是西班牙神经解剖学家SantiagoRamónyCajal的手中,新染色显示出数百种不同类型的神经元,每种神经元都有自己独特的树突结构和连接模式。[123]
在黄色纸上绘图与角落里的存档邮票。蜘蛛树分支结构连接到质量的顶部。一些狭窄的过程跟随质量的底部。
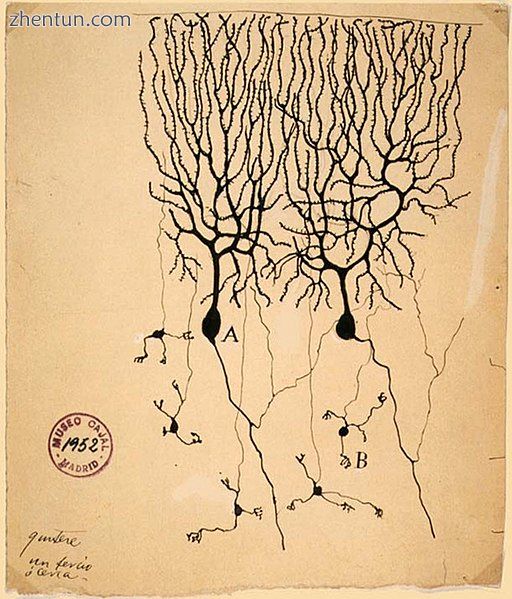
来自Santiago Ramon和Cajal的两只高尔基染色的神经元来自鸽子的小脑。
在20世纪上半叶,电子技术的进步使得能够调查神经细胞的电学特性,最终由Alan Hodgkin,Andrew Huxley和其他人研究动作电位的生物物理学,以及Bernard Katz和其他人的工作。关于突触的电化学。[124]这些研究补充了解剖学图像,其中大脑是一个动态实体。 1942年,查尔斯·谢林顿(Charles Sherrington)反映了新的理解,想象了大脑从睡眠中醒来的运作方式:
大质量的最顶层,几乎没有光线闪烁或移动,现在成为一个闪闪发光的节奏闪光点,火车上的火车匆匆赶往。大脑正在醒来,随之而来的是大脑正在回归。就像银河系进入一些宇宙舞蹈一样。很快,头部质量成为一个迷人的织机,数以百万计的闪光梭子编织出一种溶解模式,总是一种有意义的模式,尽管从来不是一种持久的模式;子模式的和谐变化。
-Sherrington,1942,Man on his nature [125]
20世纪40年代电子计算机的发明,以及数学信息理论的发展,使人们认识到大脑可以被理解为信息处理系统。这一概念构成了控制论领域的基础,并最终产生了现在被称为计算神经科学的领域。[126]最早的控制论尝试有些粗糙,因为他们将大脑视为伪装的数字计算机,例如John von Neumann 1958年出版的“计算机与大脑”一书。[127]然而,多年来,积累关于从行为动物记录的脑细胞电响应的信息已经稳步地将理论概念推向了增加现实主义的方向。[126]
最具影响力的早期贡献之一是1959年的一篇题为青蛙的眼睛告诉青蛙大脑的文章:该论文检查了青蛙视网膜和视顶盖中神经元的视觉反应,并得出结论:顶盖中的一些神经元。青蛙被连线起来,以一种使它们充当“虫子感知者”的方式结合基本反应。[128]几年后,David Hubel和Torsten Wiesel在猴子的初级视觉皮层中发现了细胞,这些细胞在锐边移动到视野中的特定点时变得活跃 - 这一发现为他们赢得了诺贝尔奖。[129]高阶视觉区域的后续研究发现了检测双眼视差,颜色,运动和形状方面的细胞,区域距离初级视觉皮层越来越远,显示出越来越复杂的反应。[130]对视觉无关的大脑区域的其他研究表明,细胞具有多种反应相关性,一些与记忆相关,一些与抽象类型的认知相关,如空间。[131]
理论家通过构建神经元和神经网络的数学模型,努力了解这些反应模式,这些模型可以使用计算机进行模拟。[126]一些有用的模型是抽象的,侧重于神经算法的概念结构,而不是它们如何在大脑中实现的细节;其他模型试图纳入有关真实神经元的生物物理特性的数据。[132]然而,任何级别的模型都不被认为是对脑功能的完全有效的描述。基本的困难是神经网络的复杂计算需要分布式处理,其中数百或数千个神经元协同工作 - 目前的大脑活动记录方法一次只能隔离几十个神经元的动作电位。[133]
此外,即使是单个神经元似乎也很复杂,并且能够进行计算。[134]因此,不能反映这一点的大脑模型过于抽象,无法代表大脑的运作;试图捕获这种模型的模型在计算上非常昂贵,并且可以说是目前的计算资源难以处理。然而,人脑项目正试图建立一个整个人类大脑的现实,详细的计算模型。这种方法的智慧受到了公开的争论,双方的高调科学家都在争论中。
在20世纪下半叶,化学,电子显微镜,遗传学,计算机科学,功能性脑成像等领域的发展逐渐为大脑结构和功能开辟了新的窗口。在美国,20世纪90年代被正式指定为“大脑十年”,以纪念大脑研究取得的进展,并促进此类研究的资助。[135]
在21世纪,这些趋势仍在继续,并且一些新的方法已经变得突出,包括多电极记录,其允许同时记录许多脑细胞的活动; [136]基因工程,其允许分子组分通过实验改变的大脑; [117]基因组学,它允许大脑结构的变化与DNA特性[137]和神经影像学的变化相关联。
其他用途
作为食物

Gulai otak,牛的咖喱来自印度尼西亚
动物的大脑在许多美食中被用作食物。
在仪式中
一些考古证据表明,欧洲尼安德特人的哀悼仪式也涉及大脑的消耗。[138]
众所周知,巴布亚新几内亚的前人吃人的大脑。 在丧葬仪式中,那些靠近死者的人会吃掉死者的大脑,以创造一种不朽的感觉。 一种名为库鲁的朊病毒病已被追溯到此。[139]
另见
Brain–computer interface
Central nervous system disease
List of neuroscience databases
Neurological disorder
Optogenetics
Outline of neuroscience
参考
Saladin, Kenneth (2011). Human anatomy (3rd ed.). McGraw-Hill. p. 416. ISBN 978-0-07-122207-5.
von Bartheld, CS; Bahney, J; Herculano-Houzel, S (15 December 2016). "The search for true numbers of neurons and glial cells in the human brain: A review of 150 years of cell counting". The Journal of Comparative Neurology. 524 (18): 3865–3895. doi:10.1002/cne.24040. PMC 5063692. PMID 27187682.
Yuste, Rafael; Church, George M. (March 2014). "The new century of the brain" (PDF). Scientific American. 310 (3): 38–45. Bibcode:2014SciAm.310c..38Y. doi:10.1038/scientificamerican0314-38. PMID 24660326. Archived from the original (PDF) on 2014-07-14.
Shepherd, GM (1994). Neurobiology. Oxford University Press. p. 3. ISBN 978-0-19-508843-4.
Sporns, O (2010). Networks of the Brain. MIT Press. p. 143. ISBN 978-0-262-01469-4.
Başar, E (2010). Brain-Body-Mind in the Nebulous Cartesian System: A Holistic Approach by Oscillations. Springer. p. 225. ISBN 978-1-4419-6134-1.
Singh, I (2006). "A Brief Review of the Techniques Used in the Study of Neuroanatomy". Textbook of Human Neuroanatomy. Jaypee Brothers. p. 24. ISBN 978-81-8061-808-6.
Kandel, Eric R.; Schwartz, James Harris; Jessell, Thomas M. (2000). Principles of neural science. New York: McGraw-Hill. ISBN 978-0-8385-7701-1. OCLC 42073108.
Douglas, RJ; Martin, KA (2004). "Neuronal circuits of the neocortex". Annual Review of Neuroscience. 27: 419–451. doi:10.1146/annurev.neuro.27.070203.144152. PMID 15217339.
Barnett, MW; Larkman, PM (2007). "The action potential". Practical Neurology. 7 (3): 192–197. PMID 17515599.
Shepherd, GM (2004). "Ch. 1: Introduction to synaptic circuits". The Synaptic Organization of the Brain. Oxford University Press US. ISBN 978-0-19-515956-1.
Williams, RW; Herrup, K (1988). "The control of neuron number". Annual Review of Neuroscience. 11: 423–453. doi:10.1146/annurev.ne.11.030188.002231. PMID 3284447.
Heisenberg, M (2003). "Mushroom body memoir: from maps to models". Nature Reviews Neuroscience. 4 (4): 266–275. doi:10.1038/nrn1074. PMID 12671643.
Jacobs, DK; Nakanishi, N; Yuan, D; et al. (2007). "Evolution of sensory structures in basal metazoa". Integrative and Comparative Biology. 47 (5): 712–723. doi:10.1093/icb/icm094. PMID 21669752.
Balavoine, G (2003). "The segmented Urbilateria: A testable scenario". Integrative and Comparative Biology. 43 (1): 137–147. doi:10.1093/icb/43.1.137. PMID 21680418.
Schmidt-Rhaesa, A (2007). The Evolution of Organ Systems. Oxford University Press. p. 110. ISBN 978-0-19-856669-4.
Kristan Jr, WB; Calabrese, RL; Friesen, WO (2005). "Neuronal control of leech behavior". Prog Neurobiol. 76 (5): 279–327. doi:10.1016/j.pneurobio.2005.09.004. PMID 16260077.
Barnes, RD (1987). Invertebrate Zoology (5th ed.). Saunders College Pub. p. 1. ISBN 978-0-03-008914-5.
Butler, AB (2000). "Chordate Evolution and the Origin of Craniates: An Old Brain in a New Head". Anatomical Record. 261 (3): 111–125. doi:10.1002/1097-0185(20000615)261:3<111::AID-AR6>3.0.CO;2-F. PMID 10867629.
Bulloch, TH; Kutch, W (1995). "Are the main grades of brains different principally in numbers of connections or also in quality?". In Breidbach O. The nervous systems of invertebrates: an evolutionary and comparative approach. Birkhäuser. p. 439. ISBN 978-3-7643-5076-5.
"Flybrain: An online atlas and database of the drosophila nervous system". Archived from the original on 1998-01-09. Retrieved 2011-10-14.
Konopka, RJ; Benzer, S (1971). "Clock Mutants of Drosophila melanogaster". Proc. Natl. Acad. Sci. U.S.A. 68 (9): 2112–2116. Bibcode:1971PNAS...68.2112K. doi:10.1073/pnas.68.9.2112. PMC 389363. PMID 5002428.
Shin, Hee-Sup; et al. (1985). "An unusual coding sequence from a Drosophila clock gene is conserved in vertebrates". Nature. 317 (6036): 445–448. Bibcode:1985Natur.317..445S. doi:10.1038/317445a0. PMID 2413365.
Heisenberg, M; Heusipp, M; Wanke, C. (1995). "Structural plasticity in the Drosophila brain". J. Neurosci. 15 (3): 1951–1960. doi:10.1523/JNEUROSCI.15-03-01951.1995.
"WormBook: The online review of C. elegans biology". Retrieved 2011-10-14.
Hobert, O (2005). The C. elegans Research Community, ed. "Specification of the nervous system". WormBook: 1–19. doi:10.1895/wormbook.1.12.1. PMC 4781215. PMID 18050401.
White, JG; Southgate, E; Thomson, JN; Brenner, S (1986). "The Structure of the Nervous System of the Nematode Caenorhabditis elegans". Philosophical Transactions of the Royal Society B. 314 (1165): 1–340. Bibcode:1986RSPTB.314....1W. doi:10.1098/rstb.1986.0056. PMID 22462104.
Jabr, Ferris (2012-10-02). "The Connectome Debate: Is Mapping the Mind of a Worm Worth It?". Scientific American. Retrieved 2014-01-18.
Hodgkin, J (2001). "Caenorhabditis elegans". In Brenner S, Miller JH. Encyclopedia of Genetics. Elsevier. pp. 251–256. ISBN 978-0-12-227080-2.
Kandel, ER (2007). In Search of Memory: The Emergence of a New Science of Mind. WW Norton. pp. 145–150. ISBN 978-0-393-32937-7.
Shu, D.-G.; Conway Morris, S.; Han, J.; Zhang, Z.-F.; Yasui, K.; Janvier, P.; Chen, L.; Zhang, X.-L.; Liu, J.-N.; et al. (2003). "Head and backbone of the Early Cambrian vertebrate Haikouichthys". Nature. 421 (6922): 526–529. Bibcode:2003Natur.421..526S. doi:10.1038/nature01264. PMID 12556891.
Striedter, GF (2005). "Ch. 3: Conservation in vertebrate brains". Principles of Brain Evolution. Sinauer Associates. ISBN 978-0-87893-820-9.
Armstrong, E (1983). "Relative brain size and metabolism in mammals". Science. 220 (4603): 1302–1304. Bibcode:1983Sci...220.1302A. doi:10.1126/science.6407108. PMID 6407108.
Jerison, HJ (1973). Evolution of the Brain and Intelligence. Academic Press. pp. 55–74. ISBN 978-0-12-385250-2.
Parent, A; Carpenter, MB (1995). "Ch. 1". Carpenter's Human Neuroanatomy. Williams & Wilkins. ISBN 978-0-683-06752-1.
Pardridge, W (2005). "The Blood-Brain Barrier: Bottleneck in Brain Drug Development". NeuroRx. 2 (1): 3–14. doi:10.1602/neurorx.2.1.3. PMC 539316. PMID 15717053.
Northcutt, RG (2008). "Forebrain evolution in bony fishes". Brain Research Bulletin. 75 (2–4): 191–205. doi:10.1016/j.brainresbull.2007.10.058. PMID 18331871.
Reiner, A; Yamamoto, K; Karten, HJ (2005). "Organization and evolution of the avian forebrain". The Anatomical Record Part A: Discoveries in Molecular, Cellular, and Evolutionary Biology. 287 (1): 1080–1102. doi:10.1002/ar.a.20253. PMID 16206213.
Siegel, A; Sapru, HN (2010). Essential Neuroscience. Lippincott Williams & Wilkins. pp. 184–189. ISBN 978-0-7817-8383-5.
Swaab, DF; Boller, F; Aminoff, MJ (2003). The Human Hypothalamus. Elsevier. ISBN 978-0-444-51357-1.
Jones, EG (1985). The Thalamus. Plenum Press. ISBN 978-0-306-41856-3.
Knierim, James (2015). "Cerebellum" (Section 3, Chapter 5) Neuroscience Online. Department of Neurobiology and Anatomy – The University of Texas Medical School at Houston.
Saitoh, K; Ménard, A; Grillner, S (2007). "Tectal control of locomotion, steering, and eye movements in lamprey". Journal of Neurophysiology. 97 (4): 3093–3108. doi:10.1152/jn.00639.2006. PMID 17303814.
Richard Swann Lull; Harry Burr Ferris; George Howard Parker; James Rowland Angell; Albert Galloway Keller; Edwin Grant Conklin (1922). The evolution of man: a series of lectures delivered before the Yale chapter of the Sigma xi during the academic year 1921–1922. Yale University Press. p. 50.
Puelles, L (2001). "Thoughts on the development, structure and evolution of the mammalian and avian telencephalic pallium". Philosophical Transactions of the Royal Society B. 356 (1414): 1583–1598. doi:10.1098/rstb.2001.0973. PMC 1088538. PMID 11604125.
Salas, C; Broglio, C; Rodríguez, F (2003). "Evolution of forebrain and spatial cognition in vertebrates: conservation across diversity". Brain, Behavior and Evolution. 62 (2): 72–82. doi:10.1159/000072438. PMID 12937346.
Grillner, S; et al. (2005). "Mechanisms for selection of basic motor programs—roles for the striatum and pallidum". Trends in Neurosciences. 28 (7): 364–370. doi:10.1016/j.tins.2005.05.004. PMID 15935487.
Northcutt, RG (1981). "Evolution of the telencephalon in nonmammals". Annual Review of Neuroscience. 4: 301–350. doi:10.1146/annurev.ne.04.030181.001505. PMID 7013637.
Northcutt, RG (2002). "Understanding vertebrate brain evolution". Integrative and Comparative Biology. 42 (4): 743–756. doi:10.1093/icb/42.4.743. PMID 21708771.
Barton, RA; Harvey, PH (2000). "Mosaic evolution of brain structure in mammals". Nature. 405 (6790): 1055–1058. Bibcode:2000Natur.405.1055B. doi:10.1038/35016580. PMID 10890446.
Aboitiz, F; Morales, D; Montiel, J (2003). "The evolutionary origin of the mammalian isocortex: Towards an integrated developmental and functional approach". Behavioral and Brain Sciences. 26 (5): 535–552. doi:10.1017/S0140525X03000128. PMID 15179935. Archived from the original on 2008-08-07.
Romer, AS; Parsons, TS (1977). The Vertebrate Body. Holt-Saunders International. p. 531. ISBN 978-0-03-910284-5.
Roth, G; Dicke, U (2005). "Evolution of the brain and Intelligence". Trends in Cognitive Sciences. 9 (5): 250–257. doi:10.1016/j.tics.2005.03.005. PMID 15866152.
Marino, Lori (2004). "Cetacean Brain Evolution: Multiplication Generates Complexity" (PDF). International Society for Comparative Psychology (17): 1–16. Retrieved 2010-08-29.
Shoshani, J; Kupsky, WJ; Marchant, GH (2006). "Elephant brain Part I: Gross morphology, functions, comparative anatomy, and evolution". Brain Research Bulletin. 70 (2): 124–157. doi:10.1016/j.brainresbull.2006.03.016. PMID 16782503.
Finlay, BL; Darlington, RB; Nicastro, N (2001). "Developmental structure in brain evolution". Behavioral and Brain Sciences. 24 (2): 263–308. doi:10.1017/S0140525X01003958. PMID 11530543.
Calvin, WH (1996). How Brains Think. Basic Books. ISBN 978-0-465-07278-1.
Sereno, MI; Dale, AM; Reppas, AM; Kwong, KK; Belliveau, JW; Brady, TJ; Rosen, BR; Tootell, RBH (1995). "Borders of multiple visual areas in human revealed by functional magnetic resonance imaging" (PDF). Science. 268 (5212): 889–893. Bibcode:1995Sci...268..889S. doi:10.1126/science.7754376. PMID 7754376.
Fuster, JM (2008). The Prefrontal Cortex. Elsevier. pp. 1–7. ISBN 978-0-12-373644-4.
Purves, Dale.; Lichtman, Jeff W. (1985). Principles of neural development. Sunderland, Mass.: Sinauer Associates. ISBN 978-0-87893-744-8. OCLC 10798963.
Wong, R (1999). "Retinal waves and visual system development". Annual Review of Neuroscience. 22: 29–47. doi:10.1146/annurev.neuro.22.1.29. PMID 10202531.
Rakic, P (2002). "Adult neurogenesis in mammals: an identity crisis". Journal of Neuroscience. 22 (3): 614–618. doi:10.1523/JNEUROSCI.22-03-00614.2002. PMID 11826088.
Ridley, M (2003). Nature via Nurture: Genes, Experience, and What Makes Us Human. Forth Estate. pp. 1–6. ISBN 978-0-06-000678-5.
Wiesel, T (1982). "Postnatal development of the visual cortex and the influence of environment" (PDF). Nature. 299 (5884): 583–591. Bibcode:1982Natur.299..583W. CiteSeerX 10.1.1.547.7497. doi:10.1038/299583a0. PMID 6811951.
van Praag, H; Kempermann, G; Gage, FH (2000). "Neural consequences of environmental enrichment". Nature Reviews Neuroscience. 1 (3): 191–198. doi:10.1038/35044558. PMID 11257907.
Cooper, JR; Bloom, FE; Roth, RH (2003). The Biochemical Basis of Neuropharmacology. Oxford University Press US. ISBN 978-0-19-514008-8.
McGeer, PL; McGeer, EG (1989). "Chapter 15, Amino acid neurotransmitters". In G. Siegel; et al. Basic Neurochemistry. Raven Press. pp. 311–332. ISBN 978-0-88167-343-2.
Foster, AC; Kemp, JA (2006). "Glutamate- and GABA-based CNS therapeutics". Current Opinion in Pharmacology. 6 (1): 7–17. doi:10.1016/j.coph.2005.11.005. PMID 16377242.
Frazer, A; Hensler, JG (1999). "Understanding the neuroanatomical organization of serotonergic cells in the brain provides insight into the functions of this neurotransmitter". In Siegel, GJ. Basic Neurochemistry (Sixth ed.). Lippincott Williams & Wilkins. ISBN 978-0-397-51820-3.
Mehler, MF; Purpura, DP (2009). "Autism, fever, epigenetics and the locus coeruleus". Brain Research Reviews. 59 (2): 388–392. doi:10.1016/j.brainresrev.2008.11.001. PMC 2668953. PMID 19059284.
Rang, HP (2003). Pharmacology. Churchill Livingstone. pp. 476–483. ISBN 978-0-443-07145-4.
Speckmann, E-J; Elger, CE (2004). "Introduction to the neurophysiological basis of the EEG and DC potentials". In Niedermeyer E, Lopes da Silva FH. Electroencephalography: Basic Principles, Clinical Applications, and Related Fields. Lippincott Williams & Wilkins. pp. 17–31. ISBN 978-0-7817-5126-1.
Buzsáki, G (2006). Rhythms of the Brain. Oxford University Press. ISBN 978-0-19-530106-9. OCLC 63279497.
Nieuwenhuys, R; Donkelaar, HJ; Nicholson, C (1998). The Central Nervous System of Vertebrates, Volume 1. Springer. pp. 11–14. ISBN 978-3-540-56013-5.
Safi, K; Seid, MA; Dechmann, DK (2005). "Bigger is not always better: when brains get smaller". Biology Letters. 1 (3): 283–286. doi:10.1098/rsbl.2005.0333. PMC 1617168. PMID 17148188.
Mink, JW; Blumenschine, RJ; Adams, DB (1981). "Ratio of central nervous system to body metabolism in vertebrates: its constancy and functional basis". American Journal of Physiology (Submitted manuscript). 241 (3): R203–212. doi:10.1152/ajpregu.1981.241.3.R203. PMID 7282965.
Raichle, M; Gusnard, DA (2002). "Appraising the brain's energy budget". Proc. Natl. Acad. Sci. U.S.A. 99 (16): 10237–10239. Bibcode:2002PNAS...9910237R. doi:10.1073/pnas.172399499. PMC 124895. PMID 12149485.
Mehagnoul-Schipper, DJ; Van Der Kallen, BF; Colier, WNJM; Van Der Sluijs, MC; Van Erning, LJ; Thijssen, HO; Oeseburg, B; Hoefnagels, WH; Jansen, RW (2002). "Simultaneous measurements of cerebral oxygenation changes during brain activation by near-infrared spectroscopy and functional magnetic resonance imaging in healthy young and elderly subjects". Hum Brain Mapp. 16 (1): 14–23. doi:10.1002/hbm.10026. PMID 11870923.
Ebert, D.; Haller, RG.; Walton, ME. (Jul 2003). "Energy contribution of octanoate to intact rat brain metabolism measured by 13C nuclear magnetic resonance spectroscopy". J Neurosci. 23 (13): 5928–5935. doi:10.1523/JNEUROSCI.23-13-05928.2003. PMID 12843297.
Marin-Valencia, I.; Good, LB.; Ma, Q.; Malloy, CR.; Pascual, JM. (Feb 2013). "Heptanoate as a neural fuel: energetic and neurotransmitter precursors in normal and glucose transporter I-deficient (G1D) brain". J Cereb Blood Flow Metab. 33 (2): 175–182. doi:10.1038/jcbfm.2012.151. PMC 3564188. PMID 23072752.
Boumezbeur, F.; Petersen, KF.; Cline, GW.; Mason, GF.; Behar, KL.; Shulman, GI.; Rothman, DL. (Oct 2010). "The contribution of blood lactate to brain energy metabolism in humans measured by dynamic 13C nuclear magnetic resonance spectroscopy". J Neurosci. 30 (42): 13983–13991. doi:10.1523/JNEUROSCI.2040-10.2010. PMC 2996729. PMID 20962220.
Deelchand, DK.; Shestov, AA.; Koski, DM.; Uğurbil, K.; Henry, PG. (May 2009). "Acetate transport and utilization in the rat brain". J Neurochem. 109 Suppl 1 (Suppl 1): 46–54. doi:10.1111/j.1471-4159.2009.05895.x. PMC 2722917. PMID 19393008.
Soengas, JL; Aldegunde, M (2002). "Energy metabolism of fish brain". Comparative Biochemistry and Physiology B. 131 (3): 271–296. doi:10.1016/S1096-4959(02)00022-2. PMID 11959012.
Carew, TJ (2000). "Ch. 1". Behavioral Neurobiology: the Cellular Organization of Natural Behavior. Sinauer Associates. ISBN 978-0-87893-092-0.
Dafny, N. "Anatomy of the spinal cord". Neuroscience Online. Archived from the original on 2011-10-08. Retrieved 2011-10-10.
Dragoi, V. "Ocular motor system". Neuroscience Online. Archived from the original on 2011-11-17. Retrieved 2011-10-10.
Gurney, K; Prescott, TJ; Wickens, JR; Redgrave, P (2004). "Computational models of the basal ganglia: from robots to membranes". Trends in Neurosciences. 27 (8): 453–459. doi:10.1016/j.tins.2004.06.003. PMID 15271492.
Shima, K; Tanji, J (1998). "Both supplementary and presupplementary motor areas are crucial for the temporal organization of multiple movements". Journal of Neurophysiology. 80 (6): 3247–3260. doi:10.1152/jn.1998.80.6.3247. PMID 9862919.
Miller, EK; Cohen, JD (2001). "An integrative theory of prefrontal cortex function". Annual Review of Neuroscience. 24 (1): 167–202. doi:10.1146/annurev.neuro.24.1.167. PMID 11283309.
Antle, MC; Silver, R (2005). "Orchestrating time: arrangements of the brain circadian clock" (PDF). Trends in Neurosciences. 28 (3): 145–151. doi:10.1016/j.tins.2005.01.003. PMID 15749168. Archived from the original (PDF) on 2008-10-31.
Kleitman, N (1938). Sleep and Wakefulness. revised 1963, reprinted 1987. The University of Chicago Press, Midway Reprints series. ISBN 978-0-226-44073-6.
Dougherty, P. "Hypothalamus: structural organization". Neuroscience Online. Archived from the original on 2011-11-17. Retrieved 2011-10-11.
Gross, CG (1998). "Claude Bernard and the constancy of the internal environment" (PDF). The Neuroscientist. 4 (5): 380–385. doi:10.1177/107385849800400520.
Dougherty, P. "Hypothalamic control of pituitary hormone". Neuroscience Online. Archived from the original on 2011-11-17. Retrieved 2011-10-11.
Chiel, HJ; Beer, RD (1997). "The brain has a body: adaptive behavior emerges from interactions of nervous system, body, and environment". Trends in Neurosciences. 20 (12): 553–557. doi:10.1016/S0166-2236(97)01149-1. PMID 9416664.
Berridge, KC (2004). "Motivation concepts in behavioral neuroscience". Physiology & Behavior. 81 (2): 179–209. doi:10.1016/j.physbeh.2004.02.004. PMID 15159167.
Ardiel, EL; Rankin, CH (2010). "An elegant mind: learning and memory in Caenorhabditis elegans". Learning and Memory. 17 (4): 191–201. doi:10.1101/lm.960510. PMID 20335372.
Hyman, SE; Malenka, RC (2001). "Addiction and the brain: the neurobiology of compulsion and its persistence". Nature Reviews Neuroscience. 2 (10): 695–703. doi:10.1038/35094560. PMID 11584307.
Ramón y Cajal, S (1894). "The Croonian Lecture: La Fine Structure des Centres Nerveux". Proceedings of the Royal Society. 55 (331–335): 444–468. doi:10.1098/rspl.1894.0063.
Lømo, T (2003). "The discovery of long-term potentiation". Philosophical Transactions of the Royal Society B. 358 (1432): 617–620. doi:10.1098/rstb.2002.1226. PMC 1693150. PMID 12740104.
Malenka, R; Bear, M (2004). "LTP and LTD: an embarrassment of riches". Neuron. 44 (1): 5–21. doi:10.1016/j.neuron.2004.09.012. PMID 15450156.
Bos, I; De Boever, P; Int Panis, L; Meeusen, R (August 2014). "Physical Activity, Air Pollution and the Brain". Sports Medicine. 44 (11): 1505–1518. doi:10.1007/s40279-014-0222-6. PMID 25119155.
Curtis, CE; D'Esposito, M (2003). "Persistent activity in the prefrontal cortex during working memory". Trends in Cognitive Sciences. 7 (9): 415–423. CiteSeerX 10.1.1.457.9723. doi:10.1016/S1364-6613(03)00197-9. PMID 12963473.
Tulving, E; Markowitsch, HJ (1998). "Episodic and declarative memory: role of the hippocampus". Hippocampus. 8 (3): 198–204. doi:10.1002/(SICI)1098-1063(1998)8:3<198::AID-HIPO2>3.0.CO;2-G. PMID 9662134.
Martin, A; Chao, LL (2001). "Semantic memory and the brain: structures and processes". Current Opinion in Neurobiology. 11 (2): 194–201. doi:10.1016/S0959-4388(00)00196-3. PMID 11301239.
Balleine, BW; Liljeholm, Mimi; Ostlund, SB (2009). "The integrative function of the basal ganglia in instrumental learning". Behavioural Brain Research. 199 (1): 43–52. doi:10.1016/j.bbr.2008.10.034. PMID 19027797.
Doya, K (2000). "Complementary roles of basal ganglia and cerebellum in learning and motor control". Current Opinion in Neurobiology. 10 (6): 732–739. doi:10.1016/S0959-4388(00)00153-7. PMID 11240282.
Storrow, Hugh A. (1969). Outline of clinical psychiatry. New York: Appleton-Century-Crofts, Educational Division. ISBN 978-0-390-85075-1. OCLC 47198.
Thagard, P (2008). Zalta, EN, ed. "Cognitive Science". The Stanford Encyclopedia of Philosophy. Retrieved 2011-10-14.
Bear, MF; Connors, BW; Paradiso, MA (2007). "Ch. 2". Neuroscience: Exploring the Brain. Lippincott Williams & Wilkins. ISBN 978-0-7817-6003-4.
Dowling, JE (2001). Neurons and Networks. Harvard University Press. pp. 15–24. ISBN 978-0-674-00462-7.
Wyllie, E; Gupta, A; Lachhwani, DK (2005). "Ch. 77". The Treatment of Epilepsy: Principles and Practice. Lippincott Williams & Wilkins. ISBN 978-0-7817-4995-4.
Laureys, S; Boly, M; Tononi, G (2009). "Functional neuroimaging". In Laureys S, Tononi G. The Neurology of Consciousness: Cognitive Neuroscience and Neuropathology. Academic Press. pp. 31–42. ISBN 978-0-12-374168-4.
Carmena, JM; et al. (2003). "Learning to Control a Brain–Machine Interface for Reaching and Grasping by Primates". PLoS Biology. 1 (2): 193–208. doi:10.1371/journal.pbio.0000042. PMC 261882. PMID 14624244.
Kolb, B; Whishaw, I (2008). "Ch. 1". Fundamentals of Human Neuropsychology. Macmillan. ISBN 978-0-7167-9586-5.
Abbott, LF; Dayan, P (2001). "Preface". Theoretical Neuroscience: Computational and Mathematical Modeling of Neural Systems. MIT Press. ISBN 978-0-262-54185-5.
Tonegawa, S; Nakazawa, K; Wilson, MA (2003). "Genetic neuroscience of mammalian learning and memory". Philosophical Transactions of the Royal Society B. 358 (1432): 787–795. doi:10.1098/rstb.2002.1243. PMC 1693163. PMID 12740125.
Bower, Bruce (12 January 2009). "Armenian cave yields ancient human brain". ScienceNews.
Finger, S (2001). Origins of Neuroscience. Oxford University Press. pp. 14–15. ISBN 978-0-19-514694-3.
*Hippocrates (2006) [400 BCE], On the Sacred Disease, Translated by Francis Adams, Internet Classics Archive: The University of Adelaide Library, archived from the original on September 26, 2007
Finger, S (2001). Origins of Neuroscience. Oxford University Press. pp. 193–195. ISBN 978-0-19-514694-3.
Bloom, FE (1975). Schmidt FO, Worden FG, Swazey JP, Adelman G, eds. The Neurosciences, Paths of Discovery. MIT Press. p. 211. ISBN 978-0-262-23072-8.
Shepherd, GM (1991). "Ch.1 : Introduction and Overview". Foundations of the Neuron Doctrine. Oxford University Press. ISBN 978-0-19-506491-9.
Piccolino, M (2002). "Fifty years of the Hodgkin-Huxley era". Trends in Neurosciences. 25 (11): 552–553. doi:10.1016/S0166-2236(02)02276-2. PMID 12392928.
Sherrington, CS (1942). Man on his nature. Cambridge University Press. p. 178. ISBN 978-0-8385-7701-1.
Churchland, PS; Koch, C; Sejnowski, TJ (1993). "What is computational neuroscience?". In Schwartz EL. Computational Neuroscience. MIT Press. pp. 46–55. ISBN 978-0-262-69164-2.
von Neumann, J; Churchland, PM; Churchland, PS (2000). The Computer and the Brain. Yale University Press. pp. xi–xxii. ISBN 978-0-300-08473-3.
Lettvin, JY; Maturana, HR; McCulloch, WS; Pitts, WH (1959). "What the frog's eye tells the frog's brain" (PDF). Proceedings of the Institute of Radio Engineers. 47 (11): 1940–1951. doi:10.1109/jrproc.1959.287207. Archived from the original (PDF) on 2011-09-28.
Hubel, DH; Wiesel, TN (2005). Brain and visual perception: the story of a 25-year collaboration. Oxford University Press US. pp. 657–704. ISBN 978-0-19-517618-6.
Farah, MJ (2000). The Cognitive Neuroscience of Vision. Wiley-Blackwell. pp. 1–29. ISBN 978-0-631-21403-8.
Engel, AK; Singer, W (2001). "Temporal binding and the neural correlates of sensory awareness". Trends in Cognitive Sciences. 5 (1): 16–25. doi:10.1016/S1364-6613(00)01568-0. PMID 11164732.
Dayan, P; Abbott, LF (2005). "Ch.7: Network models". Theoretical Neuroscience. MIT Press. ISBN 978-0-262-54185-5.
Averbeck, BB; Lee, D (2004). "Coding and transmission of information by neural ensembles". Trends in Neurosciences. 27 (4): 225–230. doi:10.1016/j.tins.2004.02.006. PMID 15046882.
Forrest, MD (2014). "Intracellular Calcium Dynamics Permit a Purkinje Neuron Model to Perform Toggle and Gain Computations Upon its Inputs". Frontiers in Computational Neuroscience. 8: 86. doi:10.3389/fncom.2014.00086. PMC 4138505. PMID 25191262.
Jones, EG; Mendell, LM (1999). "Assessing the Decade of the Brain". Science. 284 (5415): 739. Bibcode:1999Sci...284..739J. doi:10.1126/science.284.5415.739. PMID 10336393.
Buzsáki, G (2004). "Large-scale recording of neuronal ensembles" (PDF). Nature Neuroscience. 7 (5): 446–451. doi:10.1038/nn1233. PMID 15114356. Archived from the original (PDF) on 2006-09-10.
Geschwind, DH; Konopka, G (2009). "Neuroscience in the era of functional genomics and systems biology". Nature. 461 (7266): 908–915. Bibcode:2009Natur.461..908G. doi:10.1038/nature08537. PMC 3645852. PMID 19829370.
Connell, Evan S. (2001). The Aztec Treasure House. Counterpoint Press. ISBN 978-1-58243-162-8.
Collins, S; McLean CA; Masters CL (2001). "Gerstmann-Straussler-Scheinker syndrome, fatal familial insomnia, and kuru: a review of these less common human transmissible spongiform encephalopathies". Journal of Clinical Neuroscience. 8 (5): 387–397. doi:10.1054/jocn.2001.0919. PMID 11535002. |