子宫内膜是哺乳动物子宫的内上皮层及其粘膜。 它有一个基层和一个功能层; 功能层变厚,然后在月经期间流下人类和其他一些哺乳动物,包括猿猴,旧世界猴子,某些种类的蝙蝠和大象 .. [1] 在大多数其他哺乳动物中,子宫内膜在动情周期中被重吸收。 在怀孕期间,子宫内膜的腺体和血管的大小和数量进一步增加。 血管空间融合并相互连接,形成胎盘,为胚胎和胎儿提供氧气和营养。[2] [3] 推测存在子宫内膜微生物群[4]已被反对。[5] [6]
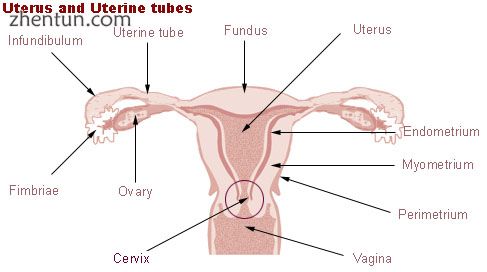
子宫和输卵管。 (子宫内膜标记在中右侧。)
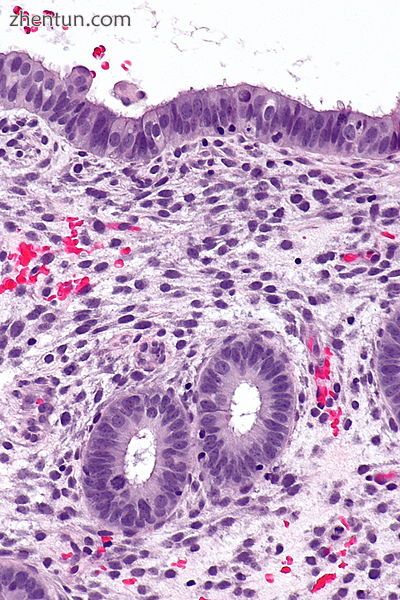
子宫内膜处于增生期
目录
1 结构
1.1 基因和蛋白质表达
1.2 微生物群的推测
2 功能
2.1 周期
3 与子宫内膜有关的疾病
3.1 胚胎移植
4 附加图像
5 参考
结构
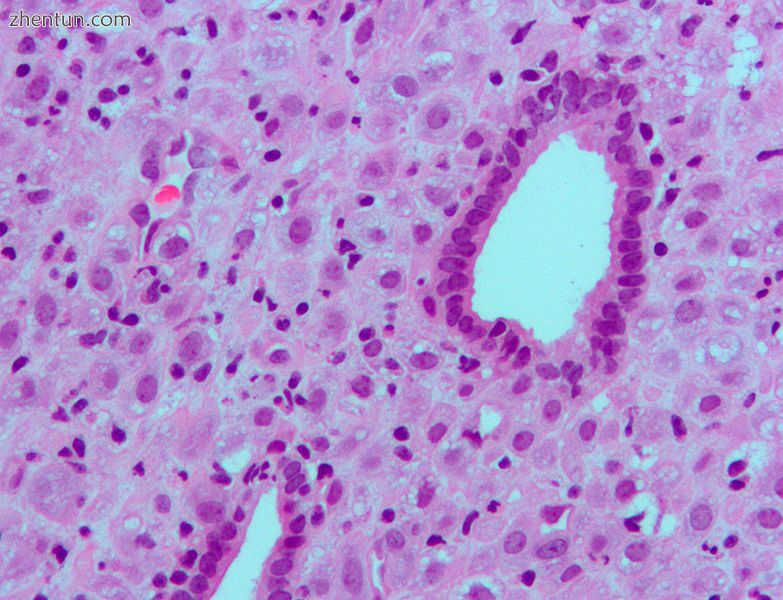
由外源性黄体酮(口服避孕药)引起的蜕膜化子宫内膜的高倍放大显微照片。 H&E染色
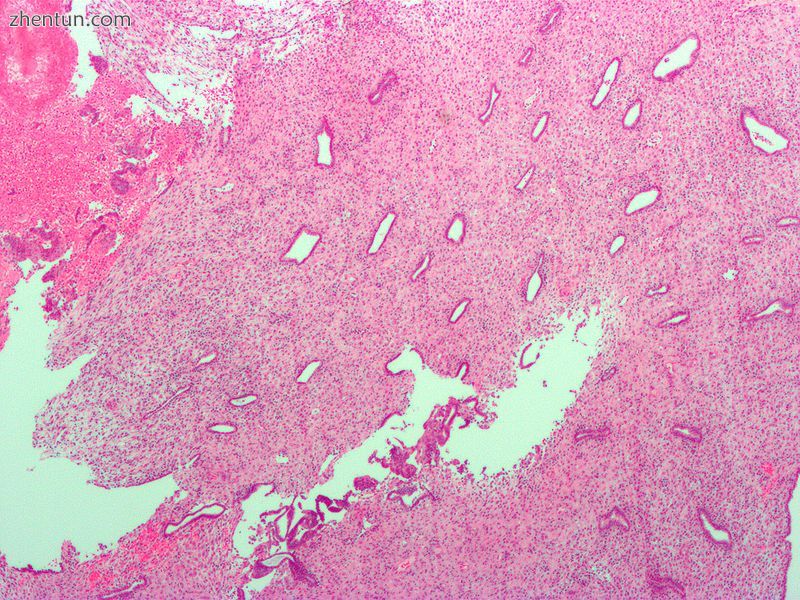
蜕膜化子宫内膜的低倍放大显微照片。 H&E染色
子宫内膜由单层柱状上皮加上其所在的基质组成。基质是一层结缔组织,其厚度根据激素的影响而变化。在子宫中,简单的管状腺体从子宫内膜表面到达基质的基部,其也携带由螺旋动脉提供的丰富的血液供应。在育龄妇女中,可以区分两层子宫内膜。这两层仅存在于子宫腔内的子宫内膜中,而不存在于输卵管的内层。[2] [3]
功能层与子宫腔相邻。这层是在月经周期的第一部分月经结束后建立起来的。雌激素(月经周期的卵泡期)诱导增殖,并且该层中的后期变化由来自黄体(黄体期)的黄体酮产生。它适于为胚胎的植入和生长提供最佳环境。这层在月经期间完全脱落。
与子宫肌层相邻且在功能层下方的基底层在月经周期期间的任何时间都不会脱落。功能层在其上发展。
在没有黄体酮的情况下,向功能层供血的动脉收缩,使得该层中的细胞变得缺血并死亡,导致月经。
通过观察每个阶段的微观差异,例如在卵巢周期中,可以通过参考卵巢周期或子宫周期来识别月经周期的阶段:
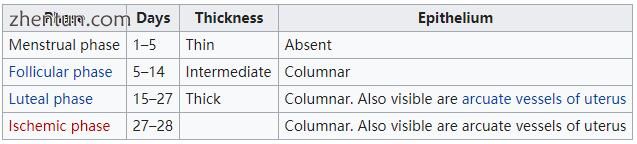
基因和蛋白质表达
更多信息:生物信息学§基因和蛋白质表达
大约20,000个蛋白质编码基因在人类细胞中表达,其中约70%在正常子宫内膜中表达[7] [8]。这些基因中只有100多个在子宫内膜中更具特异性地表达,只有极少数基因具有高度子宫内膜特异性。相应的特异性蛋白质在子宫内膜粘膜的腺体和基质细胞中表达。许多这些蛋白质的表达根据月经周期而变化,例如在增殖期表达的孕酮受体和促甲状腺激素释放激素,以及在分泌期表达的PAEP。女性生育所需的其他蛋白质如HOX11蛋白质在整个月经周期的子宫内膜基质细胞中表达。某些特定蛋白质如雌激素受体也在其他类型的女性组织中表达,如子宫颈,输卵管,卵巢和乳房。[9]
微生物群的猜测
子宫和子宫内膜长期以来被认为是无菌的。观察到粘膜的宫颈塞防止任何从阴道上升的微生物进入。在20世纪80年代,当显示子宫感染可能是由宫颈栓塞屏障的弱点引起时,这种观点受到挑战。来自阴道微生物群的生物可以在月经周期的子宫收缩期间进入子宫。进一步的研究旨在确定子宫特有的微生物群,这将有助于识别IVF和流产不成功的病例。由于采用的采样程序可能存在交叉污染,他们的研究结果被认为是不可靠的。例如,有充分证明存在的乳杆菌属物种很容易解释为阴道群体能够渗入宫颈粘液中。[5]另一项研究强调了早期研究的缺陷,包括交叉污染。还有人认为,使用无菌动物的无菌后代(无菌)的研究证据清楚地表明了子宫的不育性。作者得出结论,鉴于这些发现,没有微生物组。[6]
乳酸杆菌在阴道中的正常优势被视为阴道健康的标志。然而,在子宫中,这种低得多的人群在被女性性激素高度调节的封闭环境中被视为侵入性的,并且可能产生不良后果。在子宫内膜异位症的研究中,乳杆菌不是主要类型,并且存在更高水平的链球菌和葡萄球菌物种。一半的细菌性阴道炎病例显示多微生物生物膜附着在子宫内膜上。[5]
功能
子宫内膜是子宫的最内层衬里层,其功能是防止子宫肌层的相对壁之间的粘连,从而保持子宫腔的开放性。在月经周期或动情周期中,子宫内膜生长成厚的,富含血管的腺体组织层。这代表了胚泡到达子宫时植入的最佳环境。子宫内膜是中央的,回声的(使用超声波扫描仪可检测),平均厚度为6.7 mm。
在怀孕期间,子宫内膜的腺体和血管的大小和数量进一步增加。血管空间融合并相互连接,形成胎盘,为胚胎和胎儿提供氧气和营养。
周期
子宫内膜经历循环再生。人类,类人猿和其他一些物种表现出月经周期,而大多数其他哺乳动物则经历了发情周期。[1]在这两种情况下,子宫内膜最初在雌激素的影响下增殖。然而,一旦排卵发生,卵巢(特别是黄体)将产生更大量的黄体酮。这将子宫内膜的增殖模式改变为分泌衬里。最终,分泌衬里为一个或多个胚泡提供了一个好客的环境。
受精后,卵子可以植入子宫壁,并用人绒毛膜促性腺激素(HCG)向身体提供反馈。 HCG通过维持黄体提供持续的整个怀孕反馈,黄体将继续其释放黄体酮和雌激素的作用。子宫内膜内层要么被重吸收(月经周期),要么脱落(月经周期)。在后一种情况下,脱落过程涉及内层的破坏,小结缔血管的撕裂,以及通过阴道构成的组织和血液的损失。整个过程在几天的时间内发生。月经可伴有一系列子宫收缩;这些有助于驱逐月经子宫内膜。
然而,在植入的情况下,子宫内膜既不被吸收也不被脱落。相反,它仍然是蜕膜。蜕膜成为胎盘的一部分;它为妊娠提供支持和保护。
如果衬里刺激不足,由于缺乏激素,子宫内膜仍然很薄而且不活跃。在人类中,这将导致闭经或没有月经期。更年期后,内层通常被描述为萎缩。相反,长期暴露于雌激素而不是黄体酮的子宫内膜可能会变得增生。长期使用含有高效孕激素的口服避孕药也会诱发子宫内膜萎缩[10] [11]。
在人类中,建立和脱落子宫内膜的周期平均持续28天。子宫内膜在不同哺乳动物中以不同的速率发育。包括季节,气候和压力在内的各种因素都会影响其发展。子宫内膜本身在周期的不同阶段产生某些激素,这会影响生殖系统的其他部分。
与子宫内膜有关的疾病
绒毛膜组织可导致明显的子宫内膜变化,称为Arias-Stella反应,其外观与癌症相似[12]。从历史上看,这种变化被诊断为子宫内膜癌,只有在不应被误诊为癌症时才具有重要意义。
子宫腺肌病是子宫内膜生长到子宫肌层(子宫肌层)。
子宫内膜异位症是子宫外的子宫内膜组织的生长。
子宫内膜增生
子宫内膜癌是人类女性生殖道中最常见的癌症。
当子宫内膜的基底层被仪器(例如D&C)或感染(例如子宫内膜结核)损坏导致子宫内膜硬化和部分或完全消除子宫腔的粘连形成时,发生Asherman综合征,也称为子宫内粘连。
薄的子宫内膜可以定义为小于8mm的子宫内膜厚度。它通常发生在绝经后。可以改善子宫内膜厚度的治疗方法包括维生素E,L-精氨酸和柠檬酸西地那非。[13]
使用cDNA微阵列的基因表达谱可用于诊断子宫内膜疾病。[14]欧洲更年期和男性更年期协会(EMAS)发布了指南,其中包含评估子宫内膜的详细信息。 [15]
胚胎移植
与EMT超过7mm相比,子宫内膜厚度小于7mm会降低体外受精的妊娠率,比值比约为0.4。然而,这种低厚度很少发生,并且任何常规使用该参数都被认为是不合理的。[16]
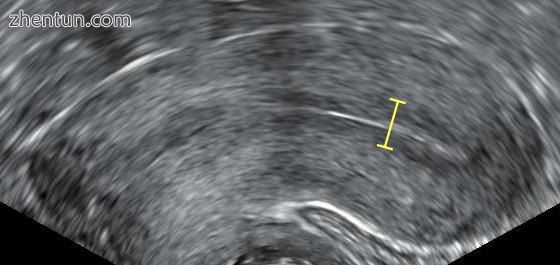
三线子宫内膜,长7mm。
在施用生育药物时,例如在体外受精中,使用经阴道超声检查观察子宫内膜。 在胚胎移植时,有利的是,子宫内膜的厚度在7到14毫米之间,具有三线结构,[17]这意味着子宫内膜含有高回声(通常显示为光)线。 中间被两条低回声(较暗)线包围。 三线子宫内膜反映了基底层和功能层的分离,并且在继发于雌二醇水平升高的排卵期后也观察到,并且在排卵后消失[18]。
其他图片
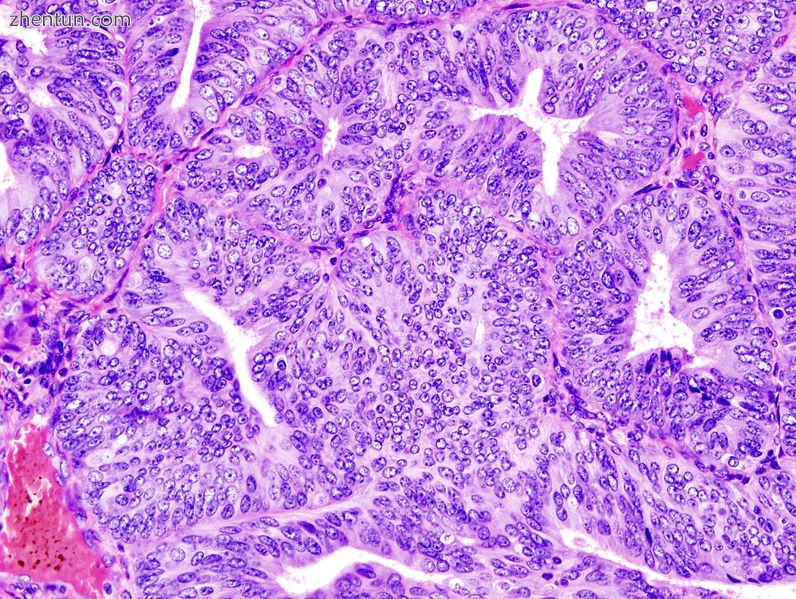
来自活组织检查的子宫内膜样腺癌。 H&E染色。
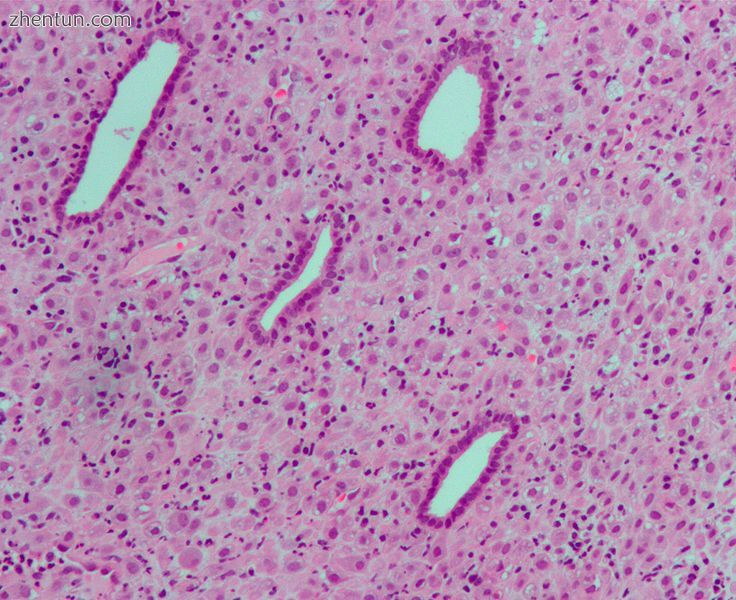
由外源性孕酮引起的蜕膜化子宫内膜的显微照片。 H&E染色。
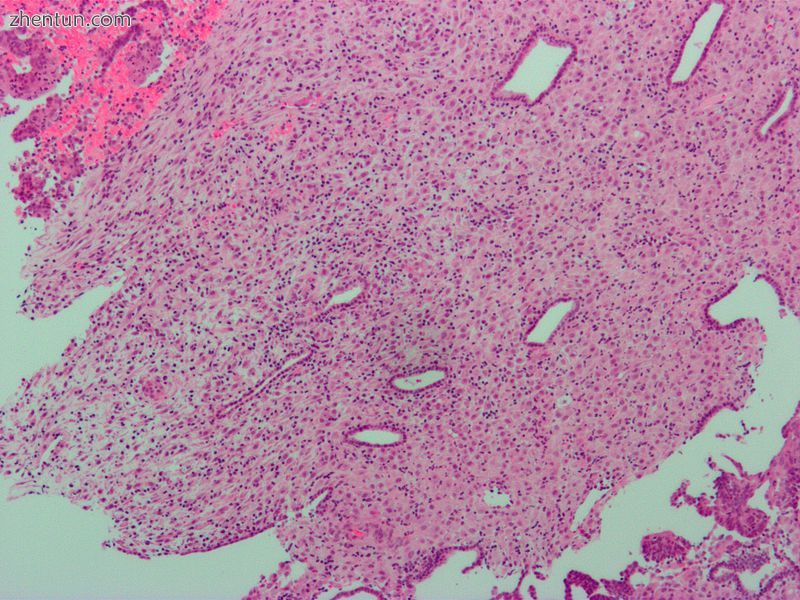
由外源性孕酮引起的蜕膜化子宫内膜的显微照片。 H&E染色。
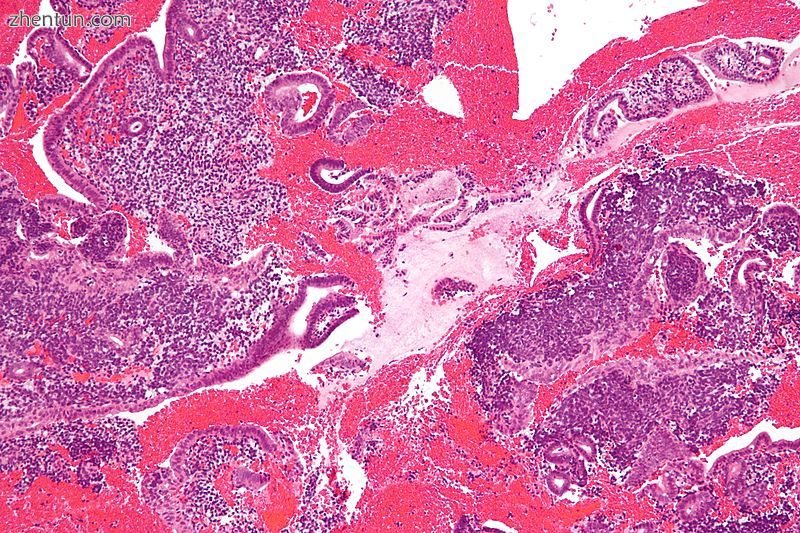
显微照片显示子宫内膜间质凝结,这是月经中的一个发现。
另见
CYTL1, also known as cytokine-like like protein 1.
参考
Emera, D; Romero, R; Wagner, G (January 2012). "The evolution of menstruation: a new model for genetic assimilation: explaining molecular origins of maternal responses to fetal invasiveness". BioEssays. 34 (1): 26–35. doi:10.1002/bies.201100099. PMC 3528014. PMID 22057551.
Blue Histology - Female Reproductive System. School of Anatomy and Human Biology — The University of Western Australia Accessed 20061228 20:35
Guyton AC and Hall JE, eds. (2006). "Chapter 81 Female Physiology Before Pregnancy and Female Hormones". Textbook of Medical Physiology (11th ed.). Elsevier Saunders. pp. 1018ff. ISBN 9780721602400.
Franasiak, Jason M.; Scott, Richard T. (2015). "Reproductive tract microbiome in assisted reproductive technologies". Fertility and Sterility. 104 (6): 1364–1371. doi:10.1016/j.fertnstert.2015.10.012. ISSN 0015-0282. PMID 26597628.
Baker, JM; Chase, DM; Herbst-Kralovetz, MM (2018). "Uterine Microbiota: Residents, Tourists, or Invaders?". Frontiers in Immunology. 9: 208. doi:10.3389/fimmu.2018.00208. PMID 29552006.
Perez-Muñoz, ME; Arrieta, MC; Ramer-Tait, AE; Walter, J (28 April 2017). "A critical assessment of the "sterile womb" and "in utero colonization" hypotheses: implications for research on the pioneer infant microbiome". Microbiome. 5 (1): 48. doi:10.1186/s40168-017-0268-4. PMID 28454555.
"The human proteome in endometrium - The Human Protein Atlas". www.proteinatlas.org. Retrieved 2017-09-25.
Uhlén, Mathias; Fagerberg, Linn; Hallström, Björn M.; Lindskog, Cecilia; Oksvold, Per; Mardinoglu, Adil; Sivertsson, Åsa; Kampf, Caroline; Sjöstedt, Evelina (2015-01-23). "Tissue-based map of the human proteome". Science. 347 (6220): 1260419. doi:10.1126/science.1260419. ISSN 0036-8075. PMID 25613900.
Zieba, Agata; Sjöstedt, Evelina; Olovsson, Matts; Fagerberg, Linn; Hallström, Björn M.; Oskarsson, Linda; Edlund, Karolina; Tolf, Anna; Uhlen, Mathias (2015-10-21). "The Human Endometrium-Specific Proteome Defined by Transcriptomics and Antibody-Based Profiling". OMICS: A Journal of Integrative Biology. 19 (11): 659–668. doi:10.1089/omi.2015.0115.
Deligdisch, L. (1993). "Effects of hormone therapy on the endometrium". Modern Pathology. 6 (1): 94–106. PMID 8426860.
William's Gynecology, McGraw 2008, Chapter 8, Abnormal Uterine Bleeding
Arias-Stella, J. (Jan 2002). "The Arias-Stella reaction: facts and fancies four decades after". Adv Anat Pathol. 9 (1): 12–23. doi:10.1097/00125480-200201000-00003. PMID 11756756.
Takasaki A, Tamura H, Miwa I, Taketani T, Shimamura K, Sugino N (April 2010). "Endometrial growth and uterine blood flow: a pilot study for improving endometrial thickness in the patients with a thin endometrium". Fertil. Steril. 93 (6): 1851–8. doi:10.1016/j.fertnstert.2008.12.062. PMID 19200982.
Tseng, L.; Chen, I.; Chen, M.; Yan, H.; Wang, C.; Lee, C. (2010). "Genome-based expression profiling as a single standardized microarray platform for the diagnosis of endometrial disorder: an array of 126-gene model". Fertility and Sterility. 94 (1): 114–119. doi:10.1016/j.fertnstert.2009.01.130. PMID 19328470.
Dreisler E, Poulsen LG, Antonsen SL, Ceausu I, Depypere H, Erel CT, Lambrinoudaki I, Pérez-López FR, Simoncini T, Tremollieres F, Rees M, Ulrich LG (2013). "EMAS clinical guide: Assessment of the endometrium in peri and postmenopausal women". Maturita. 75 (2): 181–90. doi:10.1016/j.maturitas.2013.03.011. PMID 23619009.
Kasius, A.; Smit, J. G.; Torrance, H. L.; Eijkemans, M. J. C.; Mol, B. W.; Opmeer, B. C.; Broekmans, F. J. M. (2014). "Endometrial thickness and pregnancy rates after IVF: a systematic review and meta-analysis". Human Reproduction Update. 20 (4): 530–541. doi:10.1093/humupd/dmu011. ISSN 1355-4786.
Zhao, Jing; Zhang, Qiong; Li, Yanping (2012). "The effect of endometrial thickness and pattern measured by ultrasonography on pregnancy outcomes during IVF-ET cycles". Reproductive Biology and Endocrinology. 10 (1): 100. doi:10.1186/1477-7827-10-100. ISSN 1477-7827. PMC 3551825.
Baerwald, A. R.; Pierson, R. A. (2004). "Endometrial development in association with ovarian follicular waves during the menstrual cycle". Ultrasound in Obstetrics and Gynecology. 24 (4): 453–460. doi:10.1002/uog.1123. ISSN 0960-7692. PMC 2891966. |