肺纤维化(字面意思是“肺部瘢痕”)是一种呼吸系统疾病,其中在肺组织中形成瘢痕,导致严重的呼吸问题。 瘢痕形成,过量纤维结缔组织的积聚(称为纤维化的过程),导致壁增厚,并导致血液中的氧供应减少。 因此,患者患有持续的呼吸短促。[1]
在一些患者中,可以诊断该疾病的具体原因,但在其他患者中可能无法确定可能的原因,这种情况称为特发性肺纤维化。 由于肺纤维化,没有已知的治疗方法可以治愈肺部的疤痕和损伤。[2]
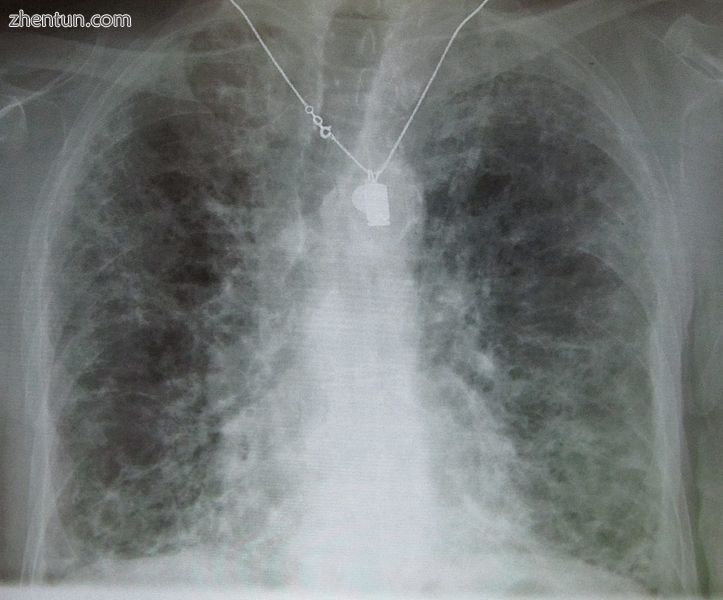
胸部X光片显示肺纤维化被认为是胺碘酮引起的。
目录
1 症状和体征
2 原因
3 发病机制
4 诊断
5 治疗
6 预后
7 流行病学
8 参考
体征和症状
肺纤维化的症状主要是:[3]
呼吸短促,尤其是劳累
慢性干燥,黑客咳嗽
疲劳和虚弱
胸部不适包括胸痛
食欲不振,体重迅速减轻
肺纤维化表现为进行性呼吸短促(呼吸困难)伴发作用的病史。在听诊时,肺基部有时会听到精细的吸气性噼啪声。胸部X光检查可能有也可能没有异常,但高分辨率CT常常表现出异常。[2]
原因
进一步的信息:间质性肺病
肺纤维化可能是其他疾病的继发效应。其中大多数被归类为间质性肺病。例子包括自身免疫性疾病,病毒感染和结核病等细菌感染,这可能导致肺部上叶或下叶的纤维化改变以及肺部的其他显微损伤。然而,肺纤维化也可以在没有任何已知原因的情况下出现。在这种情况下,它被称为“特发性”。[4]大多数特发性病例被诊断为特发性肺纤维化。这是诊断排除一组特征性的组织学/病理学特征,称为常见的间质性肺炎(UIP)。在任何一种情况下,越来越多的证据表明一部分患者存在遗传易感性。例如,已发现表面活性蛋白C(SP-C)的突变存在于一些有肺纤维化病史的家庭中[5]。在编码端粒酶的TERC或TERT基因中的常染色体显性突变已经在大约15%的肺纤维化患者中被鉴定出来。[6]
可能导致肺纤维化作为次要影响的疾病和病症包括:[2] [5]
吸入环境和职业污染物,如金属[7]石棉沉滞症,矽肺病和接触某些气体。煤矿工人,船舶工人和爆破者等风险更高。[4]
过敏性肺炎,最常见的原因是吸入被细菌,真菌或动物产品污染的粉尘。
吸烟会增加风险或使病情恶化。[4]
一些典型的结缔组织疾病[4]如类风湿性关节炎,SLE和硬皮病
其他涉及结缔组织的疾病,如结节病和肉芽肿伴多血管炎。
感染
某些药物,例如胺碘酮,博来霉素(平阳霉素),白消安,甲氨蝶呤,[4]阿扑吗啡,[8]和呋喃妥因[9]
对胸部进行放射治疗
发病
更多信息:纤维化
肺纤维化涉及正常肺实质与纤维化组织的逐渐交换。用瘢痕组织代替正常肺导致氧扩散能力的不可逆转的降低,由此导致的僵硬或依从性降低使肺纤维化成为限制性肺病。[10]肺纤维化由异常的伤口愈合而非慢性炎症延续。[11]它是肺实质内在的限制性肺病的主要原因。相反,四肢瘫痪[12]和脊柱后凸[13]是限制性肺病的原因的例子,其不一定涉及肺纤维化。
诊断
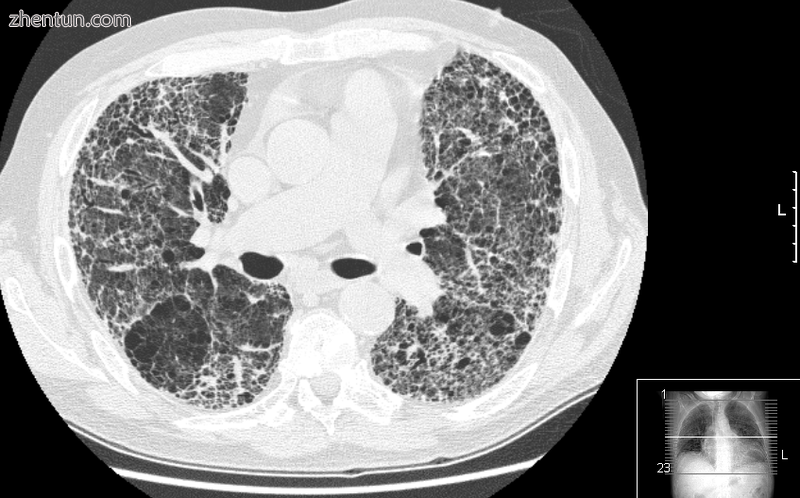
肺部HRCT显示可能来自常见间质性肺炎的广泛纤维化。还有一个大的肺气肿大疱。
肺活组织检查可以确诊[2]。全身麻醉下的视频辅助胸腔镜楔形活检(VATS)可能是获得足够组织以进行准确诊断所必需的。这种活组织检查涉及通过胸壁放置几个管,其中一个用于切断一块肺以进行评估。通过显微镜检查取出的组织进行组织病理学检查,以确认纤维化的存在和模式以及可能表明特定原因的其他特征的存在。特定类型的矿物粉尘或对治疗的可能反应,例如一种所谓的非特异性间质纤维化模式。[2]
误诊是常见的,因为尽管整体肺纤维化并不罕见,但每种类型的肺纤维化并不常见,对这些疾病患者的评估很复杂,需要采用多学科方法。术语已经标准化,但在应用中仍然存在困难。即使是专家也可能不同意某些案件的分类。[14]
在肺活量测定中,作为一种限制性肺病,FEV1(1秒内用力呼气量)和FVC(用力肺活量)均降低,因此FEV1 / FVC比值正常甚至增加,而阻塞性肺病则与此比例相同。降低。在限制性肺病中,残余体积和总肺容量的值通常会降低[15]。
治疗
肺纤维化会产生疤痕组织。疤痕一旦发展就是永久性的。[2]减缓进展和预防取决于根本原因:
特发性肺纤维化的治疗选择非常有限。尽管正在进行研究试验,但没有证据表明任何药物可以显着改善这种情况。肺移植是严重病例中唯一可用的治疗选择。由于某些类型的肺纤维化可以对皮质类固醇(例如泼尼松)和/或其他抑制身体免疫系统的药物产生反应,因此这些类型的药物有时被用于试图减缓导致纤维化的过程。
感觉免疫系统在许多形式的肺纤维化的发展中起重要作用。用免疫抑制剂如皮质类固醇治疗的目的是减少肺部炎症和随后的瘢痕形成。对治疗的反应是可变的。那些因免疫抑制治疗而病情好转的人可能没有特发性肺纤维化,因为特发性肺纤维化没有明显的治疗或治愈方法。
旨在预防轻度特发性纤维化瘢痕形成的两种药物是吡非尼酮,它可降低FVC 1年下降率的降低。吡非尼酮也减少了6分钟步行试验的距离下降,但对呼吸道症状没有影响。[16]第二种药物是nintedanib,它起抗纤维化作用,通过抑制多种酪氨酸激酶受体(包括血小板衍生生长因子,成纤维细胞生长因子和血管内皮生长因子)介导。[17]一项随机临床试验表明,它可以减少肺功能下降和急性发作[18]。
抗炎剂在减少纤维化过程方面仅取得有限的成功。一些其他类型的纤维化,例如非特异性间质性肺炎,可能对免疫抑制治疗如皮质类固醇有反应。然而,只有少数患者单独使用皮质类固醇,因此可以使用其他免疫抑制剂,例如环磷酰胺,硫唑嘌呤,甲氨蝶呤,青霉胺和环孢菌素。秋水仙碱的使用也很有限。[2]目前正在进行使用新药物如IFN-γ和霉酚酸酯的试验。
过敏性肺炎是一种不太严重的肺纤维化形式,可以通过避免接触致病物质来防止其加重。
补氧可以改善生活质量和运动能力。某些患者可考虑进行肺移植[19]。
预测
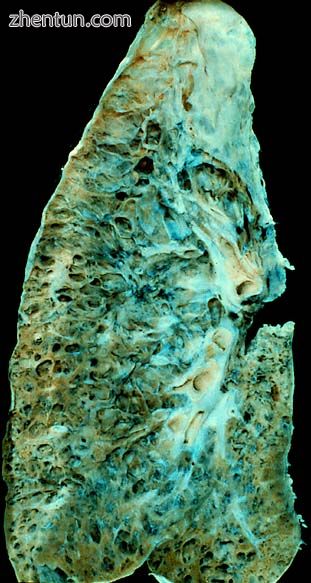
尸检时肺部有终末期肺纤维化
肺纤维化引起的缺氧可导致肺动脉高压,进而可导致右心室心力衰竭。 补充氧气可以预防缺氧。[2]
肺纤维化也可能导致肺栓塞的风险增加,这可以通过抗凝剂来预防[2]。
流行病学
全世界有500万人患有肺纤维化。 据报道,肺纤维化的发病率和患病率范围很广。 以下比率为每100,000中1人,范围分别反映了狭义和广泛的纳入标准。
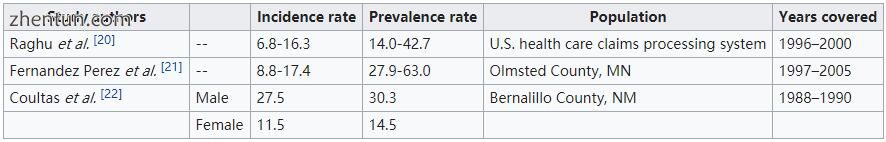
根据这些比率,根据2000年18岁或以上的人口,美国的肺纤维化患病率可能超过29,000到近132,000。 由于误诊,实际数字可能会显着增加。 通常情况下,患者在诊断时已达到四十和五十岁,而特发性肺纤维化的发病率在五十岁后急剧增加。 然而,肺功能丧失通常归因于老年,心脏病或更常见的肺部疾病。
参考
Mayo Clinic Staff. "Definition [of pulmonary fibrosis]". Mayo Foundation for Medical Education and Research. Archived from the original on 15 July 2014. Retrieved 26 July 2014.
"Pulmonary Fibrosis". MedicineNet, Inc. Archived from the original on 19 July 2014. Retrieved 26 July 2014.
Mayo Clinic Staff. "Symptoms". Mayo Foundation for Medical Education and Research. Archived from the original on 4 July 2014. Retrieved 26 July 2014.
MedlinePlus > Pulmonary Fibrosis Archived 5 July 2016 at the Wayback Machine Date last updated: 9 February 2010
Mayo Clinic Staff. "Causes". Mayo Foundation for Medical Education and Research. Archived from the original on 1 October 2014. Retrieved 26 July 2014.
"Idiopathic pulmonary fibrosis".
Hubbard R, Cooper M, Antoniak M, et al. (2000). "Risk of cryptogenic fibrosing alveolitis in metal workers". Lancet. 355 (9202): 466–467. doi:10.1016/S0140-6736(00)82017-6. PMID 10841131.
"Not Found - BIDMC". bidmc.org. Archived from the original on 16 March 2014. Retrieved 29 April 2018.
Goemaere NN, Grijm K, van Hal PT, den Bakker MA (2008). "Nitrofurantoin-induced pulmonary fibrosis: a case report". J Med Case Reports. 2: 169. doi:10.1186/1752-1947-2-169. PMC 2408600. PMID 18495029. Archived from the original on 6 March 2016.
Mayo Clinic Staff. "Complications". Mayo Foundation for Medical Education and Research. Archived from the original on 4 July 2014. Retrieved 26 July 2014.
Gross TJ, Hunninghake GW (2001). "Idiopathic pulmonary fibrosis". N Engl J Med. 345 (7): 517–525. doi:10.1056/NEJMra003200. PMC 2231521.
Walker J, Cooney M, Norton S (August 1989). "Improved pulmonary function in chronic quadriplegics after pulmonary therapy and arm ergometry". Paraplegia. 27 (4): 278–83. doi:10.1038/sc.1989.42. PMID 2780083.
eMedicine Specialties > Pulmonology > Interstitial Lung Diseases > Restrictive Lung Disease Archived 5 March 2010 at the Wayback Machine Author: Lalit K Kanaparthi, MD, Klaus-Dieter Lessnau, MD, Sat Sharma, MD. Updated: 27 July 2009
Mayo Clinic Staff. "Tests and diagnosis". Mayo Foundation for Medical Education and Research. Archived from the original on 4 July 2014. Retrieved 26 July 2014.
"www.spirXpert.com". Archived from the original on 28 January 2010.
King TE Jr; Bradford WZ; Castro-Bernardini S; et al. (May 2014). "A phase 3 trial of pirfenidone in patients with idiopathic pulmonary fibrosis". NEJM. 370 (22): 2083–2092. doi:10.1056/NEJMoa1402582. PMID 24836312.
Richeldi L, Costabel U, Selman M, et al. (2011). "Efficacy of a tyrosine kinase inhibitor in idiopathic pulmonary fibrosis". N Engl J Med. 365 (12): 1079–1087. doi:10.1056/nejmoa1103690. PMID 21992121.
Richeldi L, du Bois RM, Raghu G, et al. (May 2014). "Efficacy and Safety of Nintedanib in Idiopathic Pulmonary Fibrosis". N Engl J Med. 370 (22): 2071–2082. doi:10.1056/NEJMoa1402584. PMID 24836310.
Mayo Clinic Staff. "Lifestyle and home remedies". Mayo Foundation for Medical Education and Research. Archived from the original on 4 July 2014. Retrieved 26 July 2014.
Raghu G, Weycker D, Edelsberg J, Bradford WZ, Oster G. Incidence and Prevalence of Idiopathic Pulmonary Fibrosis. Am J Respir Crit Care Med. 2006;174:810-6.
Fernandez Perez ER, Daniels CE, Schroeder DR, St Sauver J, Hartman TE, Bartholmai BJ, Yi ES, Ryu JH. Incidence, Prevalence, and Clinical Course of Idiopathic Pulmonary Fibrosis: A Population-Based Study. Chest. Jan 2010;137:129-37.
Coultas DB, Zumwalt RE, Black WC, Sobonya RE. The Epidemiology of Interstitial Lung Diseases. Am J Respir Crit Care Med. Oct 1994;150(4):967-72. cited by Michaelson JE, Aguayo SM, Roman J. Idiopathic Pulmonary Fibrosis: A Practical Approach for Diagnosis and Management. Chest. Sept 2000;118:788-94. |